HEMORRAGIA DIGESTIVA ALTA
Nivel contenido del Médico General: Diagnóstico sospecha, Tratamiento inicial, Seguimeinto derivar.
Definición
Se define hemorragia digestiva alta (HDA) como todo sangrado procedente de una lesión, en el tubo digestivo, proximal al ligamento de Treitz.
Epidemiologia
La HDA es aproximadamente 4 veces más frecuente que la Hemorragia digestiva baja. Representa una incidencia aproximada de 100 casos por 100.000 personas al año y su tasa de mortalidad varía entre un 6-10 %.
La HDA es 2 veces más frecuente en hombres que en mujeres, sin embargo, la mortalidad es similar en ambos grupos.
Etiología
La HDA se puede dividir, según su etiología, en variceal y no variceal, siendo esta distinción importante ya que el 80% de las HDA no variceales se detienen de manera espontánea, además tanto la mortalidad como la recidiva al año es menor en las HDA de etiología no variceal.
Etiologías más frecuentes:
- Ulceras 31-67%
- Varices 6-39%
- Erosiones gastroduodenales 2-18%
- Sd Mallory-Weiss 2-8%
- Esofagitis erosiva 1-13%
- Neoplasia 2-8%
- Ectasias vasculares 0-6%
- No identificado 5-14%
Manifestaciones clínicas
Los Hallazgos habituales a la historia incluyen debilidad, mareos y/o sincope asociado a hematemesis o melena.
- Melenas (70-80 %): heces negras, brillantes, pastosas, pegajosas, malolientes, como “petróleo”. Sugiere HDA o HDB con tránsito, se deben descartar alimentos que tiñan las heces.
- Hematemesis (40-50 %): vómito de sangre fresca o restos hemáticos digeridos (posos de café). Sugiere HDA, pero hay que descartar origen respiratorio (hemoptisis) u ORL tratándose de sangre deglutida.
- Hematoquecia (15-20 %): heces sanguinolentas. Sugiere HDB o HDA con tránsito rápido.
- Dolor epigástrico (41 %)
- Dispepsia (18 %)
- Sincope (14%)
- Baja de peso (12%)
- Ictericia (5,2%)
Manejo inicial
Estabilizar al paciente. Evaluar hemodinamia e iniciar medidas de reanimación necesarias según cuantía de sangrado. Transfundir GR en caso de necesidad, con un objetivo de Hb entre 7-9 g/dl (salvo pacientes con comorbilidades donde puede ser mayor. Ej Cardiopatía coronaria.
Laboratorio de urgencias: Hemograma, función renal, electrolitos plasmáticos, Pruebas hepáticas, Coagulación, Grupo sanguíneo ABO y Rh.
Corregir coagulopatias: PFC, Vit K para normaliza el tiempo de protrombina. Plaquetas hasta un recuento mayor a 50.000.
Continuar con manejo especifico según etiología variceal o no variceal:
- HDA no variceal:
Estratificación de riesgo: permite decidir que pacientes requieren endoscópica digestiva alta (EDA) de urgencia, quienes pueden esperar y quienes no requieren. Además, permite dar un pronóstico de mortalidad.
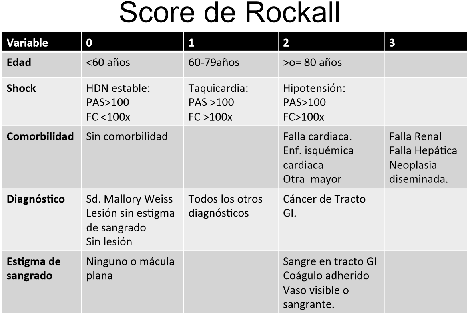
- Score Rockall: Excelente valor predictivo en términos de mortalidad. Impreciso en la predicción de resangrado. < 3 puntos excelente pronostico, > 8 elevada motalidad. Desventaja requiere EDA para cálculo de puntaje total.
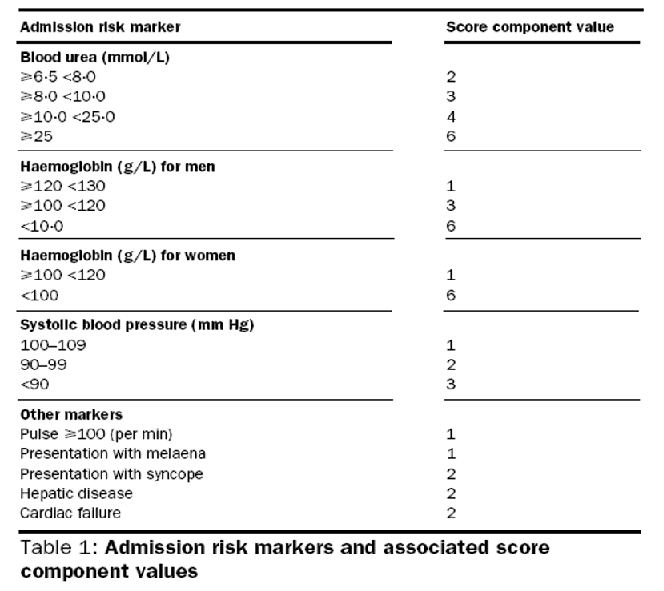
- Score Glasgow-Blatchford: redecir la necesidad de hospitalización y EDA terapeútica. Un puntaje menor o igual a 1 tienen menos de un 1% de requerir intervención y pueden ser dados de alta sin endoscopia para seguimiento y tratamiento ambulatorio.
- Clasificación de Forrest: Evaluación de la lesión que se estima provocó la HDA. Se aplica predominantemente a úlceras pépticas. El estigma se clasifica 6 tipos, dividido en 3 grupos.
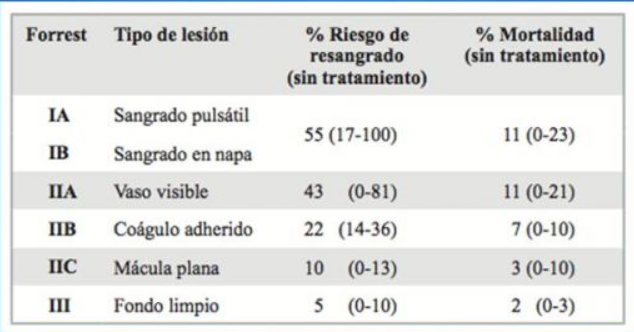
Estigmas de alto riesgo: Ia, Ib, IIa terapia endoscópica. Estigmas de bajo riesgo IIc y III sólo terapia médica. Estigma Forrest IIb decidir caso a caso, ofrecer terapia endoscópica al menos inyectoterapia con adrenalina de la base del coágulo.
Terapia medica: se basa en Inhibidores de bomba de protones (IBP) altas dosis: 80mg EV seguidos de infusión continua de 8mg/h por 72 horas o 40mg/6h EV. Su uso oral 40mg/12h post endoscopia ha demostrado beneficios comparables a EV. Aunque el uso de IBP no debe retrasar la EDA. Se puede utilizar Eritromicina 250 mg 30 a 120 min antes de la EDA permite mejorar visualización endoscópica en pacientes con sangrado severo. No se recomienda el uso rutinario de aspiración o lavado naso/oro-gástrico.
Terapia endoscópica: En forma inmediata en pacientes de alto riesgo (antes de 12 horas), el resto dentro de 24horas. Alternativas: Inyectoterapia con adrenalina (95% de hemostasia, 15-20% recidiva), termocoagulacion (electrocoagulación, sonda térmica, argón plasma), Terapia mecánica (clips hemostáticos). Se sugiere no utilizar inyectoterapia con adrenalina como monoterapia.
En Mallory Weiss la mayoría de los casos se resuelve el sangrado de manera espontánea. Ocasionalmente puede requerir inyectoterapia o métodos térmicos.
Las Malformaciones vasculares responden mejor a Termocoagulación (electrocoagulación, argón plasma).
Dieulafoy es difícil de diagnosticar y tratar. Puede responder a terapia mecánica (ligadura con bandas), inyectoterapia y métodos térmicos.
Indicaciones Quirúrgicas: Pueden variar entre distintos centros, pero en general son:
- Inestabilidad hemodinámica post reanimación
- Re-sangrado después de 2do intento endoscópico
- Vaso sangrante que no puede ser controlado por EDA
- Indicación co-existente de cirugía (neoplasia, perforación, obstrucción)
- Requerimientos de transfusión > a 8 U en 24 horas en pacientes menores de 60 años.
Los tipos de cirugía dependen de la patología:
- Ulcera gástrica: Resección en cuña de lesión o sutura simple. En algunos casos puede requerir GST mas gastroenteroanastomosis en Y de Roux
- Neoplasia gástrica: Gastrectomia parcial o total + reconstrucción en Y de Roux
- Ulcera duodenal: Sutura del ulcus. Si se realiza una piloroplastia es necesario practicar una VT. Se puede ligar la arteria gastroduodenal.
- Angiodisplasia y dieulafoy: sutura simple o resección en cuña
Manejo post endoscópico
- Pacientes que reciben hemostasia endoscópica deben continuar con IBP por 72 horas EV 8mg/h
- Dosis altas de IBP vía oral puede ser una alternativa en pacientes de bajo riesgo con tolerancia oral.
- En caso de re-sangrado se debe repetir EDA
- En pacientes con sangrado secundario a ulcera péptica se debe realizar estudio para H. pilory, en caso de ser (+) erradicar.
- El reinicio de tto anticoagulante debe ser evaluado caso a caso, sin embargo, en la mayoría de los pacientes el reinicio de warfarina luego de 7-15 días del sangrado parece seguro y efectivo en prevenir complicaciones tromboenmbolicas.
- AAS puede reiniciarse inmediatamente post EDA en pacientes de bajo riesgo de re-sangrado (FIIc, FIII), en pacientes de alto riesgo se debe esperar 3 días.
B. HDA variceal
|
|
Terapia médica: Se utiliza Terlipresina, un análogo de vasopresina, actúa como vasoconstrictor esplácnico, disminuyendo la presión portal, su dosis son bolos de 2 mg cada 4 horas, disminuir a 1 mg una vez que se controla hemorragia. También Antibióticos con uso profiláctico en pacientes con DHC, dado el alto riesgo de infecciones posterior a HDA.
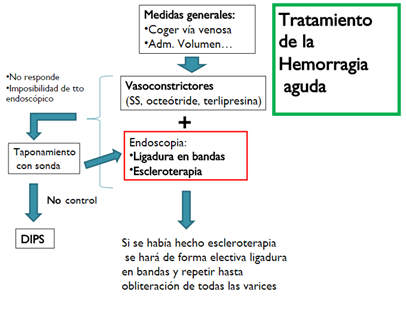
Terapia Endoscópica: La endoscopia debe efectuarse en las primeras 12 horas, o en las primeras 6 horas si existe hemorragia activa e inestabilidad hemodinámica. La ligadura en bandas es más eficaz que la escleroterapia en el control del sangrado inicial en estos casos.
Bibliografía
- Gralnek Ian M et al. Nonvariceal upper gastrointestinal hemorrhage: ESGE Guideline Endoscopy 2015; 47: a1–a46
- Manual de Patología Quirúrgica Pontificia Universidad católica de Chile, Fernando Crovari, Manuel Manzor. Capítulo 11 P151-163.
- Comparison of risk scoring systems for patients presenting with upper gastrointestinal bleeding: international multicentre prospective study. Adrian J Stanley et al. BMJ 2017;356:i6432
- Aproximación terapéutica en la hemorragia digestiva Dr. Allan Sharp Pittet, Unidad de endoscopia, Departamento de cirugía digestiva Pontificia Universidad Católica de Chile.
- Schwartz principles of surgery, 9th edition F. Charles Brunicardi, Dana K. Anderson Chapter 26 P 914-921
- The surgical management of acute upper gastrointestinal bleeding: A 12-year experience, M.G. Clarke et al. International Journal of Surgery, Volume 8, Issue 5, 2010, Pages 377-380
- ZALTMAN, Cyrla et al. Upper gastrointestinal bleeding in a Brazilian hospital: a retrospective study of endoscopic records. Arq. Gastroenterol., São Paulo, v. 39, n. 2, p. 74-80, Apr. 2002.
- al-Assi MT, Genta RM, Karttunen TJ, Graham DY. Ulcer site and complications: relation to Helicobacter pylori infection and NSAID use. Endoscopy. 1996 Feb. 28(2):229-33.
- Clasificacion de Forrest. Pablo Cortes G. Gastroenterol. Latinoam 2010; Vol 21 No 1: 59-62