Nivel de manejo del médico general: Diagnóstico: Específico. Tratamiento: Completo. Seguimiento: Completo.
Aspectos esenciales
- Evaluar tolerancia oral.
- Las Soluciones de Rehidratación Oral (SRO) de baja osmolaridad son la base del tratamiento
- Se debe mantener la alimentación normal, incluyendo la Lactancia Materna (LM).
- Se maneja v.o. la deshidratación leve y moderada; manejo e.v. de deshidratación severa.
- Despúes de cada deposición liquida 10cc/kg de SRO 60 meq vo
Caso clínico tipo
Un lactante de 7 meses, previamente sano, presenta fiebre de hasta 38 °C de 2 días de evolución acompañada de 10 deposiciones líquidas al día. Al examen se encuentra afebril, irritable, con conjuntivas secas y llanto con escasas lágrimas, extremidades frías, con llene capilar normal.
Definición
El término deshidratación aguda (DA) se emplea para designar el estado clínico consecutivo a la pérdida de agua y solutos que se produce por aportes insuficientes o pérdidas excesivas de agua. La deshidratación conduce a un compromiso variable según el grado de pérdida de líquidos, de los principales órganos y sistemas: circulatorio, renal, nervioso, respiratorio, digestivo, etc.
Se pueden producir diferentes grados de deshidratación que por motivos didácticos se clasifican en:
- Leves: <3 % en niño mayor o adulto; <5% en un lactante, de pérdida de peso corporal.
- Moderados: 3 -6 % en niño mayor o adulto; 5-10 % en un lactante, de pérdida de peso corporal.
- Graves: >6 % en niño mayor o adulto; >10% en un lactante, de pérdida de peso corporal.
Etiología
Las causas más frecuentes de DA son las digestivas, y dentro de éstas, la gastroenteritis aguda (GEA). En menor proporción, cabe considerar los vómitos, los síndromes de malabsorción, etc. Entre las causas extradigestivas, mucho más raras, podemos considerar el golpe de calor, las metabólicas (diabetes mellitus o insípida, tubulopatías, síndrome adrenogenital congénito) y las pérdidas excesivas de agua y electrolitos (quemaduras, mucoviscidosis, polipnea, hipertemia, etc.)
En niños con diarrea aguda, los factores de mayor riesgo para la deshidratación son: edad (lactantes), mal estado nutricional, suspender la lactancia materna, no administrar sales de rehidratación oral, la intensidad de la diarrea y la etiología (rotavirus, cólera).
Epidemiologia
Su frecuencia es difícil de precisar y depende fundamentalmente de factores socioculturales, higiénicos, climáticos, etc. Es más frecuente en los ambientes más desfavorecidos: con una escasa higiene, una alimentación inadecuada, infecciones frecuentes, etc. Existe un discreto predominio en varones. En cuanto a la edad, el 75-80% de los casos se produce en lactantes menores de 12 meses y más del 90% por debajo de los 18 meses.
Fisiopatología
El agua representa el 80% del peso corporal en el recién nacido y a partir del año de edad va disminuyendo hasta el 60% en los adultos, distribuyéndose en los compartimentos intracelular y extracelular. Cuando se producen alteraciones en los volúmenes o en la composición de los espacios hídricos corporales se ponen en marcha mecanismos reguladores de éstos que inmediatamente corrigen el trastorno inicial.
Se puede realizar con una historia clínica detallada y una exploración física adecuada, que puede complementarse con datos de laboratorio. La determinación de la natremia nos va a permitir definir si la DA es isonatrémica (Na: 130-150 mEq/l), hiponatrémica (Na<130 mEq/l) o hipernatrémica (Na>150 mEq/l). En el primer y segundo tipo la deshidratación es eminentemente extracelular, mientras que en el último es intracelular.
Diagnóstico
Las variaciones en el peso nos permitirán calcular las pérdidas y determinar la gravedad de la deshidratación.
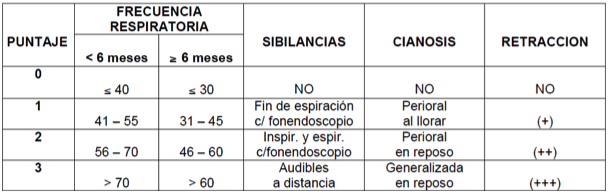
De no tener el dato exacto, puede aproximarse la pérdida de agua según la clínica, que se reúne en la siguiente tabla.
| Síntomas |
Leve |
Moderada |
Severa |
| Conciencia |
Alerta |
Normal, decaído, irritable |
Letárgico |
| Sed |
Bebe normal |
Bebe ávidamente |
Bebe con dificultad |
| Pulsos |
Normal |
Normal |
Filiforme |
| Respiración |
Normal |
Leve polipnea |
Taquipnea |
| Ojos |
Normal |
Conjuntivas secas |
Ojos hundidos |
| Lágrimas |
Presentes |
Disminuidas |
Ausentes |
| Mucosas |
Húmedas |
Algo secas |
Secas |
| Signo del pliegue |
Ausente |
Más de 2 segundos |
Muy prolongado |
| Llene capilar |
Normal |
Normal |
Más de 2 segundos |
| Extremidades |
Tibias |
Frías |
Frías, reticuladas |
| Diuresis |
Normal |
Disminuida |
Oligoanuria |
|
Pérdida de peso
– Lactantes
– Pre-escolar – Escolar
|
5-10%
3-6%
|
10-15%
6-9%
|
Más de 15%
Más de 9%
|
Tratamiento
Las soluciones de rehidratación oral están indicadas en la prevención y el tratamiento de la deshidratación aguda como complicación de las gastroenteritis agudas y otros procesos en los que haya pérdidas mantenidas de líquidos. Son válidas para cualquier tipo de deshidratación (isotónica, hipertónica o hipotónica) y en los grados de deshidratación leve y moderada. Se pueden utilizar en cualquier edad, y son preferibles frente a las soluciones caseras, expuestas a un mayor número de errores en su composición y dilución.
En el tratamiento de las deshidrataciones moderada y grave deberemos restituir rápidamente la volemia para impedir o tratar la situación de shock, reponer el déficit de agua y de electrolitos teniendo en cuenta las pérdidas continuadas que puedan seguir produciéndose, y aportar las necesidades diarias de agua y electrolitos hasta que se pueda volver a la administración de líquidos por vía oral.
La base es la SRO de baja osmolaridad (240-250 mOsm/l) que contiene Na y glucosa en relación equimolar y es isoosmótica. Se debe considerar:
Requerimiento basal (por holliday) + déficit (según grado de deshidratación) + pérdidas patológicas.
- Requerimiento basal: fórmula de Holliday:
- 100 ml x Kg. por los primeros 10 Kg, 50 ml x Kg. por los siguientes 10 Kg y 20 ml x Kg. por los siguientes.
- Déficit: Para DH leve 50cc/kg, moderada 100cc/kg y severa 150cc/kg
- Pérdidas patológicas: Se estiman entre 30-50cc/kg
Paciente no deshidratado con pérdidas aumentadas:
Dar mayor cantidad de líquidos que lo normal, continuar la alimentación, reconocer los signos que indican cuando volver a consultar. Control si no mejora en tres días o si aparecen vómitos frecuentes, decaimiento marcado, sangre fecal, fiebre alta, exceso de deposiciones líquidas.
Paciente deshidratado: Evaluar grado de deshidratación.
Contiene dos fases:
- Rehidratación: Corregir el déficit de agua y electrolitos.
- Vía oral: Se realiza en 4-6h para dh leve y moderada según tolerancia oral.
- Vía IV: Se realiza en 8 hr aportando el 50% del volumen total calculado. En Deshidratación severa pasar SF en bolo 20cc/kg y reevaluar. Se puede repetir hasta 3 veces.
- Mantención: Cubrir los requerimientos y las pérdidas exageradas por diarrea. (sin el déficit)
Seguimiento
La eficacia del tratamiento de rehidratación se valora según los siguientes parámetros:
- Estado circulatorio del paciente
- Mejoría de los signos de deshidratación
- Recuperación del peso corporal
- Volumen de la diuresis
- pH y densidad urinarios
- Electrolitos séricos
- Equilibrio ácido-base.
La deshidratación se suele acompañar de alteraciones hidroelectrolíticas y del equilibrio ácido-base, (que son detalladas en su texto respectivo). Deben valorarse los cambios del metabolismo del resto de los iones implicados en el metabolismo hidroelectrolítico, sobre todo del calcio y del potasio y corregir sus alteraciones.
Por último, en las siguientes 24 h se administrarán las cifras de agua y de electrolitos de mantenimiento, a las que se añadirán las pérdidas incrementadas que pueden persistir eventualmente, y se corregirán las posibles alteraciones no solucionadas en la fase anterior (hipopotasemia, etc.). Llegado a este punto, de forma paulatina se iniciará.