Nivel de manejo del médico general: Diagnóstico: Sospecha Tratamiento: Inicial Seguimiento: Derivar
Aspectos esenciales
▪ La causa más frecuente es TVP femoro-poplítea.
▪ La disnea y el dolor torácico son cardinales.
▪ El Gold standard para el diagnóstico es la AngioTAC de tórax.
▪ Si la sospecha es alta se debe iniciar el tratamiento anticoagulante sin demora.
Caso clínico tipo
Mujer hospitalizada por Fx de cadera no resuelta, presenta de manera súbita disnea y dolor torácico con tope inspiratorio. Al examen está normotensa, taquicárdica y taquipneica. Dada la alta sospecha clínica solicita Angio TAC de tórax que muestra TEP. Inicia manejo con HBPM.
Definición
La tromboembolia pulmonar (TEP) es la obstrucción al flujo arterial pulmonar, secundario a trombo que frecuentemente se origina y desprende del territorio venoso. De acuerdo a su localización se caracterizan como centrales o proximales (de la art. pulmonar principal, lobar o segmentaria) y distales o subsegmentarios. En relación a la temporalidad pueden ser agudo, sub agudo y crónicos.
Se define como TEP masivo en sujetos sin enfermedad cardiopulmonar previa una obstrucción > 50% del lecho vascular pulmonar y en aquéllos con enfermedad cardiopulmonar una obstrucción > 23%, que causa hipotensión (PAS < 90 mmHg o una disminución en la PAS ≥ 40 mmHg desde su basal, por un período > 15 minutos).
Etiología-epidemiología-fisiopatología
La principal causa de TEP es la migración de un émbolo arterial proveniente de una TVP (60% de los pacientes con TEP presentan una TVP). Los factores de riesgo principales son los que determinan la denominada Tríada de Virchow (estasia venosa, daño endotelial e hipercoagulabilidad): cirugías mayores (abdominpelvianas, cadera y EEII), cesárea y puerperio, neoplasias, fracturas/traumas de EEII, inmovilización prolongada, tabaquismo, uso de anticonceptivos orales y el antecedente personal de TVP o TEP.
El émbolo puede producir infartos pulmonares, alteración de la relación V/Q, y compromiso de corazón derecho. La afectación cardíaca está mediada por aumento de la resistencia del territorio vascular secundaria a tanto a obstrucción por el émbolo como por vasoconstricción pulmonar secundaria a la hipoxemia; este aumento de la resistencia vascular pulmonar lleva a dilatación del ventrículo derecho, y eventualmente a disminución del gasto cardíaco debido a caída de la precarga.
exámenes que son de utilidad (sospecha): ECG (Bloqueo de rama derecha, desviación del eje a derecha y patrón S1Q3T3), Ecocardiograma que evidencia compromiso de ventrículo derecho y mide la PAP (no hace el diagnóstico), y las enzimas cardíacas que pueden estar elevadas (indica compromiso del miocardio).
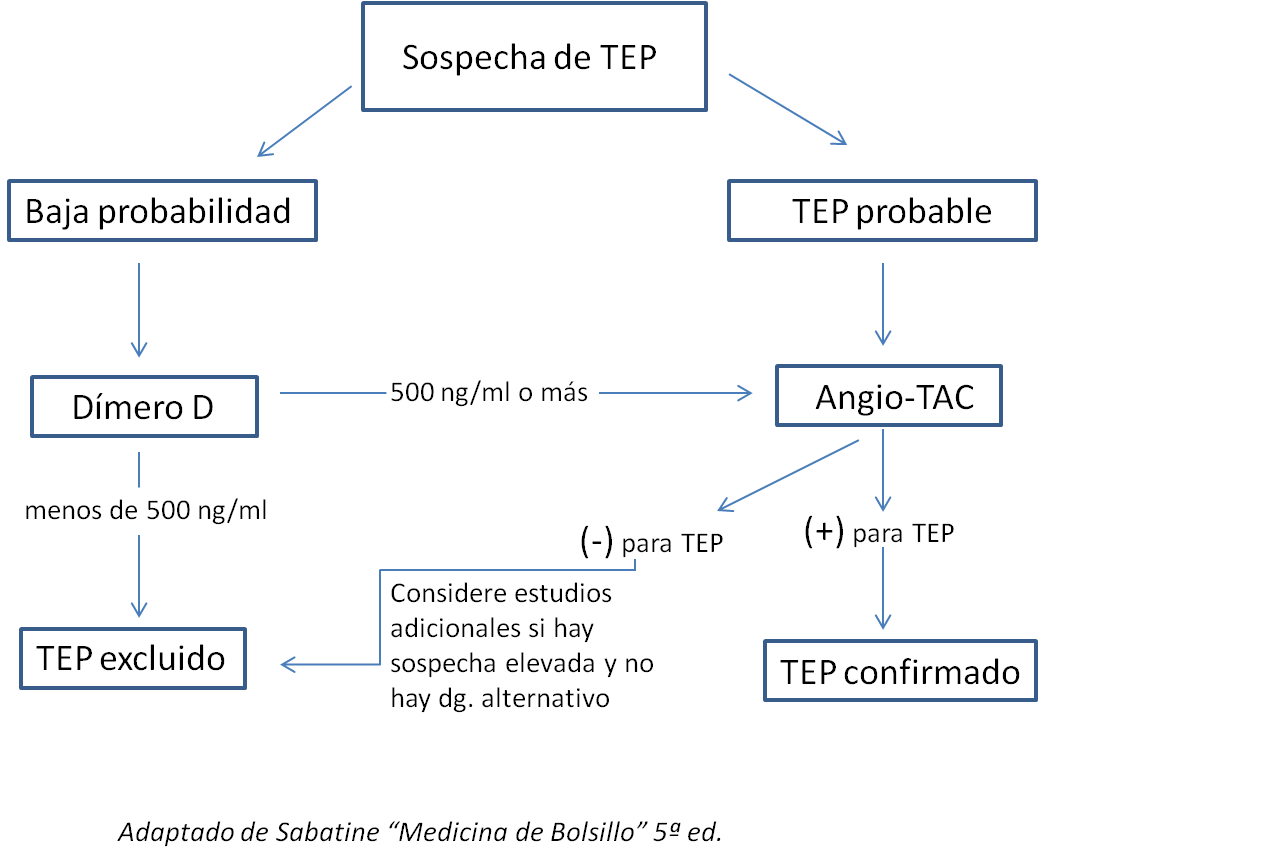
La probabilidad pre-test nos ayuda a definir la conducta diagnóstica, de acuerdo al siguiente algoritmo:
| CRITERIO | PUNTOS |
|---|---|
| Síntomas y signos clínicos de TVP | 3.0 |
| Diagnóstico alternativo menos probable que TEP | 3.0 |
| Frecuencia cardíaca >100x’ | 1.5 |
| Inmovilización prolongada | 1.5 |
| Cirugía en las últimas 4 semanas | 1.5 |
| TVP o TEP previos | 1.5 |
| Hemoptisis | 1.0 |
| Cáncer (en tratamiento actual o menos 6 meses o en cuidados paliativos) | 1.0 |
| RIESGO | |
| Baja | <4 |
| Alta | ≥4 |
Factores de riesgo
Escalas de probabilidad clínica
Las escalas de probabilidad clínica permiten estratificar el riesgo de embolia pulmonar y guiar la necesidad de pruebas complementarias. Las más utilizadas son:
- PESI y sPESI (Pulmonary Embolism Severity Index): para evaluar la gravedad y el pronóstico.
- Regla PERC (Pulmonary Embolism Rule-Out Criteria): utilizada en pacientes con baja sospecha de embolia pulmonar para descartar la enfermedad sin necesidad de pruebas adicionales.
- YEARS: algoritmo de ajuste del punto de corte del D-dímero en función de la probabilidad clínica.
Pruebas diagnósticas
El diagnóstico de la embolia pulmonar se basa en una combinación de pruebas de laboratorio e imagen:
- D-dímero: prueba de alta sensibilidad pero baja especificidad. Se recomienda su ajuste por edad en pacientes mayores de 50 años.
- Angio-TC pulmonar: prueba de referencia para la confirmación diagnóstica.
- Gammagrafía de ventilación-perfusión: alternativa en pacientes con contraindicación para TC.
- Ecocardiografía: útil en pacientes con inestabilidad hemodinámica.
Tratamiento de la embolia pulmonar
Fases del tratamiento
El manejo de la embolia pulmonar se divide en tres fases:
- Fase aguda o inicial (primeros 5-21 días): Prevención de la progresión del trombo y recurrencias tempranas.
- Fase de tratamiento prolongado (3-6 meses): Reducción del riesgo de recurrencia.
- Fase extendida (más de 6 meses): Prevención secundaria en pacientes con alto riesgo de recurrencia.
Anticoagulación
Los anticoagulantes orales de acción directa son la primera línea de tratamiento en la mayoría de los casos. Incluyen inhibidores del factor Xa (rivaroxabán, apixabán, edoxabán) y un inhibidor directo de la trombina (dabigatrán). Alternativamente, se pueden usar antagonistas de la vitamina K (warfarina) o heparinas de bajo peso molecular en pacientes con contraindicaciones para anticoagulantes orales de acción directa.
Terapias de reperfusión
En pacientes con embolia pulmonar de alto riesgo y deterioro hemodinámico, se recomienda considerar:
- Fibrinolisis sistémica con rTPA (alteplasa)
- Trombectomía percutánea
- Cirugía de embolectomía en casos seleccionados
Filtro en vena cava inferior
Indicados en pacientes con tromboembolismo venoso reciente y contraindicación absoluta para la anticoagulación. Debe retirarse tan pronto como la anticoagulación sea viable.
Situaciones especiales
Embarazo y puerperio
La heparina de bajo peso molecular es el tratamiento de elección durante el embarazo, ya que no atraviesa la placenta. Se debe evitar el uso de anticoagulantes orales de acción directa y warfarina en el primer y tercer trimestre.
Enfermedad renal avanzada
Los anticoagulantes orales de acción directa están contraindicados en pacientes con filtrado glomerular menor de 15 ml/min. Se recomienda el uso de heparina no fraccionada o heparina de bajo peso molecular con ajuste de dosis.
Embolia pulmonar subsegmentaria
El tratamiento debe ser individualizado. En pacientes con alto riesgo de sangrado y bajo riesgo de trombosis, podría considerarse la no anticoagulación.
Manejo del TEP
¿Cuándo deberíamos considerar el tratamiento domiciliario en la Aproximadamente el 85% de los gastos corresponden a la estancia hospitalaria. De acuerdo con las guías de práctica clínica vigentes, un porcentaje no desdeñable de pacientes podrían beneficiarse de un alta precoz (es decir, antes de 48 h) o tratamiento domiciliario.
-
– El riesgo de muerte o complicaciones relacionadas con la TEP tiene que ser bajo.
- – Ausencia de comorbilidades graves que requieran hospitalización.
- – El paciente puede recibir un tratamiento y atención ambulatoria adecuados.
Selección de los pacientes
Criterios de Hestia
| ¿Inestabilidad hemodinámica? |
|---|
| ¿Es necesario tratamiento con trombólisis o embolectomía? |
| ¿Existe sangrado activo o riesgo de sangrado? |
| ¿Es necesario tratamiento con oxígeno para mantener saturaciones > 90% durante más de 24 h? |
| ¿La embolia de pulmón ha sido diagnosticada mientras ya recibía tratamiento anticoagulante? |
| ¿Precisa de tratamiento analgésico intravenoso > 24 h? |
| Motivo médico o social que precise de ingreso hospitalario > 24 h |
| Aclaramiento de creatinina < 30 ml/min |
| Presencia de enfermedad hepática severa |
| Embarazo |
| Antecedentes de trombocitopenia inducida por heparina |
Escala de gravedad de la embolia de pulmón PESI (versión original y simplificada)
| Parámetro | Versión original | Versión simplificada |
|---|---|---|
| Edad | Edad en años | 1 punto para edad > 80 años |
| Sexo masculino | + 10 puntos | |
| Cáncer | + 30 puntos | 1 punto |
| Insuficiencia cardiaca crónica | + 10 puntos | 1 punto |
| Enfermedad pulmonar crónica | + 10 puntos | |
| Frecuencia cardiaca > 110 lpm |
+ 20 puntos | 1 punto |
| PA sistólica < 100 mmHg |
+ 30 puntos | 1 punto |
| Frecuencia respiratoria > 30 rpm |
+ 20 | – |
| Temperatura < 36 °C | + 20 puntos | – |
| Estado mental alterado | + 60 puntos | – |
| Saturación O2 < 90% | + 20 puntos | 1 punto |
| Clasificación de riesgo | Empty Cell |
|---|---|
| Clase I: < 65 puntos (riesgo muy bajo) | 0 puntos |
| Clase II: 66-85 puntos (riesgo bajo) | |
| Clase III: 86-105 puntos (riesgo moderado) | ≥ 1 punto |
| Clase IV: 106-125 puntos (riesgo alto) | |
| Clase V: > 125 puntos (riesgo muy alto) |
¿Cuándo deberíamos considerar las terapias de reperfusión en el tratamiento de la TEP de riesgo intermedio-alto?
¿Cuándo deberíamos considerar el tratamiento domiciliario en la TEP?
- – El riesgo de muerte o complicaciones relacionadas con la TEP tiene que ser bajo.
- – Ausencia de comorbilidades graves que requieran hospitalización.
- – El paciente puede recibir un tratamiento y atención ambulatoria adecuados.
El manejo inicial debe ir enfocado a la estabilización del paciente: hemodinamia, suplementación de oxígeno en caso de hipoxemia (y valorar la necesidad de ventilación mecánica). Si el paciente tiene una baja probabilidad de TEP, se solicita un dimero-D, el cual tiene un alto valor predictivo negativo, de esta manera, una baja probablidad de TEP más dimero-D negativo, descarta la posibilidad de TEP.
Educación del paciente
En casos de alta sospecha con hemodinamia estable, se debe iniciar tratamiento con heparina corriente o de bajo peso molecular mientras se prepara al paciente para el angioTAC. Una vez confirmado por este examen, se inicia el tratamiento anticoagulante oral paralelo a la heparina, la que se suspende una vez que el tratamiento oral esté en niveles terapéuticos (INR 2-3). El tratamiento anticoagulante oral se mantiene por 3 a 6 meses, y si el factor de riesgo se mantendrá activo, será de por vida.
En casos de alta sospecha de TEP con hemodinamia inestable, se inicia tratamiento con heparina no fraccionada o de bajo peso molecular a dosis plena, en espera del resultado del AngioTAC. Una vez confirmado, se realiza trombolisis, siempre y cuando no haya contraindicaciones absolutas. La trombolisis se puede realizar con estreptoquinasa (250.000 U EV los primeros 30 minutos y luego 100.000 U/h por 24 horas, con atención a aparición de hipotensión, anafilaxia, asma o reacciones alérgicas), tPA (100 mg EV en 2 horas). Generalmente se descontinúa la terapia anticoagulante durante la infusión del trombolítico.
Se contraindica la trombolisis en caso de neoplasia intracraneana, trauma o cirugía intracraneana reciente (<2 meses), hemorragia interna activa o reciente en los últimos 6 meses, historia de ACV hemorrágico, coagulopatía, HTA severa e incontrolada, ACV no hemorrágico en los últimos 2 meses, cirugía en los últimos 10 días y trombocitopenia. Si estuviese contraindicada se debe realizar estudio angiográfico y trombectomía o lisis del coágulo. Algunos autores plantean que ante un paciente con evidente probabilidad de TEP y hemodinamia inestable, podría iniciarse de entrada trombolisis, idealmente con tPA (tenecteplase 100mg a pasar en 2 horas) acompañado de heparina. Y realizar luego sin premura el AngioTAC para confirmar la sospecha, sin embargo, está en discusión.
Seguimiento
Debe ser por especialista, decidir por cuánto tiempo mantener ACO (INR 2-3) y evaluar la necesidad de buscar algún factor protrombótico (por ejemplo neoplasia oculta o trombofilia).
Bibliografia
1. M. Sabatine. «Tromboembolia venosa (TEV)», pág. 65-68. Medicina de Bolsillo, 5° edición. Wolters Kluwer Health, 2014.
3. Konstantinides S, Meyer G, Becattini C, Bueno H, Geersing G, Harjola V, et al.;Grupo de Trabajo de la Sociedad Europea de Cardiología (ESC) para el diagnóstico y tratamiento de la tromboembolia pulmonar aguda. Guía ESC 2019 para el diagnóstico y tratamiento de la embolia pulmonar aguda. Rev Esp Cardiol. 2020;73(6):497.11-497.e58. [ Links ]
4. Essien E, Rali P, Mathai S. Pulmonary embolism. Med Clin N Am. 2019;103(3):549-64. [ Links ]4. Fields J, Davis J, Girson L, Au A, Potts J, Morgan C, et al. Transthoracic echocardiography for diagnosing pulmonary embolism:A systematic review and meta-analysis. J Am Soc Echocardiogr. 2017;30(7):714-23.e4. [ Links ]

