ECG en intoxicaciones
- Introducción
La Intoxicación por drogas corresponde a una de las mayores causas de morbi-mortalidad en el mundo, que puede ser accidental o intencional. Su importancia también radica en que, debido a la amplia cantidad de sustancias disponibles que pueden ser causa de intoxicación, existe gran desconocimiento de la población general y el personal de salud para identificar y tratar estos cuadros. Además, en gran parte de los casos, la forma clínica de presentación puede ser confundente debido a esta gran variabilidad de sustancias que conlleva una gran variabilidad clínica. En este texto se expondrán las principales características de las intoxicaciones, su diagnóstico y manejo, haciendo especial hincapié en el electrocardiograma (ECG) como una útil herramienta en su enfrentamiento.
Epidemiologia
En Estados Unidos la American Association of Poison Control Centers (AAPCC) registro más de 2,1 millones de llamadas por exposición de humanos a diversos tóxicos en el año 2014. El 28,3% de esta población requirió atención médica, el 7,9% de los casos fueron hospitalizados y el 0,07% falleció por esta causa. Se estima que en Estados Unidos, hay 1,1 millones de consultas anuales al Servicio de Urgencias debido a intoxicaciones1.
En Chile, si bien existe una falta de reporte por parte de los centros asistenciales de urgencias, un estudio realizado por el Centro de Información Toxicológica y de Medicamentos de la Pontificia Universidad Católica (CITUC)2 en que se analizaron las intoxicaciones más frecuentes entre el año 1992-2002, demostró que las intoxicaciones más frecuentes eran por fármacos, seguidos por los productos de aseo, plaguicidas (domésticos y agrícolas), productos industriales y químicos, y productos cosméticos. Dentro de los fármacos los más utilizados eran los depresores del SNC (tricíclicos, benzodiacepinas, opioides, antipsicóticos) con un 40,3% seguidos por antihistamínicos, broncodilatadores, mucolíticos, antitusígenos con 10,9%, antimicrobianos 6,2%, hormonales con 5,5% y finalmente las drogas que actúan a nivel cardiovascular (antiarrítmicos, antihipertensivos, vasodilatadores) con 4,7%.
- Diagnóstico
Al momento de enfrentar inicialmente a un paciente intoxicado, se deben tener en cuenta una serie de conceptos generales. En primer lugar, no se debe olvidar que el foco de la atención del médico debe ser el paciente y no el tóxico ingerido, es decir, la primera parte de la atención estará focalizada en la estabilización y soporte del paciente siguiendo el lineamiento del ABCDE universal (con algunos acápites particulares a la intoxicación) para posteriormente realizar una anamnesis rápida con el fin de intentar determinar el tóxico ingerido, el tiempo transcurrido desde la ingesta, la dosis, etc. y un examen físico acucioso, con el fin de pesquisar un posible “toxindrome” (síndrome atribuible a un tóxico en específico) en los casos en que a través de la anamnesis no se logra determinar la sustancia responsable. En el mejor de los escenarios, ambos pasos deben ser realizados en forma simultánea por el equipo de salud.
No se debe perder tiempo en solicitar múltiples exámenes de laboratorio, puesto que en muchos casos la mayoría de estos no serán de ayuda.
Por otro lado, se debe intentar contactar a algún centro toxicológico para apoyar el diagnóstico y guiar el tratamiento (Ej, CITUC).
Cabe mencionar, que en la gran mayoría de los casos los pacientes se presentaran conscientes y asintomáticos, pudiendo comunicar a través de la anamnesis la sustancia y la dosis ingerida, requiriendo en la mayoría de los casos solo un periodo de observación.
Valoración rápida
Como se mencionó anteriormente, el foco de la atención debe estar en el paciente, en su estabilización y soporte a través del ABC universal, el cual puede ampliarse a ABCDEFG en caso de las intoxicaciones3:
- – Vía aérea (A): Se debe evaluar la permeabilidad y protección refleja de la vía aérea. El paciente que está consciente y ventilando adecuadamente probablemente tenga una vía aérea segura, en caso contrario, se debe descartar una depresión respiratoria o pérdida de conciencia profunda secundaria a la droga ingerida. Si existe sospecha de riesgo es preferible asegurar la vía aérea a través de la intubación orotraqueal.
- – Ventilación/ Breathing (B): Evaluado en conjunto con el punto anterior, a través de la inspección de los movimientos respiratorios y la auscultación del murmullo pulmonar, y apoyándose con la saturometría sanguínea. Se debe administrar oxigeno suplementario en caso de hipoxia, ya sea a través de naricera, mascarilla o intubación y ventilación mecánica en los casos más severos. Recordar que algunas sustancias, como el monóxido de carbono, puede comprometer la oxigenación del paciente sin alterar la saturometría.
- – Circulación (C): Los medicamentos consumidos pueden tener acción sobre el corazón directamente, causando hiper o hipotensión, taqui o bradicardia, por lo que la monitorización cardiovascular es de regla en todos los pacientes y también la instalación de vías venosas en forma preventiva, aunque el paciente esté asintomático, ya que algunas sustancias pueden tener un efecto retardado. Se debe administrar volumen en caso de hipotensión, y manejar las crisis hipertensivas o arritmias que se puedan presentar.
- – Déficit neurológico + Descontaminación + DONT (D): En primer lugar, se evalúa el estado neurológico del paciente en forma rápida, a través de la escala de Glasgow, el examen pupilar y el tono muscular. En caso de presentar Glasgow menor a 9 o un deterioro progresivo está indicada la intubación orotraqueal protectora. En caso que se sospeche un tóxico que ingrese al organismo por vía cutánea (Ej, organofosforados) se debe descontaminar al paciente, eliminando su ropa, lavándolo copiosamente con agua y jabón, siempre asegurando la seguridad del personal de salud con las medidas universales de protección (guantes, mascarillas, gafas, etc).
La mnemotecnia DONT se refiere al llamado “coctel del coma” para pacientes con compromiso de conciencia, que incluye Dextrosa, Oxigeno, Naloxona y Tiamina. Múltiples sustancias pueden causar hipoglicemia, por lo cual el uso de hemoglucotest debe ser de rutina en todos los pacientes. En caso de no tener hemoglucotest disponible podría indicarse Dextrosa 50 gr IV sin mayores consecuencias. La Naloxona es un efectivo antagonista de opioides. Los pacientes presentan una rápida respuesta a este fármaco, y la ausencia de respuesta prácticamente descarta la intoxicación por opioides4. Se debe recordar que la Naloxona tiene una corta vida media, y que en paciente dependientes podría desencadenar un síndrome de abstinencia en forma aguda. El síndrome de Wernicke-Korsakoff se debe sospechar en pacientes alcohólicos con signos de desnutrición, quienes se benefician del uso de Tiamina IV. El uso rutinario de tiamina en pacientes sin estas características es controversial5.
- – Eliminación (E): En este punto se reúnen todas las medidas usadas para evitar la absorción del tóxico, favorecer su adsorción o su eliminación. Cabe mencionar que existe mucha controversia en relación a los distintos métodos existentes hoy en día para realizar estas acciones, debido a la complejidad de hacer estudios randomizados que demuestren su real eficacia. Dentro de las medidas que están avaladas por la evidencia encontramos:
- – Lavado gástrico: Procedimiento que requiere el uso de una sonda específica (Sonda orogástrica de 36-40 F o Sonda Ewald), la que no se encuentra disponible en la mayoría de los servicios de urgencia del país. Se realiza con el paciente en decúbito izquierdo, instilando alícuotas de 250 ml (10 ml/kg en niños) hasta obtener líquido claro. Recomendado actualmente cuando se puede realizar dentro de la primera hora de ingerido el tóxico6. Solo está indicado en pacientes con vía aérea segura y que el beneficio del procedimiento supere el riesgo, debido a que se ha asociado a perforación esofágica, aspiración y muerte6. El mayor beneficio se obtiene cuando se utiliza precozmente, cuando se han ingerido fármacos que retrasan el vaciamiento gástrico (antidepresivos tricíclicos [ATC]) o cuando el uso de carbón activado no es útil (metales pesados, litio, ácidos, álcalis, solventes, pesticidas) o está contraindicado.
- – Carbón activado: Es la medida más eficaz actualmente7. Se debe administrar por vía oral, en una concentración al 25% en agua, dosis de 1 g/kg en forma repetida cada 2-4 horas hasta alcanzar una relación tóxico : carbón de 1 : 103. Su eficacia aumenta mientras más precoz sea la administración después de ingerido el tóxico. Al igual que la anterior, solo puede indicarse en pacientes que tengan vía aérea protegida debido al riesgo de aspiración. El efecto adverso más común es la constipación.
- – Alcalinización urinaria: Útil en la eliminación de drogas como los salicilatos y el fenobarbital, inyectando bicarbonato de sodio 3-4 meq/kg cada 4 horas. Se debe controlar el pH sanguíneo y los niveles de potasio debido al riesgo de alcalosis e hipokalemia3.
- – Hemodiálisis: Útil especialmente para salicilatos, alcoholes, litio y etilen glicol. Usado generalmente cuando no hay respuesta a otras medidas de primera línea8.
Otras medidas como el uso de catárticos, eméticos y de irrigación intestinal no se recomiendan en la práctica debido a sus efectos adversos y al escaso beneficio demostrado en los estudios9, 10, 11.
- – Terapia dirigida / Focus Therapy (F): Referida al uso de antídotos, los cuales son un número reducido, y específicos para ciertos tóxicos. Es importante destacar que, salvo la naloxona, ninguno debe usarse en forma empírica debido a sus posibles efectos adversos y que la mayoría de los pacientes intoxicados tienen un buen pronóstico con el soporte adecuado, independiente del uso de antídotos. En la tabla 1 se presentan algunos tóxicos y sus antídotos, los cuales deben ser conocidos por el médico de urgencias.
|
Antídoto |
Tóxico |
|
n-acetil cisteína |
Paracetamol |
|
Etanol / Fomepizol |
Metanol / Etilen glicol |
|
Oxigeno 100% |
Monóxido de carbono |
|
Naloxona |
Opioides |
|
Fisostigmina |
Anticolinérgicos |
|
Atropina/ Pralidoxina |
Organofosforados |
|
Nitritos |
Cianuro |
|
Deferoxamina |
Hierro |
|
Dimecaprol |
Arsénico |
|
Succimer |
Plomo, Mercurio |
|
Fragmento Fab |
Digoxina, colchicina |
|
Glucagón |
B-bloqueadores |
|
Calcio/ Insulina/ Dextrosa |
Bloqueadores de canal de calcio |
|
Dextrosa, glucagón |
Hipoglicemiantes orales |
Tabla 1. Algunos tóxicos y sus antídotos
- – Ayuda a un centro toxicología/ Get Tox Help (G): Siempre será útil ponerse en contacto con algún centro de toxicología, con el fin de recibir apoyo en el diagnóstico y el manejo de este tipo de pacientes.
Exploración clínica
Una vez que el paciente se encuentra fuera de riesgo vital (o paralelamente a la estabilización cuando es posible) se debe completar la exploración diagnóstica con la anamnesis, el examen físico y algunos exámenes complementarios que pueden ser de utilidad. Dentro de estos destacaremos y analizaremos en profundidad el ECG como método diagnóstico.
- – Anamnesis: En la mayoría de los casos, a través de la entrevista, se podrá determinar la sustancia ingerida por el paciente. Sin embargo, en algunas ocasiones la información no estará disponible, y es en estos casos donde es importante recabar información como los antecedentes de salud del paciente y sus familiares, los medicamentos disponibles en el hogar y otras fuentes de intoxicación. Se debe intentar determinar la hora exacta de la ingesta, así también como la dosis y la vía de exposición. No debe olvidarse explorar los antecedentes psiquiátricos del paciente que nos hagan sospechar una conducta suicida.
- – Examen físico: Debe ser lo más completo posible, buscando alteraciones en los signos vitales, alteraciones del examen pupilar y otros signos clínicos. Los llamados toxíndromes, si bien son frecuentes tienen baja especificidad debido a que tienen una gran cantidad de manifestaciones diferentes y pueden superponerse cuando existe ingestión de más de un tóxico. Los toxíndromes más frecuentes se presentan en la tabla 2.
|
Síndrome |
Fármacos asociados |
Clínica |
|
Anticolinérgico |
Antihistamínicos, ATC, antiparkinsonianos, antiespasmódicos, atropina, escopolamina |
Hipervigilancia, agitación, alucinación, delirium, coma, midriasis, hipertermia, taquicardia, hipertensión, taquipnea, piel seca, mucosas secas, retención urinaria, mioclonías |
|
Simpaticomimético |
Cocaina, anfetaminas, efedrina |
Hiperalerta, agitación, alucinaciones, midriasis, hipertermia, taquicardia, hipertensión, taquipnea, diaforesis, temblores, hiperreflexia, crisis convulsivas |
|
Colinérgico |
Organofosforados e insecticidas, pilocarpina, fisostigmina |
Confusión, coma, miosis, bradicardia, hipertensión, taquipnea o bradipnea, salivación, incontinencia urinaria y fecal, diarrea, emesis, diaforesis, broncoconstricción. |
|
Opioide |
Heroína, morfina, metadona |
Depresión del SNC, coma, miosis, hipotermia, bradicardia, hipotensión, apnea, bradipnea , hiporeflexia, edema pulmonar |
|
Serotoninérgico |
IMAO, ISRS, meperidina |
Confusión, agitación, coma, midriasis, hipertermia, taquicardia, hipertensión, taquipnea, temblores, mioclonías, hiperreflexia, diaforesis, trismus, diarrea |
Tabla 2. Toxíndromes más frecuentes
- – Exámenes complementarios: Como se mencionó anteriormente, solo un número reducido de exámenes son útiles al momento de enfrentarse al paciente intoxicado. Dentro de estos exámenes cabe destacar la medida de electrolitos plasmáticos, nitrógeno ureico, creatinina, glicemia, función hepática y gases venosos o arteriales idealmente, sin olvidar el test de embarazo en mujer de edad fértil.
En general, solicitar exámenes toxicológicos específicos en el servicio de urgencias no es de utilidad, salvo en el seguimiento del paciente una vez conocido el toxico, como en el caso de las intoxicaciones por paracetamol, salicilatos, y alcoholes.
En ocasiones es útil el cálculo del anión GAP y el GAP osmolal, ya que sabiendo ambos parámetros podemos estrechar el abanico de posibilidades ante la sospecha de una intoxicación por un agente desconocido. En la Tabla 3 se mencionan algunos ejemplos de esto.
|
Tóxico |
Alteración de laboratorio |
|
Paracetamol Etanol Hierro Salicilatos Monóxido de carbono |
Anión GAP elevado |
|
Etanol Manitol Sorbitol Magnesio Medios de contraste |
GAP osmolal elevado |
Tabla 3. Ejemplos de alteraciones metabólicas por tóxicos
ECG
Las alteraciones del ECG en contexto de intoxicaciones son comunes debido a que múltiples fármacos pueden tener una acción cardiovascular, provocando distintas manifestaciones. Cabe destacar en este punto, que muchas de los fármacos usados comúnmente para tratar estas arritmias pueden no ser efectivas o empeorar el cuadro cuando se presentan en contexto de una intoxicación12.
Cuando se entiende la fisiología cardiovascular y como esta se altera por los distintos fármacos, pueden agruparse según su mecanismo fisiopatológico y con esto optimizar el proceso diagnóstico y terapéutico del paciente intoxicado. En el siguiente apartado se pretende revisar estos temas.
Fisiología cardiovascular
En primer lugar se debe comprender como es que se produce el ciclo cardiaco y como este se relaciona con las ondas del ECG.
La actividad eléctrica cardiaca depende del equilibrio y traspaso de iones a través de la membrana de la célula miocárdica, la que es estrictamente regulada por la apertura y cierre de distintos canales iónicos, y la acción de la bomba Na/k atpasa que es la responsable de mantener las concentraciones iónicas intra y extracelulares, y con esto el gradiente de concentración transmembrana. Así, el ciclo cardiaco puede dividirse en cinco fases (Figura 1)13.
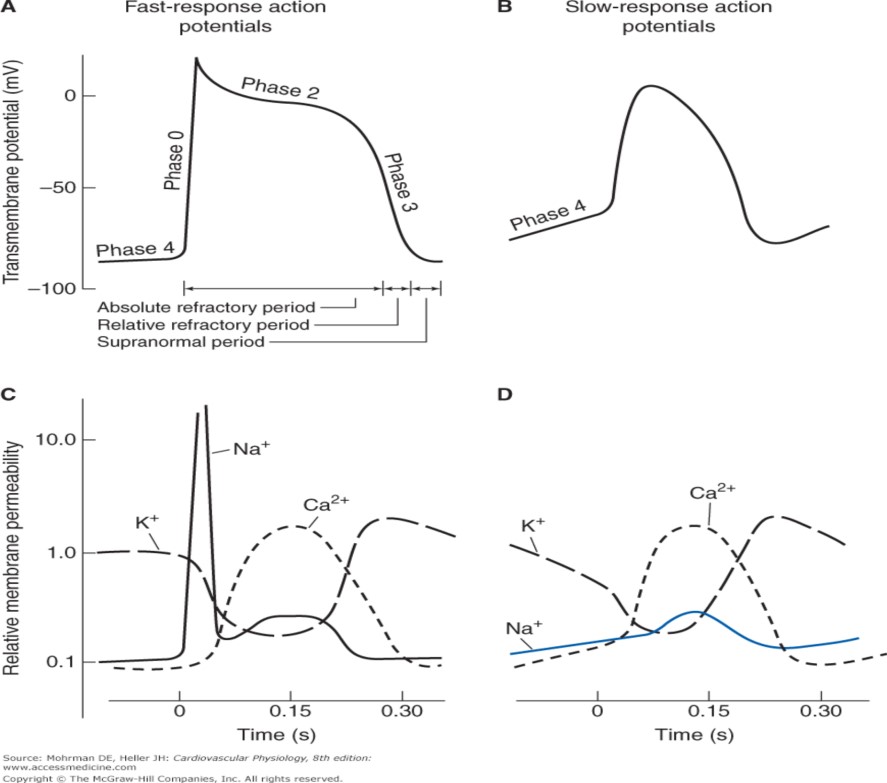
Fig 1. Ciclo cardiaco.
Por acción de la bomba Na/k atpasa se mantiene un potencial de membrana negativo cercano a los -90 mV (Fase 4). Luego, por el potencial de acción trasmitido desde las células del sistema exitoconductor cardiaco se abren canales de Sodio (Na) provocando un influjo de este ión, causando una elevación rápida del potencial de membrana (Fase 0) lo que se relaciona con el complejo QRS en el ECG. El peak de este cambio de potencial termina con el cierre de estos canales de Na y la apertura de canales de potasio (K), provocando el eflujo de este ión (Fase 1). Posteriormente, se abren canales de Calcio (Ca) provocando influjo de este ion que contrarresta el eflujo de K, lo que se traduce en un plateu del potencial de membrana (Fase 2). Cuando estos canales de Ca se cierran y se abren nuevos canales de K, el potencial de membrana vuelve a negativizarse cerca de los -90 mV (Fase 3) terminando el ciclo cardiaco. Este último eflujo de K se relaciona directamente con el intervalo QT del ECG.
Entiendo cómo funciona el ciclo cardiaco, se pueden categorizar los distintos tóxicos según su acción farmacológica14:
- Bloqueadores del eflujo de K: Como este ión es el principal responsable de la repolarización cardiaca, al bloquearse su conductancia por la membrana esta repolarización se prolongará, traduciéndose en un alargamiento del segmento QT. Como consecuencia de esta prolongación en la repolarización, la diferencia de potencial entre las distintas células miocárdicas disminuye, lo que puede provocar la activación de nuevas corrientes de depolarización, que eventualmente generen un nuevo potencial de acción, progresando a un circuito de reentrada que se traduzca en una arritmia ventricular (taquicardia ventricular, Torsades de pointes)15.
Dentro de los fármacos asociados a este fenómeno se encuentran: Antihistamínicos, Antipsicóticos, Citalopram, Antiarrítmicos (Clase IA, IC, III), ATC, Quinolonas y Macrolidos.
El manejo de este tipo de intoxicación debe ser con sulfato de magnesio IV, que actúa previniendo la aparición de Torsades de pointes.
- Bloqueadores del canal de Na: Al bloquear la entrada de este ión, que es el responsable de la fase de depolarización rápida del miocardio, se enlentecerá este proceso, traduciéndose en el ECG como un ensanchamiento del QRS. La prolongación del QRS puede desembocar en un patrón sinusoidal del ECG y eventualmente en asistolia. También, por el enlentecimiento de la conducción ventricular, pueden generarse circuitos de reentrada resultando de taquicardias ventriculares y fibrilación ventricular.
Fármacos asociados a este fenómeno son: Amantadina, Carbamazepina, Cloroquina, Antiarrítmicos (Clase IA y IC), Citalopram, Cocaina, ATC, Diltiazem, Verapamilo y Propanolol.
El manejo de estos pacientes debe ser con Bicarbonato de sodio IV, evitándose los antiarrítimicos clase IA y IC.
- Bloqueadores de bomba Na/k atpasa: Cuando se bloquea la acción de esta bomba, disminuye la gradiente de concentración de ambos iones a través de la membrana. Al disminuir la gradiente de Na ocurre un aumento de la actividad del intercambiador Na/Ca lo que aumenta la concentración intracelular de Ca, lo que resulta en una mayor actividad de las miofibrillas del miocito (aumento del inotropismo). Además de esto, estos fármacos pueden provocar un aumento del tono vagal y un bloqueo del nodo sinoauricular. Ambo fenómenos resultan en un aumento del automatismo cardiaco asociado a un bloqueo AV, lo que puede provocar variadas arritmias, siendo las manifestaciones más frecuentes los impulsos ventriculares prematuros, taquicardia auricular paroxística con bloqueo variable y el ritmo de la unión acelerado. Además de esto, es frecuente ver signos de hiperkalemia en el ECG.
Estos fenómenos son característicos de la sobredosis por digitálicos, aunque pueden producirse con la ingesta de plantas que tienen alta concentración de sustancias con el mismo efecto (Lirio de los valles, Laurel en flor, Drimia marítima).
Para el manejo de estos pacientes, lo más efectivo es el uso de fragmentos Fab anti-digoxina (no disponible en todos los servicios de urgencia). Otras medidas que se pueden usar es la Atropina para revertir el bloqueo AV. La fenitoina aumenta el umbral para la fibrilación ventricular y mejora la conducción AV por lo cual es otra medida aceptada para el tratamiento16. Deben evitarse los antiarrítmicos que disminuyan la conductividad del nodo AV (Procainamida, Quinidina)
- Bloqueadores del canal de Ca: Al bloquear la conductancia de este ión hacia el espacio intracelular se produce una disminución de la velocidad de conducción, de la contractilidad y del gasto cardiaco, debido a las funciones en que participa este ion dentro de la célula. Además de esto, también ejercen una acción vasodilatadora sistémica, con lo que contribuyen a generar hipotensión. En el ECG puede apreciarse tanto bradiacardia sinusal como bloqueo AV de grado variable, pudiendo llegar a la asistolía. Además de esto, también puede producirse un ensanchamiento del QRS similar al revisado anteriormente, con las mismas consecuencias mencionadas.
Estos fármacos son ampliamente utilizados en la clínica, cabe mencionar los bloqueadores dihidropiridinimicos (nifedipino, amlodipino, etc) y no dihidropiridinimicos (diltiazem, verapamilo).
El manejo de estos pacientes es complejo debido a que son propensos a desarrollar bradiarritmias severas e hipotensión. El tratamiento incluye atropina, calcio IV, glucagón, insulina, bicarbonato de sodio y drogas vasoactivas.
- Bloqueadores Beta-adrenérgicos: Actúan bloqueando los receptores de adrenalina a nivel cardiaco. La inhibición del receptor b1 resulta en una disminución de la contractilidad miocárdica, del ritmo cardiaco y de la conducción AV. El bloqueo en receptores b2 y α1, que producen algunos de estos fármacos, tienen acción a nivel metabólico, pulmonar y vascular principalmente. Los efectos de la intoxicación por estos medicamentos son bradicardia, bloqueo AV de grado variable e hipotensión.
Existen distintos fármacos de esta familia, de los más utilizados encontramos al propanolol, atenolol, bisoprolol, carvedilol, sotalol, entre otros.
Cabe mencionar que algunos de estos fármacos tienen acción en otros canales. Por ejemplo, el propanolol tiene acción sobre canales de calcio y canales de sodio, por lo que pueden tener otras manifestaciones del ECG asociadas a estos efectos.
El tratamiento de estos paciente incluye el uso de atropina, glucagón, insulina, calcio IV y drogas vasoactivas.
Como se puede apreciar, existen fármacos que pueden actuar sobre más de un canal o bomba, por lo cual tener una combinación de manifestaciones electrocardiográficas.
- Conclusiones
- – Las intoxicaciones son un problema de salud pública debido a que generan alta mortalidad por un evento potencialmente evitable.
- – Un toxico puede ser cualquier sustancia en una dosis específica, por lo cual cualquier medicamento puede actuar como tóxico si existe una sobredosis.
- – La multiplicidad de agentes que pueden actuar como tóxico implica que haya una multiplicidad de síndromes que lo pacientes pueden presentar y que el médico debe enfrentar.
- – Al enfrentar un paciente intoxicado se debe privilegiar siempre en primer lugar la estabilización del paciente, dejando la identificación del tóxico para un paso posterior o hacerlo paralelamente siempre que sea posible.
- – La mayoría de los pacientes se presentaran asintomáticos en el servicio de urgencia, pero todo requieren monitorización ya que en gran parte de los casos pueden comportarse en forma impredecible.
- – La anamnesis y examen físico pueden ser fundamentales al momento de determinar un tóxico desconocido.
- – Los exámenes de laboratorio útiles en el diagnóstico son acotados, y deben ser conocidos por el médico de urgencias.
- – El ECG es una herramienta fundamental en el manejo de estos pacientes, ya que la gran mayoría de los tóxicos tienen una acción cardiovascular que puede resultar en la muerte del paciente, por lo cual su comprensión es fundamental para el diagnóstico y manejo del paciente intoxicado.
Referencias
- Mowry JB, Spyker DA, Brooks DE. 2014 Annual Report of the American Association of Poison Control Centers’ National Poison Data System (NPDS): 32nd Annual Report. Clin Toxicol (Phila). 2015;53(10):962-1147. doi: 10.3109/15563650.2015.1102927.
- Mena H, Cristián, Bettini S, Marli, Cerda J, Patricia, Concha S, Flor, & Paris M, Enrique. (2004). Epidemiología de las intoxicaciones en Chile: una década de registros. Revista médica de Chile, 132(4), 493-499. https://dx.doi.org/10.4067/S0034-98872004000400013
- Erickson TB1, Thompson TM, Lu JJ. The approach to the patient with an unknown overdose. Emerg Med Clin North Am. 2007 May;25(2):249-81
- Mokhlesi B, Leiken JB, Murray P. Adult toxicology in critical care: part I: general approach to the intoxicated patient. Chest. 2003 Feb;123(2):577-92.
- Hoffman RS, Goldfrank LR. The poisoned patient with altered consciousness. Controversies in the use of a ‘‘coma cocktail.’’ JAMA 1995;274:562–9.
- Vale JA, Kulig K. Position paper: gastric lavage. J Toxicol Clin Toxicol 2004;42:933–43.
- Chyka PA, Seger D, Krenzelok EP, et al. Position paper: single-dose activated charcoal. Clin Toxicol (Phila) 2005;43:61–87.
- Pond SM. Extracorporeal techniques in the treatment of poisoned patients. Med J Aust 1991;154:617–22.
- Position paper: ipecac syrup. J Toxicol Clin Toxicol 2004;42:133–43.
- American Academy of Clinical Toxicology. Position paper: cathartics. J Toxicol Clin Toxicol 2004;42:243–53.
- American Academy of Clinical Toxicology. Position paper: whole bowel irrigation. J Toxicol Clin Toxicol 2004;42:843–54.
- Albertson TE, Dawson A, de Latorre F, et al. TOX-ACLS: toxicologic-oriented advanced cardiac life support. Ann Emerg Med 2001;37(4 Suppl):S78–90
- Mohrman DE, Heller L. Cardiovascular Physiology, 8e; 2014 Available at: http://accessmedicine.mhmedical.com/content.aspx?bookid=843§ionid=48779650 Accessed: January 20, 2017
- Holstege CP, Eldridge DL, Rowden AK. ECG manifestations: the poisoned patient. Emerg Med Clin North Am. 2006 Feb;24(1):159-77, vii.
- Nelson LS. Toxicologic myocardial sensitization. J Toxicol Clin Toxicol 2002;40(7):867–79.
- Irwin J. Intensive care medicine. In: Kirk M, Judge B, editors. Digitalis poisoning. 5th edition. Baltimore: Lippincott Williams & Wilkins; 2003.

