Nivel de manejo del médico general: Diagnóstico: Sospecha. Tratamiento: Inicial. Seguimiento: Derivar.
Aspectos esenciales
- Alteración celular que se origina en el epitelio del cuello del útero, de lenta y progresiva evolución.
- En Chile constituye un importante problema de salud pública.
- Casi el 100% de los tumores se relacionan con VPH.
- La citología exfoliativa (papanicolau, PAP) constituye una herramienta de tamizado fundamental.
Caso clínico tipo
Mujer de 45 años sin antecedentes mórbidos consulta por metrorragia. Nunca se ha realizado PAP. Al examen con espéculo se visualiza lesión exocervical proliferativa, sangrante y friable.
Definición
El cáncer cervicouterino (CaCu) es una alteración celular que se origina en el epitelio del cuello del útero, de lenta y progresiva evolución. Se manifiesta inicialmente a través de lesiones precursoras que se suceden generalmente en etapas. Abarcando desde un cáncer in situ, cuando compromete sólo a la superficie epitelial, hasta un cáncer invasor, cuando el compromiso traspasa la membrana basal.
Etiología-Epidemiología-Fisiopatología
Etiología: La OMS reconoce varios tipos histológicos, siendo los dos principales de cáncer invasor el carcinoma de células escamosas (80-85%) y Adenocarcinoma (10-12% de todos los casos). Casi el 100% de los tumores indicados están relacionados con el virus papiloma humano (VPH) de alto riesgo oncogénico (sobre todo VPH 16 y 18).
Epidemiología: El Cáncer Cervicouterino en Chile constituye un importante problema de salud pública. Ocupa el sexto lugar de muertes por cáncer en mujeres y el primer lugar en tasa de años de vida potencialmente perdidos con 129 por 100.000 mujeres. El año 2008 fallecieron 636 mujeres, con una tasa total de mortalidad para ese año de 7,5 por 100.000 mujeres y una tasa ajustada de 5,9 por 100.000 mujeres (según el MINSAL). El 48,4% de las muertes se produce en mujeres entre 35 y 64 años. Al comparar la tasa observada de mortalidad entre los años 1987 y 2008 en mujeres del grupo objetivo del Programa Nacional de Cáncer Cervicouterino (Entre 25 y 64 años) se observa una disminución en un 57,3%. En mujeres menores de 25 años la mortalidad es ocasional y a partir de los 45 años se produce un ascenso progresivo en la tasa. La distribución por etapas, según clasificación FIGO de los casos diagnosticados muestra que el 68,3% se diagnostica en etapas precoces (etapa I y II) y el 7,7% en etapa IV (no se tiene información de los casos nuevos diagnosticados por el Sistema Privado de Salud).
Diagnóstico
1) Prevención Primaria:
- La implementación de programas institucionalizados de educación a la población favorece la prevención y control de cáncer cervicouterino incluyendo actividades en terreno y la participación de equipos interdisciplinarios.
- Incorporar en los programas de educación para la salud la prevención de factores de riesgo; edad temprana al primer coito, múltiples parejas sexuales, multiparidad (7 o más partos), antecedentes de infecciones de transmisión sexual, tabaquismo, inmunosupresión, malnutrición, uso prolongado (mayor de 5 años) de anticonceptivos orales.
- Control de cáncer cervicouterino: Vacunar contra VPH 16 y 18 a mujeres que no hayan tenido contacto con los genotipos incorporados en la vacuna, como complemento de un Programa de tamizaje con citología.
- Tamizaje:
• Toma de muestra citológica del cuello uterino (PAP) a las mujeres entre 25 y 64 años con una periodicidad de 3 años
• Lograr y mantener cobertura con PAP vigente iguales o mayores al 80% en mujeres de 25-64 años, reduce la morbimortalidad por cáncer cervicouterino.
• Utilizar un sistema único para reportes citológicos.
• Optimizar el funcionamiento de los laboratorios de citología con énfasis en control de calidad y productividad
• Pacientes que presenten una lesión atípica de significado indeterminado deberán repetirse un PAP a los 4-6 meses. Luego de dos PAP (-) podrán volver a tamizaje de rutina.
2) Sospecha diagnóstica: Definición de caso sospechoso (GES): PAP positivo, es aquel PAP que presente alguna de las siguientes situaciones:
a. PAP sugerente de cáncer invasor.
b. PAP sugerente de Neoplasia Intraepitelial (NIE I, II y III o Ca in Situ).
c. Primer PAP Atípico que no pueda descartar lesión de alto grado o mayor.
d. Primer PAP Atípico glandular.
e. Segundo PAP Atípico inespecífico.
3) Sospecha Clínica: Visualización a la especuloscopía de lesión exocervical proliferativa, sangrante y/o friable
Toda mujer con un informe de PAP positivo y/o con sospecha clínica de cáncer de cuello uterino, debe ser derivada a consulta por especialista.
4) Confirmación diagnóstica:
• La confirmación diagnóstica de lesiones preinvasoras o Cáncer Cervicouterino, requiere del informe histológico, emitido por médico anatomopatólogo y su tratamiento debe realizarlo un equipo especialista.
• La colposcopía es el primer procedimiento para confirmación diagnóstica, en todas las pacientes, excepto en aquellas con lesión macroscópica evidente.
• De acuerdo a hallazgos del examen colposcópico y criterio médico, el examen para confirmación diagnóstica es la Biopsia Endo y/o exocervical. Cuando la colposcopía es insatisfactoria o cuando la alteración citológica es una atipia glandular la indicación es un Legrado endocervical (Anexo b)
• Conización cervical es un procedimiento diagnóstico y eventualmente terapéutico en los casos que se sospeche una microinvasión o disociación colpo-citohistológica en mujeres no embarazadas.
• Etapificación del cáncer cérvico uterino Se recomienda utilizar la clasificación de FIGO para etapificar el cáncer.
• Realizar estudio de rutina (hemograma, glicemia, protrombinemia, creatininemia, urocultivo, orina completa, ECG), realizar TAC de pelvis y abdomen o RM para los estadios IB o superiores.
• Realizar además TAC de tórax, cistoscopía y rectoscopía en estadios III y IV clínicamente sospechosos.
Tratamiento
1. Tratamiento de lesiones preinvasoras y recidivas NIE I:
• Con antecedente de citología previa de Bajo grado o atípico inespecífico (Anexo c):
• Con colposcopía satisfactoria se recomienda seguir a las pacientes con control citológico cada 6 meses o con tipificación viral para VPH a los 12 meses
• Si tipificación viral negativa a los 12 meses o 2 controles citológicos consecutivos negativos, puede volver al programa rutinario de tamizaje
• Ante una NIE I persistente (2 años) las alternativas son continuar la observación o realizar tratamiento (ablativo o escisional).
• Con colposcopía insatisfactoria o legrado endocervical positivo o paciente fue tratada, se recomienda cono escisional
• Con antecedente de citología previa de alto grado o atípico glandular: Se puede realizar diagnóstico escisional u observación con colposcopía y citología cada 6 meses por 1 año.
Si colposcopía satisfactoria y legrado endocervical negativo:
• Se recomienda realizar diagnóstico escisional si repite citología de alto grado
2. Tratamiento de lesiones intraepiteliales NIE II y III / Cáncer In Situ:
• Con colposcopia satisfactoria el tratamiento indicado es la conización.
• Con colposcopía insatisfactoria está indicada la conización escisional diagnóstica.
• En este tipo de lesiones la histerectomía no está indicada, excepto en condiciones especiales (NIE II o más persistentes o recurrentes)
• La Histerectomía es la alternativa de elección en una mujer que ha completado su paridad y tiene el diagnóstico de Adenocarcinoma in situ (AIS) en un cono.
3. Tratamiento de cáncer cérvico uterino según etapa clínica:
I.- EtapaI IA1 y IA2:
▪Paciente etapa IA1 Sin compromiso vascular ni linfático se sugiere histerectomía total extrafascial o tipo I de Piver. Si desea preservar fertilidad se recomienda conización
▪Paciente etapa IA2 se recomienda histerectomía radical con linfadenectomía pélvica. Si quiere conservar fertilidad se puede realizar traquelectomía radical
▪Pacientes en etapa IAI y IA2 con contraindicación de cirugía se puede realizar radioterapia intracavitaria exclusiva
II.- Etapa IB1: el tratamiento de elección es la histerectomía radical tipo Piver II o III y linfadenectomía pelviana completa bilateral. Como alternativa se puede utiliza la radioterapia con un porcentaje similar de curación.
III.- Etapa IB2 a IVA: el tratamiento de elección es la Radioterapia concomitante con quimioterapia con cisplatino.
IV.- Etapa IV B: se realiza terapia paliativa.
4. Tratamiento de recidiva de cáncer invasor
En caso de recidiva loco-regional se sugiere radioterapia en pacientes tratados primariamente con cirugía. Por otro lado, el rescate quirúrgico, se sugiere en pacientes en que el tratamiento inicial fue radioterapia.
Seguimiento
Lesiones preinvasoras y recidivas NIE I: Mencionado como parte del tratamiento.
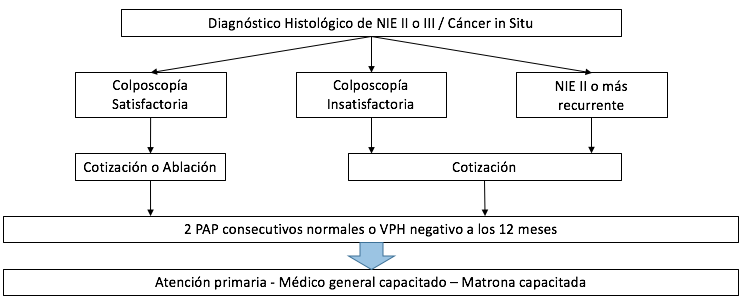
Lesiones intraepiteliales NIE II y III / Cáncer In Situ:
• Se puede realizar con tipificación VHP a los 6-12 meses, citología exclusiva o combinada con colposcopía cada 6 meses, colposcopía más legrado endocervical en mujeres VPH positiva o citología con PAP atípico inespecífico o más
• Si presentan tipificación viral negativa a los 12 meses o 2 controles citológicos consecutivos negativos, puede volver a atención primaria.
Cáncer cérvico uterino:
• Se ha demostrado que el 17% de pacientes en etapa IB recurren; en etapas avanzadas el porcentaje de recurrencia es mayor.
• Los casos tratados por cáncer invasor, deben continuar el seguimiento por ginecólogo-colposcopista, de preferencia gineco-oncólogo con al menos examen clínico general, hemograma, urocultivo y dependiendo de la sintomatología específica o signos de diseminación, pueden solicitarse exámenes complementarios.
Frecuencia recomendada para los controles en el seguimiento:
o Control c/ 3 meses los dos primeros años.
o Control c/ 6 meses del 3° a 5° año.
o Control anual desde el 5° año en adelante.
ANEXOS
a. Recomendaciones GES 2015


b. Algoritmo de derivación a especialista o UPC de primer PAP atípico según clasificación Behtesda 2001
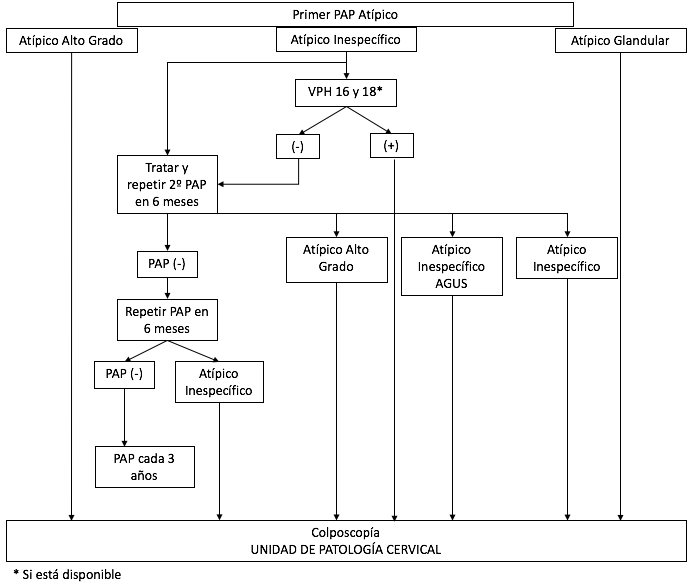
c. Algoritmos para confirmación diagnóstica.
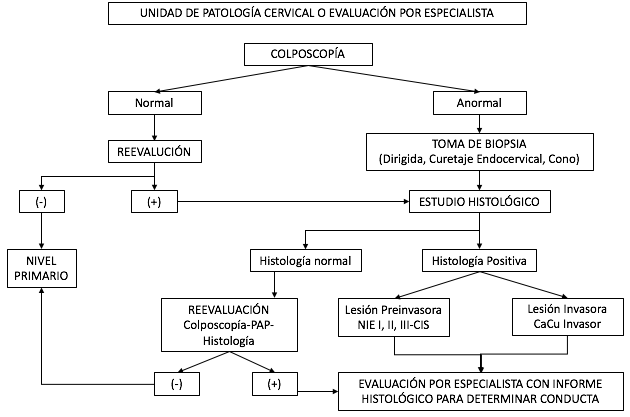
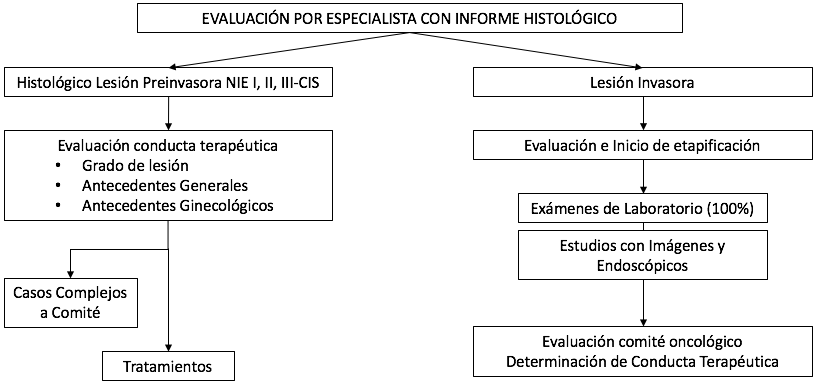
d. Algoritmo NIE de bajo grado.
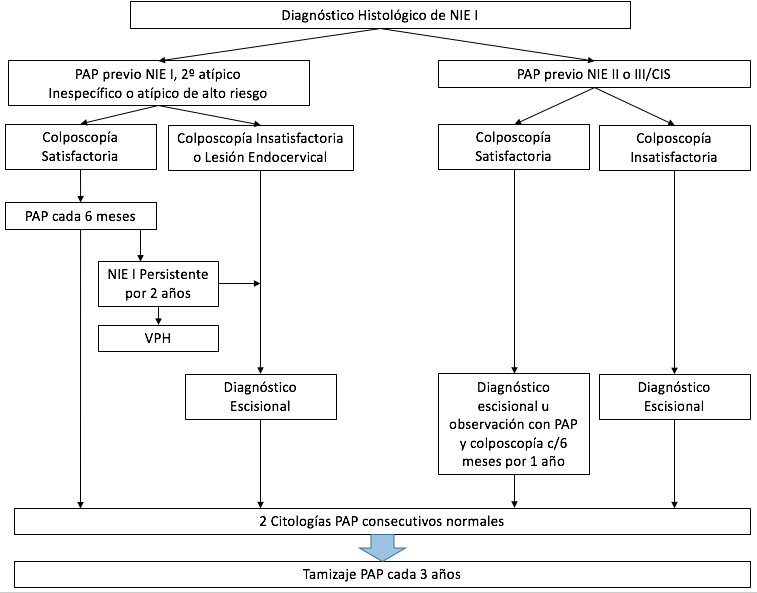
e. Algoritmo NIE alto grado.
Bibliografía:
http://web.minsal.cl/wp-content/uploads/2015/09/GPC-CaCU.pdf (Guia minsal 2015)







