INTRODUCCIÓN
El trauma es la primera causa de muerte entre 1 y 45 años, siendo responsable del 75% de las muertes de adolescentes entre 15 y 24 años y del 66% de las muertes de personas entre 25 y 34 años. De los pacientes que fallecen por trauma, el 60% lo hace en la etapa prehospitalaria, mientras que el 60% de los que fallecen en el hospital, lo hacen dentro de las primeras horas. El 10% de las causas de muerte en trauma están vinculadas a infecciones, la cual representa el 54% de las muertes después de las 48 horas y el 76% luego de 7 días. La infección en trauma suele relacionarse con la disfunción orgánica múltiple y esta puede presentarse en dos etapas: temprana (dentro de los primeros cuatro días) y tardía a partir del quinto día. La incidencia de infección nosocomial en pacientes traumatizados es del 24% según diferentes autores.
El riesgo de infección por trauma se produce por la ruptura de las barreras mecánicas, contaminación bacteriana exógena, factores locales de la herida (en especial tiempo de evolución al ingreso >6 horas), intervenciones diagnósticas y terapéuticas invasivas y disminución de la resistencia al paciente a las infecciones.
Bone, reportó que algunos pacientes traumatizados presentan Síndrome de Respuesta Inflamatoria Sistémica (SIRS), otros Síndrome de Respuesta Antiinflamatoria Compensatoria (CARS) con franca disminución de la respuesta inflamatoria, mientras que en otros predomina Síndrome de Respuesta Inflamatoria Antagonista Mixta (MARS), en los que la respuesta es equilibrada. Sin embargo, aún en los casos en donde predomina el CARS la infección no se asocia con gérmenes especiales, sino con los que habitualmente producen infecciones en pacientes críticos.
Factores de riesgo
Los factores de riesgo relacionados con la infección, dependen de las lesiones que provoca el traumatismo (tipo de herida y daño que produce) y los factores defensivos del huésped alteración de la barrera cutáneo-mucosa, desnutrición secundaria al estado hipercatabólico, inhibición de la quimiotaxis y adherencia de los neutrófilos, etc). Los traumatismos graves pueden causar serias alteraciones inmunitarias en el paciente comprometiendo tanto la inmunidad humoral como celular.
|
Tabla 1. Factores asociados a infección en pacientes traumatizados |
|||||
| Tipo de herida | Tejido desvitalizado | Cuerpo extraño | Contaminación exógena | Contaminación endógena | Riesgo de infección |
| Arma blanca | + | – | + | + | + |
| Bala de baja velocidad | ++ | + | – | ++++ | +++ |
| Bala de alta velocidad | ++++ | + | – | ++++ | ++++ |
| Escopeta |
+++ |
+++ | – | – | ++ |
| Quemadura | ++++ | – | ++++ | – | ++++ |
| Contusa | ++ | – | ++++ | ||
Tipos de infección en trauma
A. Infección asociada al trauma en sí mismo.
Se encuentra relacionada con situaciones como:
- Laceraciones infectadas
- Meningitis asociada a fractura de base de cráneo
- Empiema por trauma torácico penetrante (causa más común de empiema es el hemotórax inadecuadamente drenado)
- Infección intraabdominal debida a lesión de víscera hueca
- Osteomielitis en el sitio de fractura.
B. Infección asociada al cuidado de la salud
Esta se manifiesta durante o después de la internación del paciente traumatizado. Se define como aquella que no está presente ni incubándose en el momento de la admisión del enfermo salvo que salvo que haya sido contraída en una internación previa.
Categorías de contaminación
La infección asociada al trauma se debe a la contaminación de la lesión inicial, las que se describen a continuación:
- Contaminación exógena mínima: están comprendidas las heridas laceradas, por ejemplo, instrumental u objeto contuso-cortante limpio.
- Contaminación exógena grosera: heridas laceradas con material extraño, en general de extremidades por trauma contuso y mordeduras de animales. La mordedura de perro o gato suele producir una laceración o avulsión muy contaminada, por lo que la complicación infecciosa de la herida es muy probable. Las bacterias asociadas con esta provienen de la flora de la piel del paciente, pero sobre todo de la flora “normal” del animal. Por lo general, se manifiestan con celulitis focalizada dolor en el sitio de la mordedura y drenaje purulento con frecuencia maloliente. En menos del 10% de los pacientes se presentan fiebre adenopatía y linfangitis. La osteomelitis es una complicación grave y frecuente en este tipo de heridas, y debe sospecharse siempre en presencia de dolor en una articulación. El tratamiento de la herida implicará el lavado profuso y el desbridamiento agregado al uso de antibióticos. La elección del agente antimicrobiano correcto evitará la falla terapéutica y permitirá la resolución donde la mayoría de los patógenos involucrados son susceptibles a penicilina/amoxicilina.
- Posible contaminación endógena: fracturas de base de cráneo.
- Contaminación endógena definida: lesiones de víscera hueca y las del tracto genital.
- Sin contaminación exógena o endógena inmediata (o sin contaminación): lesiones cerradas de hígado, bazo, páncreas, riñón y fracturas cerradas.
FISIOPATOLOGÍA
Existe una estrecha relación entre el trauma y los factores que generan la infección, pudiendo llegar a instaurarse una sepsis en algunos casos, llegando a comprometer seriamente la vida del paciente. Dentro de estos factores, podemos destacar a las características constitucionales e inmunológicos del enfermo, aspectos del trauma (tipo de herida fracturas, quemaduras, aplastamientos, compromiso de vísceras) y los relacionados con el manejo clínico post-traumático (reanimación, protocolos invasivos, utilización de drogas). En general, cuanto peor es el daño producido por la lesión traumática, más posibilidades tiene el enfermo de adquirir una infección y, posteriormente, una sepsis.
Otro de los factores relacionados con el paciente, es la llamada respuesta de estrés o endocrino-metabólica y que está presente en estadios consecutivos al trauma. Comprende las siguientes alteraciones:
- Activación simpática, que produce vasoconstricción venular y arteriolar, incremento de la frecuencia cardíaca y de la contractilidad miocárdica, así como glucogenólisis y disminución de la liberación de insulina.
- Respuesta del sistema renina-angiotensina-aldosterona, que conduce a retención de sodio y agua y excreción de potasio.
- Secreción de ADH, que trae consigo incremento en la reabsorción de sodio y agua.
- Secreción de ACTH, que incrementa el catabolismo, la gluconeogénesis con aumento de aminoácidos, de glucosa en sangre y del cortisol plasmático, así como disminuye la percepción del dolor, lo que conduce a vasodilatación e hipotensión.
Se ha descrito que los tejidos lesionados son capaces también de generar estímulos neurogénicos y hormonales que provocan liberación de enzimas proteolíticas, polipéptidos y otras sustancias que, a su vez, son capaces de activar el sistema del complemento, de la coagulación y la cascada de plasminas y quininas. Además, se estimula el macrófago para liberar interleukina. Las citadas alteraciones son las responsables, entre otras, del catabolismo aumentado que aparece en el paciente con trauma y que eleva considerablemente sus requerimientos calóricos y proteicos.
En relación con el manejo del paciente, la reanimación en el sitio donde ocurrió el trauma debe encaminarse a garantizar la perfusión de los órganos vitales. La transportación y la asistencia en los diferentes sitios donde se le brinda la atención inicial constituye un encadenamiento de situaciones que deberá garantizar no sólo la supervivencia del lesionado, sino que procurará minimizar las posibilidades de adquirir una infección. Para esto, resulta vital el correcto cumplimiento de las normas epidemiológicas para la canalización de venas y arterias, la introducción de catéteres y sondas y la intubación de la vía aérea. Acciones como la adecuada limpieza y sutura de las heridas, la eliminación de tejidos necróticos, la reducción de las fracturas y el drenaje de colecciones y hematomas resultan elementos cuyo olvido imperdonable ha costado muchas muertes por sepsis.
Durante las horas o días consecutivos al trauma puede ser necesario someter al paciente a intervenciones quirúrgicas, muchas veces prolongadas, donde se imbrican el estrés quirúrgico de la operación y el uso de anestésicos que constituyen también factores condicionantes de sepsis.
El uso de antibióticos y esteroides debe ser evaluado profundamente Los primeros deben ser utilizados con orientación etiológica y con la precocidad requerida. El control del dolor ha sido enfatizado, pues se ha comprobado que desempeña un importante papel en la respuesta de estrés y en la respuesta inmune que desencadena la sepsis.
La acción del trauma (accidental o quirúrgico) en el sistema inmunológico ocasiona una disminución en la liberación de linfocitos y en la proliferación y liberación de linfocinas. Se ha evidenciado afectación de la quimiotaxis, depresión del funcionamiento de los linfocitos T y depresión de linfocitos B y macrófagos. Aparecen células supresoras funcionalmente activas, macrófagos esplénicos supresores y, algunos trabajos reportan la presencia de polipéptidos de bajo peso molecular con acción supresora en el suero, así como la liberación de interleukina 2 y prostaglandinas. Para evaluar el estado inicial y las variaciones posteriores en la inmunidad celular del lesionado se recomiendan pruebas de hipersensibilidad demorada con carácter seriado.
Se ha propuesto un esquema de patogénesis que describe cómo la infección libera toxinas microbianas que estimulan el sistema de defensa de los tejidos y producen en el organismo la llamada respuesta inflamatoria y puede ser de 3 tipos: adecuada, excesiva e insuficiente. En la primera, la infección va a ser controlada por el organismo, donde las toxinas microbianas son «aclaradas o neutralizadas» y el paciente sobrevive.
Cuando la respuesta inflamatoria es excesiva, los mediadores liberados ocasionan una agresión tisular con cambios metabólicos al nivel de células y tejidos, responsables de alteraciones clínicas que pueden conducir al shock, la disfunción orgánica y con frecuencia a la muerte. Y se considera inadecuada cuando la infección no se controla, y por lo tanto, la liberación continuada de toxinas microbianas puede exacerbar aún más la respuesta inmunológica mediante una excesiva liberación de mediadores inflamatorios. También las propias toxinas microbianas son capaces de producir una severa agresión tisular que termina casi siempre con shock, disfunción multiorgánica (DMO) y muerte.
INFECCIONES OPORTUNISTAS EN TRAUMA
Se define como oportunista a todo microorganismo que presenta capacidad para multiplicarse y producir enfermedades si el paciente presenta alteraciones en sus mecanismos de defensa. Es bien conocida la presencia de respuesta inflamatoria en trauma y de inmunosupresión. Sin embargo, el paciente traumatizado no se comporta como un inmunosuprimido clásico (post trasplante, inmunosupresores, HIV-SIDA, etc) excepto que presente algunas de estas patologías asociadas. Algunas infecciones que pueden encontrarse asociados a trauma son:
A. Infecciones con Cándida 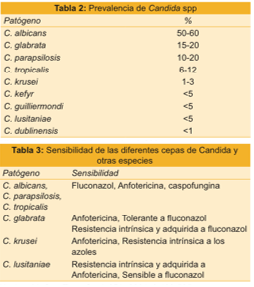
Las infecciones fúngicas han adquirido gran relevancia en las últimas décadas, debido a la mayor expectativa de vida de los pacientes, a la gravedad e inmunosupresión de los hospitalizados, al uso de métodos diagnósticos invasivos y terapéuticos, y al uso de múltiples esquemas antimicrobianos.
Generalmente, el hábitat de las especies de Cándida son la piel y las mucosas de los tractos gastrointestinal, genitourinario y respiratorio. Se encuentran colonizando la orofaringe en el 30-55% de las personas y pueden ser detectadas hasta en el 40-60% de la flora fecal normal. El tracto respiratorio también puede colonizarse en el 20-25% de los pacientes hospitalizados.
Cuando el paciente traumatizado tiene alguna situación predisponente, la cándida puede producir infección localizada (candidiasis mucocutánea, genitourinaria, respiratoria, etc) o generalizada (candidemia y candidiasis diseminada). El primer paso para el desarrollo de la infección por cándida es la colonización mucocutánea y, en particular, del tracto gastrointestinal.
La candidiasis sistémica puede ser dividida en: candidemia y candidiasis diseminada (infección orgánica por especies de cándida). Ambas pueden asociarse, y en particular, la segunda con disfunción o falla multiorgánica. En caso de candidemia, (4° organismo más comúnmente aislado en sangre), el paciente presenta fiebre de varios días que no responde a los antibióticos de amplio espectro, catéteres intravenosos por tiempo prolongado, varios factores de riesgo y signos clínicos de sepsis y de disfunción orgánica múltiple. En el 10% de los casos, puede asociarse con lesiones macronodulares y, entre el 10% al 30% de los casos, a endoftalmitis candidiásica. Es importante descartar la candidiasis asociada al catéter intravascular (que remite con la remoción del catéter), la tromboflebitis supurativa y la endocarditis (en particular, aórtica y mitral) y que puede asociarse con macroembolías sépticas en órganos mayores.
En la candidiasis diseminada, el paciente presenta compromiso de órganos en forma múltiple. Se trata de pacientes sépticos con fiebre que no responden a antibióticos de amplio espectro con hemocultivos negativos (incluso para cándida) y que tienen factores de riesgo. Puede asociarse con endoftalmitis candidiásica en el 10%-30% de los casos, candidiasis del SNC (meningitis, vasculitis granulomatosa, cerebritis difusa con microabscesos y aneurismas micóticos, etc.), candidiasis musculoesquelética (artritis, osteocondritis, osteomelitis y miositis), candidiasis cardíaca (miocarditis con abscesos miocárdicos y pericarditis), candidiasis peritoneal (habitualmente localizada, puede generalizarse en un 10 a 15% de los casos), candidiasis hepatoesplénica (abscesos esplénicos y hepáticos, con hiperesplenismo y hepatomegalia, colecistitis, etc.), entre otras. Existe una tendencia publicada en la literatura de infecciones a candida de especies no albicans, por lo que es muy importante diagnosticar precozmente la especie involucrada dado que algunas tienen resistencia al tratamiento habitual.
Los cultivos de sitios no estériles, aunque no son útiles en establecer el diagnóstico, pueden demostrar la colonización; en cambio, los cultivos de sitios estériles deben ser considerados significativos y hacer sospechar que la infección está presente. En los casos de candidemia o de candidiasis diseminada, los hemocultivos son positivos en el 50 – 60% de los casos.
El urocultivo puede ser de utilidad, aunque puede tratarse de colonización. En el cultivo de esputo o de la secreción respiratoria, el aislamiento de cándida puede considerarse como colonización; para realizar diagnóstico de infección respiratoria, la biopsia pulmonar es mandatoria. Las endoscopias bronquiales y digestivas permiten efectuar el diagnóstico y tomar muestra del material y el ecocardiograma permite la evaluación cardíaca y pericárdica. En la tabla 2 se muestran la prevalencia de las especies de Cándida.
El tratamiento de la candidiasis se basa en la localización de la misma, en el tipo de especie aislada y en la diseminación (candidemia, candidiasis diseminada). En los casos que haya dispositivos, consiste en la remoción de los mismos (catéteres venosos centrales, catéteres de diálisis peritoneal, sondas vesicales, etc.). En los catéteres venosos centrales no se recomienda el recambio por cuerda de piano (‘over the wire’). Si los catéteres no son removidos, la mortalidad se duplica. En la tabla 3 se muestra la sensibilidad de las diferentes cepas de Cándida y otras especies.
Si se trata de Candida albicans u otra cepa sensible, el tratamiento puede empezar con un azol como fluconazol (ver tabla 4). En caso de cepas resistentes a fluconazol (C. glabrata, C. Krusei y C. norvegensis) y sensibles a anfotericina-B deoxicolato (un polieno), debe comenzarse con anfotericina a dosis de 0.5 – 0.6 mg/kg/día (a pasar durante 2-4 horas). La administración tiene efectos colaterales como escalofríos, fiebre, taquipnea que disminuyen con la administración simultánea de esteroides y antiinflamatorios. El 30-50% de los pacientes pueden presentar nefrotoxicidad, en particular si se asocian otras drogas nefrotóxicas. Para disminuir este efecto adverso a nivel renal, se pueden emplear otras fórmulas lipídicas (LFAmB) que postulan mayor concentración, como el Complejo Lipídico Anfotericina (ABLC), la Anfotericina B en dispersión (ABCD) y la Anfotericina B Liposomal (AMB).
Las equinocandinas (caspofungina y anidulafungina), surgen como alternativa ya que conservan su actividad fungicida ante cepas resistentes a los azoles y a los polienos y, dado que actúan en la pared del hongo y no en las células humanas, mantienen un nivel de seguridad favorable. Se ha reportado que la caspofungina es tan efectiva en el tratamiento de candidiasis invasiva y candidemia como anfotericina-B. La tasa de respuesta favorable en pacientes con infección postquirúrgica (peritonitis candidiásica y abscesos intraabdominales) es alta.
B. Infecciones por Clostridium Difficile.
La infección por Clostridium difficile (ICD) es la causa principal de diarrea asociadas al cuidado de la salud en los países desarrollados. Se ha reportado que hasta 20% de los pacientes pueden estar colonizados a su ingreso a una sala general y que 8% puede desarrollar diarrea y/o colitis seudomembranosa. Se define a la ICD como la presencia de diarrea y la positividad en materia fecal de la toxina para C. difficile o una colonoscopía con hallazgos de colitis seudomembranosa.
El principal modo de transmisión de la ICD es de persona diseminada a través de la vía fecal-oral. La exposición a tratamientos antibióticos produce alteraciones de la flora intestinal normal permitiendo la infección oportunista del Clostridium difficile. La diarrea o aún las heces pastosas suelen presentarse luego de tratamientos antibióticos (dentro de las 8 semanas previas), en particular a cefalosporinas de 3° generación, aunque existan casos en los que el antecedente es de una sola dosis. Habitualmente, los pacientes muestran leucocitos en materia fecal y pueden desarrollar megacolon tóxico. Pueden cursar con fiebre, hipoalbuminemia y anasarca y marcado compromiso del estado general. Los factores de riesgo para el desarrollo de ICD son la edad (pacientes > 64 años), la internación prolongada, el uso de antibióticos y la exposición a otros pacientes con ICD.
La diarrea y la colitis se deben a la acción de las exotoxinas liberados por Clostridium difficile (toxina A y B) que son citotóxica y proinflamatorias. Los factores atribuibles al huésped determinan que el paciente presente una colonización o una colitis seudomembranosa grave. Tres factores pueden indicar una evolución grave o complicada y deben ser considerados al iniciar tratamiento: la edad, los leucocitos (> 15.000/mm3) y el nivel de creatinina sérica.
El diagnóstico se efectúa realizando enzimoinmunoensayo rápido de membrana para detección simultánea del antígeno glutamato deshidrogenasa de C. difficile y de toxinas A y B. La sensibilidad es del 87,8% y la especificidad es del 99,4%. El cultivo tarda 2-3 días, pero no descarta la colonización (portadores crónicos). La PCR es rápida, sensible y específica, pero no se recomienda rutinariamente. La rectosigmoidoscopía es el procedimiento diagnóstico de preferencia si no existen contraindicaciones para efectuarlo y muestra las típicas membranas, habitualmente en recto y colon sigmoideo.
El tratamiento de elección de la ICD moderada es metronidazol 500 mg cada 8 horas por vía oral y el ICD severa consiste en la administración de vancomicina en dosis de 125 mg cada 6 horas por vía oral, durante 10 – 14 días. En los casos de ICD severa y complicada se puede realizar tratamiento con vancomicina oral (500 mg cada 6 horas) o por recto en los casos de íleo (500 mg en 100 ml de solución salina cada 6 horas) con o sin metronidazol endovenoso 500 mg cada 8 horas. Deben evitarse las drogas que disminuyen el tránsito intestinal, suspender los antibióticos parenterales que no sean imprescindibles, hidratar adecuadamente al paciente y colocar al paciente en aislamiento de contacto. Las recaídas se observan en el 10 – 20% de los pacientes y deben ser retratados con el mismo esquema utilizando en el primer episodio. El metronidazol no debe ser utilizado más allá de la primera recurrencia. En algunos casos de refractariedad se ha sugerido el uso de la asociación de vancomicina con rifampicina (400 mg cada 12 horas por dos semanas). También se ha reportado la utilidad de la colestiramina (4 g cada 8 horas + lactobacillus 1 g cada 6 horas). Se ha evaluado, asimismo, la administración de inmunoglobinas IV en casos de recaída o refractariedad (150 a 400 mg/kg) o nitaxozanida. Se encuentra en estudio la utilidad de una vacuna contra la toxina.
C. Infecciones por Citomegalovirus.
La infección por citomegalovirus (CMV) se encuentra en todas las localizaciones geográficas. El 50 a 85% de la población adulta de los EUA tiene serología positiva. Es más común en países en desarrollo y en niveles socioeconómicos bajos.
Una vez que la persona se infecta, el virus permanece latente, residiendo en las células sin causar daño detectable o enfermedad clínica. La enfermedad recurrente rara vez sucede a menos que el sistema inmune de la persona se altere, ya sea por medicamentos o por enfermedad. Los grupos de alto riesgo son embarazadas, personas que trabajan con niños e inmunosuprimidos.
El CMV pertenece al grupo de la familia Herpesviriade como así también el virus herpes simple tipo I y II, varicela-zoster y Epstein-Bar. La transmisión ocurre de persona a persona, con íntimo contacto, a través de la saliva, orina u otros fluidos corporales (transmisión sexual, lactancia, órganos trasplantados y transfusiones). En paciente inmunocomprometidos, el problema no es tanto la infección por CMV es una causa importante de enfermedad y muerte. Las manifestaciones clínicas más frecuentes son la presencia de neumonía intersticial, retinitis, encefalitis, hepatitis y enfermedad gastrointestinal (enteritis).
Se ha reportado unos pocos casos que hacen sospechar que un huésped inmunocompetente puede desarrollar una reactivación endógena si se dan las condiciones necesarias (por ejemplo, sepsis). Asimismo, se han reportado reactivaciones endógenas en pacientes traumatizados.
En los pacientes pertenecientes a la UCI, la infección por CMV puede ser causada por vía transfusional. El espectro de enfermedad relacionada a infección postransfusional varía desde presentación asintomática hasta el síndrome mononucleósico con fiebre persistente (generalmente aparece dentro del mes de la transfusión) que no responde al tratamiento antibiótico y con cultivos bacteriológicos negativos. En el laboratorio se puede observar pancitopenia con linfocitosis atípica y moderada elevación de enzimas hepáticas. En los huéspedes inmunocomprometidos la infección postranfusional pueden tener serias consecuencias, incluyendo enfermedad diseminada fatal o neumonía intersticial difusa.
Los factores de riesgo para su reactivación son la presencia de sepsis al ingreso y tratamientos prolongados antes de la admisión a la UCI. La sepsis bacteriana se asocia con un riesgo 4,6 más alto de reactivación de CMV.
Además, se ha reportado la colitis ulcero-hemorrágica como manifestación de infección por CMV severa diseminada en paciente con trauma múltiple y que falleció por FOM. Sus características son ulceración hemorrágica, escasos infiltrados inflamatorios con células en ojo de búho, grandes células con infiltrado eosinofílico, por lo que se debe descartar colitis por CMV cuando la colitis seudomembranosa está sospechada pero no probada.
D. Infecciones por Herpes Simple.
El virus del herpes simple (HSV) es un patógeno común de distribución mundial. Existen dos tipos de HSV: el tipo I (HSV-1) y el tipo 2 (HSV-2). Las infecciones por HSV son asintomáticas en alrededor del 80% de los pacientes, pero en aquellos sintomáticos se caracteriza por la morbilidad y recurrencia, y en los huéspedes inmunocomprometidos puede generar infecciones severas y fatales. Las manifestaciones clínicas son herpes labial, genital, infecciones cutáneo-mucosas primarias o recurrentes. El modo de transmisión es de persona a persona. La infección ocurre por inoculación del virus en una mucosa susceptible.
Se ha reportado su presencia en pacientes traumatizados no previamente inmunosuprimidos que presentan neumonía por HSV. Los pacientes traumatizados críticamente enfermos tienen una alteración en la respuesta inmune que incluye la inmunidad mediada por células y esta alteración produce un aumento en la susceptibilidad a la infección por HSV. La enfermedad o la inmunosupresión pueden generar en un paciente con HSV oral latente la reactivación del virus. Una vez reactivado, el virus puede propagarse desde la boca al pulmón por inoculación directa. Sin embargo, solo el 10% de los pacientes presenta vesículas mucocutáneas antes del diagnóstico de neumonía por lo que la reactivación puede ser asintomática. La serología no es útil porque es tardía 10 días). La PCR en el lavadobroncoalveolar es un método rápido pero no puede diferenciar la contaminación de la orofaringe. El diagnóstico se efectúa por histología en el lavado broncoalveolar que muestra cuerpos de inclusión intranuclear de eosinófilos y el cultivo de virus. El 50% de los pacientes se asocian a neumonía bacteriana. El tratamiento se efectúa con acyclovir.
PREVENCIÓN DE LAS INFECCIONES
Medidas generales
Están enfocadas en efectuar:
- Resucitación adecuada y oportuna
- Adecuado cuidado de las heridas
- Profilaxis antitetánica
- Profilaxis quirúrgica de las heridas producidas por trauma (dosis plenas, tiempos cortos).
Medidas locales
Las medidas locales deben estar destinadas a:
- Cambiar dentro de las 24 horas las vías intravenosas (IV) colocadas de emergencia.
- Cambiar las vías V periféricas a las 72-96 horas.
- Observar el sitio de punción y estado de la curación de las vías centrales diariamente y retirar si hay fiebre o signos locales de infección
- Remover las vías arteriales no utilizadas.
- Los catéteres intraventriculares no deben permanecer más de 7 días y se debe cultivar el LCR al cambiar un catéter de PIC (si no hay contraindicaciones)
- Fiel cumplimiento de la higiene de manos en el área de atención del paciente y en todos los momentos de la misma.
A pesar de esto se deben considerar herramientas orientadas al control de la infección e incluyen: prevención de las infecciones asociadas a dispositivos (ventilación mecánica, catéter urinario, etc.), descontaminación del equipo del paciente, manejo de la ropa de cama y de los desechos, entre otras.
Es fundamental poseer en forma escrita normas o guías de procedimientos para prevenir estos tipos de infecciones asociados al cuidado de la salud, ya que de esta manera se pueden evaluar los procesos y el conocimiento de las mismas. Por lo tanto, es importante realizar acciones para disminuir las infecciones basado en incrementar la adherencia a lo que ya se conoce como efectivo, teniendo en cuenta la evidencia científica, y en utilizar las recomendaciones centradas en los pacientes en forma de bundles. Estos, se definen como el conjunto de prácticas necesarias para cuidar en forma eficiente y segura a los pacientes con distintos factores de riesgo, por ejemplo:
- Bundles para el cuidado de pacientes con catéter central:
- Lavado de manos
- Precauciones de barreras máximas
- Antisepsia de la piel con clorhexidina
- Elección de un sitio óptimo para la colocación del catéter con preferencia en la vena subclavia para un catéter no tunelizado
- Revisión diaria de la necesidad de permanencia del catéter, con remoción temprana del mismo
- Bundles para el cuidado de pacientes con asistencia ventilatoria mecánica:
- Elevación de la cabecera de la cama entre 30-45 grados
- Retiro precoz de la sedación y evaluación diaria para la extubación
- Profilaxis contra la enfermedad de úlcera péptica
- Profilaxis para la trombosis venosa profunda
- Bundles para el cuidado de pacientes con catéter urinario:
- Evitar catéteres vesicales innecesarios
- Colocar el catéter vesical con técnica aséptica
- Mantener los catéteres de acuerdo a las recomendaciones
- Revisar diariamente la necesidad de los catéteres y removerlos prontamente
CONCLUSIÓN
El trauma constituye la causa de muerte para el grupo etario entre 1 y 45 años de edad. La principal causa de muerte es el traumatismo de cráneo, seguido por la hemorragia. La infección es responsable globalmente del 10% de las causas de muerte, pero es la causa del 54% de las muertes luego de las primeras 48 horas y del 76% luego de la primera semana.
El cuerpo humano responde a la agresión mediante un síndrome de respuesta inflamatoria (SIRS), seguido por el CARS (compensatory antiinflamatory response syndrome) con franca disminución de la respuesta inflamatoria mientras que en otros, predomina MARS (mixed anti and inflamatory response syndrome) cuando la respuesta es equilibrada. Recientemente, se ha jerarquizado la importancia de las células T en la respuesta de la infección.
El paciente traumatizado puede desarrollar infecciones relacionadas con el trauma en sí mismo (lesiones de partes blandas, fracturas expuestas, traumatismo de víceras huecas, infecciones asociadas a la colocación de tubos de drenaje pleural) o infecciones del paciente crítico (neumonía asociada al ventilador, bacteremias asociadas a catéteres o infecciones urinarias). es muy importante conocer la flora autóctona microbiológica de la UCI para comenzar los tratamientos empíricos hasta la detección del microorganismo causante de la infección.
Se define como oportunista a todo microorganismo que presenta la capacidad para multiplicarse y producir enfermedad si el paciente presenta alteraciones en sus mecanismos de defensa. La presencia de respuesta inflamatoria en trauma y de alteraciones de la inmunidad lo pueden exponer a infecciones asociadas a candida, Clostridium difficile, a Citomegalovirus o Herpes simple, que deben tenerse en cuenta en el diagnóstico diferencial. Asimismo, se debe contar en la institución con un programa de control de infecciones, un programa de control de antibióticos y de bundles para la adecuada vigilancia infectológica y de prevención de infecciones.
Hay medidas preventivas que pueden aplicarse temprano al paciente y que disminuyen el riesgo de infección. Como medidas preventivas generales se recomienda la reanimación oportuna y adecuada, cuidados de la herida, profilaxis antitetánica y profilaxis antibiótica. Respecto al cuidado de la herida, el elemento fundamental a considerar es el tiempo de evolución de la herida y las características del mecanismo de lesión, donde este último se obtiene mediante la historia clínica. Además, es importante observar la presencia de tejido necrótico o elementos contaminantes (suciedad, heces, tierra, saliva) y la aparición de signos de infección.
Finalmente, es necesario contar con un programa de control de infecciones para definir las medidas de prevención en prácticas de alto riesgo, calcular las tasas de infecciones y detectar eventuales brotes epidémicos.
BIBLIOGRAFÍA
- Castro, B., Ponce, L., González, M., & Álvarez, D. (1997). Trauma y sepsis. Revista Cubana de Medicina Militar, 26(2). 129-140.
- Neira, J., Zitto, T., Stepanik, D., & Silva, C. (2013). Infecciones oportunistas en trauma. Panamerican Journal of Trauma, Critical Care & Emergency Surgery, 2(1). 1-13.
- Sociedad Argentina de Medicina y Cirugía del Trauma. (2002). Trauma: Prioridades. Editorial Médica Panamericana: Argentina.
- Tamanes, S., & Martínez, C. (1997). Cirugía: Fisiopatología general, aspectos básicos, manejo del paciente quirúrgico. Editorial Médica Panamericana: España.

