1. INTRODUCCIÓN
El shock es la expresión clínica de una falla circulatoria que asocia defectos de perfusión, traduciéndose en hipoxia celular y tisular dada una baja entrega de oxígeno, su mayor consumo o su utilización inadecuada. Inicialmente es un estado reversible, siempre que sea diagnosticado y tratado rápidamente para prevenir la progresión al estado de falla orgánica múltiple y muerte.
Es una condición común, que afecta a aproximadamente un tercio de los pacientes en unidades de paciente crítico.
El shock séptico, que es una forma de shock distributivo, es el más común en las unidades de cuidados intensivos, seguido por el cardiogénico e hipovolémico. En Chile, un estudio multicéntrico encontró una prevalencia de sepsis severa en pacientes críticos de 40%, con una mortalidad asociada de 27%.
El shock cardiogénico es la complicación más grave del infarto agudo al miocardio, con una mortalidad que oscila entre un 40 y 60%. El registro GEMI registró, entre el año 2001 y 2009, un 3,7% de infartos complicados con shock cardiogénico, con una mortalidad global del 55%.
El shock hipovolémico es una de las principales causas de muerte en pacientes quirúrgicos y politraumatizados, dando cuenta de la mayoría de las muertes potencialmente prevenibles, del 80% de las muertes intraoperatorias y de la mitad de las muertes en el primer día de hospitalización después de un trauma. Además, representa la principal causa de muerte en pacientes jóvenes, entre los 1 y 44 años.
En los servicios de urgencia, el porcentaje de cada tipo de shock depende de la población que éste atiende; así, por ejemplo, hospitales de trauma reciben mayor porcentaje de pacientes en shock hipovolémico.
2. FISIOPATOLOGÍA
Las determinantes fisiológicas de la perfusión tisular son el gasto cardíaco, correspondiente al producto entre el volumen expulsivo (dependiente de la precarga, contractibilidad miocárdica y postcarga) y la frecuencia cardíaca, y la resistencia vascular periférica, dependiente de la longitud de los vasos sanguíneos, la viscosidad sanguínea y el tono vascular.
Expuesto lo anterior, queda en evidencia que la alteración en cualquiera de las variables mencionadas anteriormente puede llevar a un estado de shock. En general, la fisiopatología subyacente a la mayoría de éstos implica un gasto cardíaco o una resistencia vascular periférica disminuida. La hipovolemia severa, el shock obstructivo y la etapa final del shock cardiogénico se caracterizan por un gasto cardíaco bajo y un aumento compensatorio de la resistencia vascular periférica para mantener la perfusión de los órganos vitales; en las fases iniciales del shock hipovolémico y obstructivo el gasto cardíaco puede ser normal. Por otra parte, el shock distributivo se caracteriza por resistencia vascular periférica y aumento compensatorio del gasto cardiaco. En algunos tipos de shock tanto el gasto cardíaco como la resistencia vascular periférica se mantienen en rangos normales, como ocurre en todos aquellos casos que involucran una disfunción mitocondrial (intoxicación por cianuro, monóxido de carbono, miopatías mitocondriales).
La hipoxia ocurre como resultado de una reducción en la perfusión tisular o en la entrega de oxígeno, y/o a un incremento en su consumo o a su utilización inadecuada. La hipoxia celular progresa a la disfunción en el transporte a nivel de membrana, edema intracelular, liberación de contenido intracelular al espacio extracelular y a una desregulación del pH intracelular. Estos procesos, reproducidos a nivel sistémico, conducen a acidosis y disfunción endotelial, que una vez agravados llevan a reducción de la perfusión tisular por alteraciones humorales y de la microcirculación que finalmente comprometen el flujo sanguíneo regional.
ETAPAS DEL SHOCK
Como entidad fisiopatológica el shock es un proceso continuo; sin embargo, clásicamente se divide en pre-shock, shock y disfunción orgánica múltiple. Las dos primeras son susceptibles de tratamiento y eventualmente pueden revertirse; a diferencia de la última, que progresa a daño orgánico irreversible y muerte.
- Pre-Shock O Shock Compensado. Los mecanismos compensatorios logran disminuir la hipoperfusión tisular. En este estado los signos vitales se encuentran al límite. Por ejemplo, en el shock hipovolémico temprano la compensación implica taquicardia y vasoconstricción periférica, que permite mantener asintomáticos a pacientes con hasta un 10% menos de volumen arterial efectivo.
- Shock. Los mecanismos compensatorios se ven sobrepasados, apareciendo signos y síntomas de hipoperfusión y disfunción orgánica como taquicardia sintomática, disnea, dificultad respiratoria, diaforesis, acidosis metabólica, hipotensión, oliguria y piel húmeda y fría. Cabe destacar que esta clínica se corresponde con una perturbación fisiopatológica importante; por ejemplo, en el shock hipovolémico la clínica se hace manifiesta con una disminución del 20-25% en el volumen arterial efectivo; mientras en el shock cardiogénico se requiere una disminución del índice cardíaco menor a 2.5 lts/min/m2.
- Falla Orgánica Múltiple. Durante esta etapa, dada la hipoperfusión e hipoxia generalizada mantenida se desarrolla falla renal aguda con anuria; la acidosis compromete el gasto cardíaco y la hipotensión se vuelve severa y refractaria a la terapia: la hiperlactatemia empeora y la dificultad respiratoria lleva a obnubilación y coma, siendo frecuente la progresión hasta la muerte.
3. APROXIMACIÓN INICIAL
Es recomendable comenzar la evaluación valorando la apariencia general del paciente; si está pálido, rubicundo, diaforético. Los signos vitales son de gran relevancia; frecuencia cardíaca, presión arterial, frecuencia respiratoria y saturación de oxígeno si está disponible. Respecto del laboratorio, lo más recomendado (y accesible en diferentes escenarios) es el electrocardiograma y glicemia capilar. Si está disponible, una ecografía de shock (rush) es de gran utilidad.
Al enfrentar un paciente hipotenso, taquicárdico, con signos de hipoperfusión tisular y lactato sérico elevado se está ante un paciente en shock. En ese contexto, si se cuenta con monitoreo hemodinámico invasivo, puede orientar hacia la etiología del cuadro. En general, si el gasto cardíaco es normal o alto, se trata de un shock distributivo, en el cual el ecocardiograma no evidencia alteraciones (cámaras cardíacas normales, contractibilidad conservada habitualmente). Si el gasto cardíaco es bajo, debe evaluarse la presión venosa central: si ésta es baja, se está ante un shock hipovolémico, y en el ecocardiograma se evidenciarán cámaras cardíacas disminuidas de tamaño y contractibilidad normal o incluso elevada. Por el contrario, si estamos ante una presión venosa central elevada, puede tratarse de un shock cardiogénico u obstructivo; la diferencia la hace el ecocardiograma, donde se evidencia ventrículos aumentados de tamaño con contractibilidad disminuida en el shock cardiogénico, y dilatación de ventrículo derecho con ventrículo izquierdo de menor tamaño en tromboembolismo pulmonar y pneumotórax, o derrame pericárdico con ventrículos disminuidos de tamaño si se trata de un taponamiento (Figura 1).
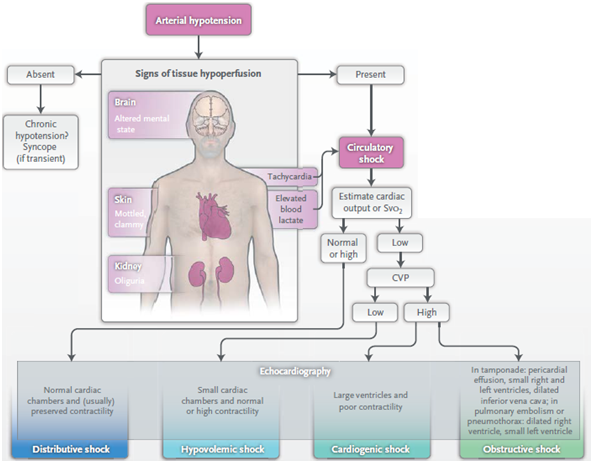
Figura 1. Aproximación inicial al estado de shock. Tomado de Circulatory Shock. N Engl J Med 2013;369:1726-34.
El soporte hemodinámico adecuado es crucial para prevenir la progresión del shock hasta la falla orgánica múltiple. La resucitación debe iniciarse aun cuando se trate de un shock indiferenciado; una vez se identifique la causa ésta debe ser corregida rápidamente.
El monitoreo invasivo ideal debe realizarse con una línea arterial y un catéter venoso central, para la resucitación con fluidos y drogas vasoactivas. El manejo inicial es orientado a problemas, y con metas orientadas a su resolución. Una nemotecnia útil para la resucitación es VIP: Ventilación (administración de oxígeno), infusión (resucitación con fluidos) y pump (bomba, drogas vasoactivas).
- Soporte ventilatorio. La administración de oxígeno debe ser inmediata, para aumentar su entrega a los tejidos y prevenir la hipertensión pulmonar. La monitorización con oximetría de pulso en este contexto no es válida, por lo que debe realizarse con gases arteriales o venosos. La ventilación mecánica (mediante máscara más intubación endotraqueal) tiene una utilidad limitada en el tratamiento del shock, dado que errores en la técnica pueden resultar rápidamente un paro cardiorrespiratorio. Sin embargo, puede ser necesaria en pacientes con disnea severa, hipoxemia o acidosis persistente (pH < 7.3); los beneficios de la ventilación mecánica invasiva radican en la disminución de la demanda de oxígeno por parte de los músculos ventilatorios, y en disminución en la postcarga del ventrículo izquierdo al incrementar la presión intratorácica.
- Resucitación con fluidos. En shock, se administran fluidos con el objetivo de favorecer el retorno venoso, con ello aumentar el gasto cardiaco y asi corregir la hipoperfusión. Todos los shock se benefician inicialmente de cargas de volumen; incluso en pacientes con shock cardiogénico se pueden iniciar pequeñas cargas y reevaluar; lo importante es la monitorización estricta dado los problemas que implica una volemización excesiva en ese contexto. La reanimación con fluidos debe efectuarse con una carga inicial; en forma precoz y protocolizada, no guiándose por metas macrohemodinámicas y cuidando la sobrevolemización, ya que ésta última asocia una serie de complicaciones posteriores que aumentan la mortalidad, asociadas a deterioro respiratorio (SDRA y menos frecuentemente, EPA) e hipertensión abdominal (en pacientes sometidos a cirugía abdominal, shock séptico, trauma, grandes quemados), y otras que dificultan el manejo posterior, como la mala cicatrización (por filtraciones), íleo o prolongación del tiempo en ventilación mecánica. Dado lo anterior, se recomienda administrar un bolo inicial, de 300 a 500 ml de solución en 20-30 minutos. Como aproximación inicial, se recomienda el uso de cristaloides, salvo en el subgrupo de pacientes con sepsis severa o hipoalbuminemia < 2,5 g/dL, donde un estudio demostró el beneficio de la reanimación con albúmina versus cristaloides, aunque hace falta más evidencia para establecerlo como una recomendación.
- Drogas Vasoactivas. Se utilizan cuando la hipotensión es severa o persiste a pesar de la administración de fluidos. Los agonistas adrenérgicos son la primera línea de vasopresores gracias a su rápido inicio de acción, alta potencia y corta vida media, lo que permite ajustar sus niveles fácilmente. La norepinefrina es la droga de primera elección; tiene propiedades principalmente a-adrenérgicas, con un modesto efecto b-adrenérgico que colabora en la mantención del gasto cardiaco. Su administración en general determina un aumento en la presión arterial. La dosis habitual es 0.1 hasta 2.0 mg por kilo/minuto. La dopamina tiene un efecto predominantemente b-adrenérgico a bajas dosis, y a-adrenérgico a dosis más altas, aunque es relativamente débil. Un estudio randomizado, controlado, doble ciego demostró que la dopamina no es mejor que la epinefrina como primera línea de droga vasoactiva, produce más arritmias y se asocia a mayor mortalidad dentro de los 28 días siguientes a su uso en pacientes con shock cardiogénico. Su uso también se asocia a mayor mortalidad versus norepinefrina en pacientes con shock séptico. La epinefrina tiene un riesgo aumentado de arritmias, disminuye el flujo sanguíneo esplácnico y puede incrementar los niveles de lactato sérico, probablemente debido al aumento del metabolismo celular. No se ha demostrado superioridad de la epinefrina sobre la norepinefrina en shock séptico, reservándose como droga de segunda línea en casos severos. En algunas formas de shock distributivo puede desarrollarse una deficiencia de vasopresina, en cuyos casos su administración a bajas dosis, asociada a norepinefrina puede favorecer el aumento de la presión arterial, lo que se traduce en un aumento en la sobrevivencia en shock no severo. La dosis no debe exceder los 0.04 U por minuto, y debe administrarse sólo en pacientes con gasto cardíaco alto. El agente ionotrópico de elección es la dobutamina. Su efecto es predominantemente b-agonista, y produce menos taquicardia que el isoprotenerol. Una dosis inicial pequeña suele bastar para incrementar sustancialmente el gasto cardiaco, siendo los 20 mg/kilo/min la dosis a partir de la cual no se agregan efectos benéficos de su uso.
Como parámetro de perfusión se utiliza el lactato sérico, asociado a peor pronóstico. Valores sobre 2 mmol/litro se consideran anormales, y >4 mmol/litro son sugerentes de hipoperfusión tisular. Su disminución >10% en 6 horas asocia una disminución de la mortalidad en 3 veces, y a su vez disminuye la necesidad de drogas vasoactivas.
4. DIAGNÓSTICO Y DIAGNÓSTICOS DIFERENCIALES
Se describen cuatro tipos de shock, no necesariamente exclusivos: cardiogénico, hipovolémico, obstructivo y distributivo. En general, los tres primeros se caracterizan por un gasto cardiaco bajo; en el shock distributivo, el déficit está en la periferia, debido a una resistencia vascular sistémica disminuida (Figura 2).
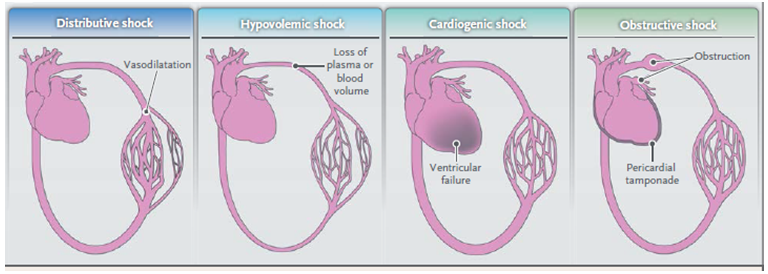
Figura 2. Representación esquemática de los cuatro tipos de shock. Tomado de Circulatory Shock. N Engl J Med 2013;369:1726-34.
a. SHOCK DISTRIBUTIVO
En el shock distributivo hay una mala distribución del volumen circulante. Incluye muchas causas, entre ellas shock séptico, SIRS, shock neurogénico, shock anafiláctico, shock relacionado a toxinas y de causa endocrina.

b. SHOCK CARDIOGÉNICO
En el shock cardiogénico hay una función cardíaca inadecuada; sea por inquemia, debido a una arritmia (ej. taquicardia ventricular sostenida) o una anormalidad mecánica (ej. ruptura valvular aguda).

c. HIPOVOLÉMICO
Hemorrágico (ej. trauma) o no hemorrágico (pérdidas de fluidos)

d. OBSTRUCTIVO
Se debe a una obstrucción circulatoria estracardíaca, que determinan una disminución de la precarga (ej. neumotórax a tensión, taponamiento cardíaco) o a alteraciones vasculares (tromboembolismo pulmonar).

5. CONCLUSIONES
- El shock corresponde a un estado de hipoxia celular y tisular resultado de una reducción en la entrega de oxígeno y/o un incremento en el consumo de oxígeno o a su utilización inadecuada.
- Se reconocen cuatro tipos de shock, aunque muchos pacientes presentan más de uno. Éstos son: Distributivo, Cardiogénico, Hipovolémico y Obstructivo.
- En general, los tres primeros se caracterizan por un gasto cardiaco bajo; en el último, el déficit está en la periferia, debido a una resistencia vascular sistémica disminuida.
- Como entidad fisiopatológica el shock es un proceso continuo. Sin embargo, se reconoce un pre-shock, donde los mecanismos compensatorios logran disminuir la hipoperfusión tisular, por lo que los signos vitales se encuentran al límite; el shock propiamente tal, cuando los mecanismos compensatorios se ven sobrepasados con repercusión clínica, y la disfunción orgánica múltiple, debido al estado de hipoxia sistémica sostenido.
- Como aproximación inicial a todo paciente en shock deben evaluarse los signos vitales. Como examen adicional, un electrocardiograma y glicemia capilar basta. Si está disponible, una ecografía de shock (rush) es de gran utilidad, especialmente en contexto de trauma.
- El manejo inicial de todo paciente en shock responde a la sigla VIP: Ventilatory support, administrando oxígeno al 100% por la vía que esté disponible y monitorizando con gases arteriales o venosos (salvo excepciones, no es necesario intubar al paciente); Infussion o volemización con un bolo inicial, idealmente de cristaloides, de 300 a 500 ml de solución en 20-30 minutos, y Pump (bomba), utilizando drogas vasoactivas cuando la hipotensión es severa o persiste a pesar de la administración de fluidos, siendo de primera línea el uso de norepinefrina en dosis de 0.1 hasta 2.0 mg por kilo/minuto.
- Como parámetro de perfusión se utiliza el lactato sérico; valores sobre 2 mmol/litro se consideran anormales, y >4 mmol/litro son altamente sugerentes de hipoperfusión tisular.
6. BIBLIOGRAFÍA
1. Kauvar DS & Wade CE. The epidemiology and modern management of traumatic hemorrhage: US and International perspectives. Critical Care 2005; 9: 1-9.
2. Johansson PI, Ostrowski SR, Secher NH. Management of major blood loss: An update. Acta Anaesthesiol Scand 2010; 54: 1039-1049.
3. Martín Valdebenito, Nicolás Veas, Dante Lindefjeld, José Luis Winter, Eduardo Guarda, Osvaldo Pérez, Manuel Méndez, Eugenio Marchant, Alejandro Fajuri, Alejandro Martínez. Características clínicas, predictores de mortalidad y resultados Inmediatos y a largo plazo en el tratamiento con angioplastía primaria del infarto agudo al miocardio con supradesnivel del ST complicado con shock cardiogénico. Rev Chil Cardiol 2014; 33: 116-122
4. Alberto Dougnac L, Marcelo Mercado F, Rodrigo Cornejo Ra, Mario Cariaga Va, Glenn Hernández P, Max Andresen H, Guillermo Bugedo T, Luis Castillo F. Prevalencia de sepsis grave en las Unidades de Cuidado Intensivo. Primer estudio nacional multicéntrico. Rev Méd Chile 2007; 135: 620-630
5. Jean-Louis Vincent, M.D., Ph.D., and Daniel De Backer, M.D., Ph.D. Circulatory Shock. N Engl J Med 2013;369:1726-34.
6. David F Gaieski, MD, Mark E Mikkelsen, MD, MSCE. Definition, classification, etiology, and pathophysiology of shock in adults. UpToDate 2016.
7. Dellinger RP, Levy MM, Rhodes A, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock: 2012. Crit Care Med 2013;41:580-637.
8. De Backer D, Biston P, Devriendt J, et al. Comparison of dopamine and norepinephrine in the treatment of shock. N Engl J Med 2010;362:779-89.
9. De Backer D, Aldecoa C, Njimi H, Vincent JL. Dopamine versus norepinephrine in the treatment of septic shock: a metaanalysis. Crit Care Med 2012;40:725-30.
10. Levy B, Perez P, Perny J, Thivilier C, Gerard A. Comparison of norepinephrinedobutamine to epinephrine for hemodynamics, lactate metabolism, and organ function variables in cardiogenic shock: a prospective, randomized pilot study. Crit Care Med 2011;39:450-5.

