Neumonía Adquirida en la Comunidad
28/10/2016
Nivel de manejo del médico general: Diagnóstico Específico Tratamiento Completo Seguimiento Completo
Definición
La Neumonía Adquirida en la Comunidad es definida por el Ministerio de Salud como la “inflamación aguda del parénquima pulmonar que puede comprometer alveolos, intersticio o ambos, cuya etiología es habitualmente viral, bacteriana, asociada (bacteriana-bacteriana) o mixta (bacteriana-viral), adquirida por la exposición a un microorganismo fuera del hospital, en un paciente inmunocompetente”.(1)
Epidemiología
A nivel mundial la neumonía es la primera causa de mortalidad en menores de cinco años. La OMS estima que la incidencia en este grupo de edad es aproximadamente 0,3 y 0,05 episodios por niño al año en países en vías de desarrollo y en países desarrollados respectivamente. Esto significa que cada año existen alrededor de 156 millones de nuevos casos de los cuales el 96% ocurre en países en desarrollo. Las naciones que mayor número de episodios registran son India, China y Pakistán.(2)
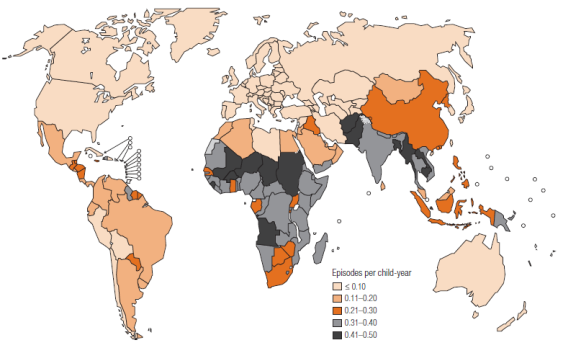
Figura 1. Incidencia de casos clínicos de neumonía por país. Imagen original de Bulletin of the World Health Organization 2008;86:408–416.
Por otro lado, se estima que entre el 7% y el 13% de los casos serán lo bastante graves como para requerir hospitalización. Respecto a la mortalidad asociada, la neumonía es causa de un 19% de las muertes de niños menores de 5 años, y más del 70% de estas ocurren en países del sudeste asiático y áfrica subsahariana.(2)
En Chile, según las estadísticas más recientes del Departamento de Estadísticas e Información en Salud (DEIS) en el grupo de menores de 5 años, la neumonía representó:
- El 0.15% de las consultas de urgencia el año 2017.
- El 42% de las hospitalizaciones por causa respiratorias y el 13% del total el año 2012.
- La primera causa identificada de muerte el año 2015.
Fisiopatología
La neumonía clínica es a la vez el resultado de la multiplicación de microorganismos a nivel alveolar, así como de la respuesta inmune del huésped desencadenada por ellos. Dichos microorganismos pueden llegar a los alveolos de distintas maneras:(3)
- Aspiración desde la orofaringe (lo más frecuente)
- Inhalación de gotitas contaminadas
- Propagación hematógena (raro)
- Por contigüidad con otros espacios adyacentes infectados, como el mediastino o pleura.
Entre las defensas del huésped se encuentran principalmente las mecánicas (vibrisas, cornetes de las fosas nasales, aclaramiento mucociliar, tos y reflejo nauseoso) y celulares (macrófagos alveolares).
Cuando dichas medidas son sobrepasadas y ocurre proliferación de microorganismos, será la respuesta inmune del huésped la que cause el síndrome clínico de la neumonía. Los macrófagos locales desencadenan una respuesta inflamatoria con liberación de mediadores que ocasionarán la fiebre, el reclutamiento de neutrófilos (y por ende la leucoitosis propia de las infecciones) y una fuga alveolocapilar (reflejada en las imágenes radiológicas con infiltrados y estertores en la auscultación). Finalmente, estos cambios también tendrán repercusión en la dinámica respiratoria con disnea, aumento del esfuerzo respiratorio y en consecuencia alcalosis respiratoria.(3)
Los procesos mencionados, tiene también una correlación con cambios histopatológicos (descritos preferentemente en la neumonía neumocócica), que pasan por varias fases:(3)
- Edema: etapa inicial en la cual se identifican bacterias en los alveolos y un exudado predominantemente proteínico.
- Hepatización roja: en el exudado se identifican principalmente eritrocitos y neutrófilos y en forma secundaria bacterias.
- Hepatización gris: reflejo de una contención de la infección. Se detiene la extravasación de glóbulos rojos y la célula predominante es el neutrófilo, asociado a depósitos de fibrina. Ya no se detectan bacterias.
- Resolución: son degradados los restos de fibrina, bacterias y neutrófilos (cede la inflamación), y los macrófagos vuelven a ser la célula predominante en los alveolos.
En cuanto a los factores de riesgo para dquirir neumonía, diversos datos muestran que los más importantes serían déficit de lactancia materna exclusiva, desnutrición, bajo peso al nacer, contaminación del aire en lugares cerrados, hacinamiento y la falta de inmunización contra el sarampión.
Cuadro Clínico
La presentación de la neumonía en niños es muy variable, y dependerá de la edad, microorganismo y severidad del cuadro. Algunos de los signos y síntomas que se pueden encontrar en la neumonía infantil son:(4,5)
- Taquipnea: es el mejor predictor de neumonía (especificidad de 67% y sensibilidad de 74%), teniendo en cuenta que la frecuencia respiratoria normal se modifica con la edad. Se ha descrito una importante relación entre taquipnea e hipoxemia, aunque ésta puede estar ausente en un niño con gran aumento del trabajo respiratorio.
- Fiebre: signo común aunque inespecífico, y puede estar ausente en algunos casos (por ejemplo en infecciones por Chlamydia trachomatis, o en desnutridos severos)
- Tos: la presencia de tos asociada a fiebre es sugerente de neumonía, sin embargo, se debe tener en cuenta que los neonatos y lactantes más pequeños podrían no presentarla.
- Dolor: el dolor tipo pleurítico se presenta preferentemente en niños mayores (escolares y adolescentes y podría ser indicativo de derrame pleural. Así mismo una forma de presentación de la neumonía podría ser con dolor abdominal, referido desde lóbulos pulmonares inferiores.
- Tiraje: suele ser subcostal, intercostal o supraclavicular, y es el mejor indicador de neumonía grave.
Otros indicadores de máxima severidad son cianosis, quejido respiratorio, aleteo nasal, rechazo de líquidos, entre otros.(5)
El examen físico pulmonar igualmente es variable, dependiendo de la edad y la etiología. Destaca el clásico síndrome se condensación pulmonar, que está compuesto por los siguientes signos:(5)
- Disminución del murmullo pulmonar
- Estertores que no se modifican con la tos
- Soplo Tubario
- Aumento de las vibraciones vocales
- Broncofonía y pectoriloquia áfona
Por último, tal como ya se ha mencionado, la presentación clínica del cuadro variará también de forma importante según la edad del paciente:(1,4)
|
Anamnesis |
Examen Pulmonar |
|
|
Lactante |
< 3 meses: la presentación puede ser bastante sutil predominando el rechazo alimentario, irritabilidad, fiebre, taquipnea, apnea y retracciones. |
Es frecuente asculutar crépitos, así como signos de obstrucción pulmonar tales como espiración prolongada, sibilancias, roncus, disminución del murmullo pulmonar |
|
>3 meses: compromiso de estado general, quejido, taquipnea, aleteo nasal y retracciones |
||
|
Preescolar |
Cuadro más específico; tos expectorante, fiebre, calosfríos, y aumento del esfuerzo respiratorio |
Signos de condensación pulmonar: aumento de las vibraciones vocales, matidez, respiración soplante, crépitos. |
|
Escolar y adolescente |
Además de los síntomas clásicos también podrían tener como única manifestación dolor torácico (irritación pleural), dolor abdominal (neumonía basal) o rigidez de nuca (referido de lóbulos superiores) |
Tabla 1. Hallazgos clínicos más frecuentes de acuerdo a la edad del niño
AGENTES ETIOLÓGICOS
La neumonía puede ser causada por distintos microorganismos; virus, bacterias y hongos (estos últimos propios de las personas inmunodeprimidas). En los niños, la prevalencia de cada una de estas entidades tendrá una distribución típica dependiente de la edad.(1)
|
Microorganismo |
RN |
1 – 3 m |
4 – 24 m |
Preesc. |
Escolar |
|
Virus |
|||||
|
VRS |
+ |
+++ |
++++ |
++ |
— |
|
ADV |
— |
+ |
++ |
+ |
— |
|
Influenza |
— |
— |
+ |
++ |
+++ |
|
Parainfluenza |
— |
+ |
+ |
+ |
— |
|
MNV |
— |
+ |
+ |
+ |
— |
|
Bacterias |
|||||
|
S. pneumoniae |
+ |
+ |
++ |
++++ |
++++ |
|
M. penumoniae |
— |
– |
+ |
++ |
++++ |
|
H. influenzae |
— |
+ |
+ |
– |
– |
|
S. aureus |
+ |
+ |
+ |
+ |
+ |
|
S. agalactiae |
+++ |
+ |
– |
– |
– |
|
E. coli y otros Bacilos gram (-) |
++ |
+ |
– |
– |
– |
|
C. trachomatis |
– |
– |
– |
+ |
+ |
|
C. penumoniae |
– |
– |
+ |
+ |
++ |
|
S. Pyogenes |
– |
– |
– |
+ |
+ |
Tabla 2. Agentes etiológicos más frecuentes según edad. ADV adenovirus. MNV: metaneumovirus. VRS: virus respiratorio sincicial. Imagen original de Guía Clínica IRA baja de Manejo Ambulatorio en Menores de 5 años. MINSAL, 2013
Por otro lado, la presentación clínica, hallazgos radiológicos y en el laboratorio pueden ser muy variables y parte de esta diversidad está dada por los agentes causales que la desencadenan, que comprenden una gran multiplicidad de virus y bacterias. Debido a la importancia de su caracterización individual, a continuación se revisarán algunos de los agentes etiológicos con mayor importancia en la clínica pediátrica.
– Agentes VIRALES
Virus Respiratorio Sincicial (VRS)
- Agente etiológico más frecuente de neumonía en el lactante (<2 años).(7)
- Pertenece género Pneumovirus de la familia Paramixoviridae. Su genoma corresponde a ARN monocatenario de desentido negativo. Tiene dos subtipos A y B que usualmente se presentan simultáneamente en los brotes.(8)
- Estacionalidad: las epidemias ocurren durante el invierno, usualmente con peacks entre mayo y julio.(8)
- Transmisión e incubación: lo más común es la transmisión por contacto directo con secreciones o fómites contaminados, pero también pude ocurrir por aerosoles. El período de incubación es de 4 a 5 días y pude transmitirse hasta por 3 semanas.(7,8)
- Clínica: es ampliamente variable, desde un resfrío común hasta un enfermedad severa como bronquiolitis, neumonía e insuficiencia respiratoria.(7,8) Se pude presentar con fiebre moderada (<38,3ºC), sibilancias, crépitos, tos y retracciones, que pueden ser precedidas por sintomatología respiratoria alta por 1 a 3 días.(9) Otra forma de presentación, especialmente en lactantes pequeños puede ser con apnea, e incluso puede ser causa de muerte súbita.(8)
-
Radiografía: Se puede observar infiltrado intersticial perihilar, atelectasias subsegmentarias e hiperinsuflación.(
6)
- Diagnóstico: pude realizar con muestras de secreción nosofaríngea. La inmunofluorescencia directa tiene una sensibilidad de hasta 95% y para la confirmación se puede usar técnica de PCR, habitualmente incluida en ensayos múltiples.
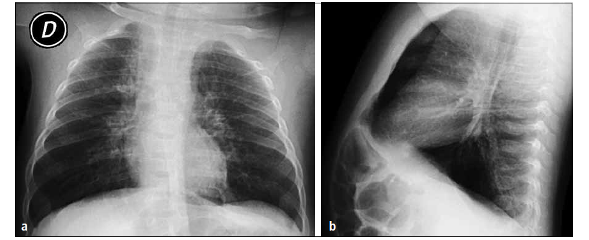
Figura 2. Radiografía AP (a) y lateral (b) que muestra infiltrado intersticial y severa hiperinsuflación. Imagen original de REV. MED. CLIN. CONDES – 2013; 24(1) 27-35
Adenovirus (ADV)
- Su mayor incidencia ocurre entre los 6 meses y los 2 años.(1) Se estima que causa el 10% de las hospitalizaciones en lactantes y preescolares.(7)
- Pertenece a la familia Adenoviridae y su material genético se encuentra codificado en ADN de doble cadena. Los serotipos que provocan neumonía son el 1, 2, 3, 5, 7 y 21 (el 2 y 7 se asocian a cuadros más graves).(7)
- Transmisión: las posibles vías de contagio incluyen aerosoles, fecal-oral y contacto directo con fómites contaminados.(10)
- Clínica: este virus posee una amplia gama de presentaciones. Se debe sospechar en pacientes con fiebre alta, disnea progresiva, tos persistente, faringitis, adenitis cervical, diarrea y exantema. El serotipo 5 se asocia a síndrome coqueluchoideo de curso prolongado. Se han descrito también secuelas pulmonares severas, tales como bronquiectasias y bronquiolitis obliterante (la más grave).(1,7)
- Radiografía: altamente variable; puede presentar patrón intersticial, mixto, e incluso consolidación pulmonar.(7,10)
- Laboratorio: parámetros inflamatorios (VHS, PCR, leucocitos) variables. Pueden mostrar patrón típicamente bacteriano.
- Diagnóstico: cultivo viral y PCR de aspirado nasofaríngeo tienen alta sensibilidad y especificidad, sin embargo el cultivo puede tardar hasta 28 días. La inmnofluerescencia tiene mal rendimiento (sensibilidad 38-65%).(11)
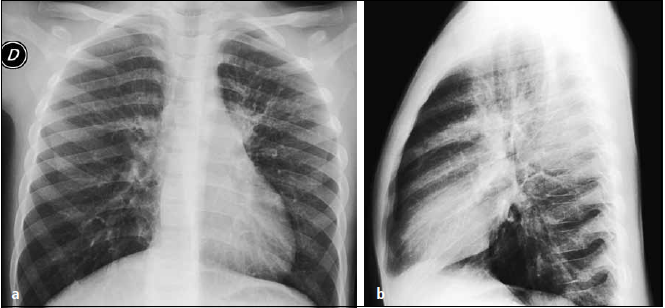
Figura 3. Radiografía AP (a) y lateral (b) que muestra patrón mixto que se puede hallar en infecciones por ADV, M. pneumoniae y otros. Imagen original de REV. MED. CLIN. CONDES – 2013; 24(1) 27-35
– Agentes BACTERIANOS
Streptococcus pneumoniae
- Principal causa de neumonía bacteriana en la infancia.(1)
- Corresponde a un coco gram (+) de la familia Streptococcaceae. Posee una cápsula de polisacáridos, no forma endosporas y es inmóvil. Es un anaerobio facultativo, catalasa (-). Se estima que son microorganismos residentes en un 5-401% de las vías respiratorias altas de los humanos. Los serotipos 6, 14, 19 y 23 son causa habitual de neumonía en niños.(7)
- Clínica: la presentación más clásica incluye fiebre elevada, tos, dolor pleurítico o abdominal. La auscultación puede presentar disminución del murmullo pulmonar, crépitos, broncofonía o respiración soplante.(7)
- Radiografía: la consolidación puede tardar hasta 24 horas (radiografías demasiado tempranas podrían originar falsos negativos). Lo más común será un patrón de condensación denso y homogéneo con broncograma aéreo, que en el caso de los niños puede tener forma redondeada (“neumonía redonda”), aunque eventualmente podría existir compromiso alveolar multifocal. Es necesario fijarse en ciertos sitios (perihiliar, zona retrocardíaca y bases) que pueden dar lugar a “neumonías ocultas”.(6)
- Laboratorio: los parámetros inflamatorios tendrán un patrón bacteriano (leucocitosis con predominio polimorfonuclear, VHS y PCR elevadas)
- Diagnóstico: la detección de antígenos de S. pneumoniae puede tener un alto valor predictivo negativo, y en líquido pleural alcanza una sensibilidad y especificidad >90%. El hemocultivo tiene mal rendimiento (positivo en <10%). En el caso de los ensayos múltiples con PCR, pueden ayudar a distinguir entre los distintos serotipos asociados a neumonía.
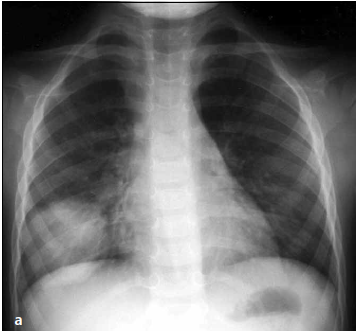
Figura 4. Radiografía de tórax AP que muestra neumonía redonda por S. neumoniae. Imagen original de REV. MED. CLIN. CONDES – 2013; 24(1) 27-35
Mycoplasma pneumoniae
- Primera causa de neumonía atípica en niños. Es el segundo agente más común en escolares y adolescentes, y tiene alta prevalencia en preescolares y lactantes que asisten a jardines infantiles.(1)
- Es un microorganismo muy pequeño, sin pared celular y con triple memebrana, por lo que no se tiñe al gram y es resistente a betalactámicos.(12)
- Se presenta en forma de brotes en primavera y verano en comunidades cerradas e instituciones. Tiene una incubación de 2 – 3 semanas.(1,12)
- Clínica: es un cuadro de evolución insidiosa, que se desarrolla en días a semanas. Su presentación es variable y generalmente leve, llegando sólo un 10% a un cuadro de neumonía.(7) Los síntomas más característicos serán tos prolongada (desde productiva hasta coqueluchoidea), fiebre, compromiso del estado general, polipnea leve y coriza. A la auscultación puede haber sibilancias y crepitaciones.(12)
- Manifestaciones extrapulmonares: se presentan en un 25 a 50% de los casos, siendo más comunes las dermatológicas (desde rash eritematoso maculopapular hasta síndrome de Steven Johnson), aunque puede afectar múltiples sistemas.
- Radiografía: muy variable, e inespecífica. Lo más frecuente es un patrón intersticial reticular de predominio basal o perihiliar, aunque también puede haber consolidación. Pueden existir atelectasias lineares y adenopatías perihiliares, y hasta en un 20% será bilateral y habrá derrame pleural. Se ha descrito comúnmente una “disociación clínico-radiológica” con abundantes hallazgos en la radiografía de un paciente oligosintomático.(5,12)
- Laboratorio: puede haber leve leucocitosis con predominio de poliorfonuclear, trombocitosis (respuesta de fase aguda) y elevación moderada de la VHS.(13)
- Diagnóstico: La detección serológica por ELISA tiene alta sensibilidad (93-100%) y especificidad (79-100%), y detecta IgM que se eleva tras la 1ª semana. La PCR tiene sensibilidad de 78-100% y sensibilidad de 92-100%.(12)
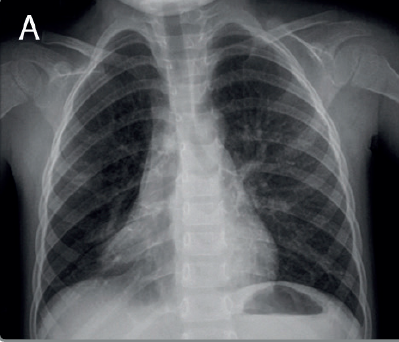
Figura 5. Radiografía de tórax AP que muestra neumonía cuasada por M. pneumoniae. Se observa condensación con pérdida de volumen del lóbulo medio, asociado a infiltrados intersticiales basales bilaterales. Imagen original de Neumol Pediatr 2015; 10 (3): 118 – 123
Chlamydia Penumoniae
- Se presenta con mayor frecuencia en adolescentes y escolares. No tiene predominio estacional.(1)
- Es una bacteria intracelular, gram (-) que contiene ARN y ADN ribosomal.(12)
- Clínica: altamente inespecífica. Habitualmente tiene un curso poco sintomático con evolución insidiosa que se puede confundir con un resfrío común, asociado a faringitis, ronquera y sinusitis. Sólo la minoría de los niños presentarán síntomas de neumonía.(12,14)
- Laboratorio: hemograma generalmente normal.(14)
- Radiografía: habitualmente infiltración en áreas irregulares de distribución segmentaria o subsegmentaria.(14)
- Diagnóstico: la técnica más usada es el factor inhibitorio de macrófagos (MIF) que mide IgM (se eleva en la 2ªo 3ª semana) e IgG (8ª semana). La PCR también tiene alta sensibilidad y especificidad.(12)
Chlamydia trachomatis
- La edad más frecuente de presentación es entre las 2 y 12 semanas de vida. El contagio de produce principalmente en el canal del parto.(1)
- Clínica: en general se presenta con un curso afebril, tos coqueluchoidea, taquipnea y conjuntivitis. El examen pulmonar puede ser normal o presentar escasos crépitos diseminados.
- Laboratorio: característicamente presenta eosifnofilia(1)
- Radiografía: importantes signos de atrapamiento aéreo (hiperinsuflación) e infiltrado intersticial bilateral difuso y microatelectasias.(5)
- Diagnóstico: el gold standard es el cultivo. Otras técnicas utilizadas son PCR, y ELISA e inmununofuoresencia directa para detectar antígenos.
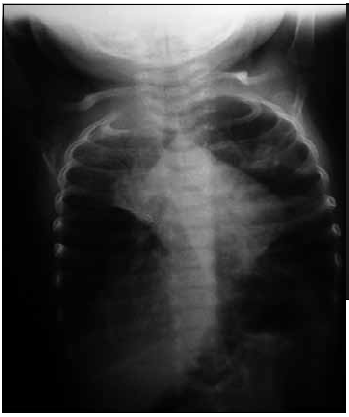
Figura 6. Radiografía de tórax AP que muestra neumonía causada por C. trachomatis con importante hiperinsuflación y múltiples atelectasias. Imagen original de Neumol Pediatr 2013; 8 (2): 66-73
Según lo revisado existirán distintas características del cuadro clínico, de los hallazgos radiográficos y de laboratorio que en su conjunto orientarán a la posible etiología del cuadro.
|
Bacteriana |
Viral |
Mycoplasma |
|
|
Edad |
Cualquiera |
Principalmente < 2 años |
5-15 años |
|
Estación |
Todo el año principalmente primavera |
Invierno* |
Todo el año |
|
Presentación |
Súbita |
Variable |
Insidiosa |
|
Fiebre |
Alta |
Variable |
Variable |
|
Taquipnea |
Común |
Común |
Poco frecuente |
|
Tos |
Escasa |
Frecuente |
Frecuente intensa |
|
Síntomas asociados |
Dolor torácico |
Coriza, conjuntivitis |
Exantema, artralgia, otalgia |
|
Auscultación |
Evidencia de consolidación |
Patrón obstructivo más usual |
Crépitos, sibilancias |
|
Hemograma |
Leucocitosis con desviación a izq. |
Variable |
Inespecífico |
|
PCR |
Alta (>8 mg/dL) |
Baja o intermedia |
Variable |
|
Hallazgos radiológicos |
Consolidación |
Infiltrado intersticial, hiperinsuflación |
Variable |
Tabla 3. Orientación etiológica según clínica. *Según patrón epidemiológico. Tabla original modificada de Enfoque Clínico de las Enfermedades Respiratorias del Niño, 2010
En la misma línea, debido a que no existen indicadores que establezcan irrefutablemente la causa etiológica de los distintos cuadros, se han inventado scores que orientan de acuerdo al conjunto de hallazgos, para diferenciar origen bacteriano versus viral de la neumonía, tal como se muestran a continuación:
|
Característica |
Bacteriana |
Viral |
|
Infiltrados |
||
|
Lobares, lobulares, segmentarios, subsegmentarios bien definidos |
+2 |
|
|
Parches menos bien definidos |
+1 |
|
|
Intersticiales, peri-bronquiales, pobremente definidos |
-1 |
|
|
Localización |
||
|
Lóbulo único |
+1 |
|
|
Múltiples lóbulos, bien definidos |
+1 |
|
|
Múltiples sitios, parahiliares pobremente definidos |
-1 |
|
|
Líquido en el espacio pleural |
||
|
Líquido evidente |
+2 |
|
|
Disminución mínima del espacio |
+1 |
|
|
Absceso o neumatocele |
||
|
Bien definido |
+2 |
|
|
Mal deinfido |
+1 |
|
|
Atelectasia subsegmentaria, usualmente en múltiples sitios |
-1 |
|
|
Compromiso del lóbulo medio o de los lóbulos superiores |
-1 |
Tabla 4. Score de Khamapirab para diferenciar neumonía bacteriana y viral en radiografía de tórax. Un puntaje promedio ≥+4,5 se relaciona con etiología bacteriana, y aquellos ≤1,9 con etiología viral. Tabla extraída de Neumol Pediatr 2013; 8 (2): 66-73
|
Variable |
Puntos |
|
Temperatura axilar ≥ 39°C |
3 |
|
Edad ≥ 9 meses |
2 |
|
Neutrófilos absolutos ≥ 8.000/mm3 |
2 |
|
Bandas ≥ 5% |
1 |
|
Rx según score Khamapirad |
3 a 7 |
|
Puntaje total posible |
15 |
Tabla 5. Puntaje predictor de neumonía bacteriana (PPNB). Un puntaje ≥4 se corresponde con neumonía bacteriana con una sensibilidad de 100% y una especificidad de 93,7%. Tabla extraída de Neumol Pediatr 2013; 8 (2): 66-73
Diagnóstico
El diagnóstico de neumonía es fundamentalmente clínico, con evidencias, ya sea al examen físico o en la anamnesis de una infección aguda (por ejemplo fiebre) asociada a sintomatología de dificultad respiratoria (retracciones, polipnea, aleteo nasal, etc). En este contexto el mejor productor negativo clínico de neumonía es la ausencia de taquipnea.(1,4)
La evaluación radiológica no se recomienda de rutina. Su mayor utilidad está en servir como apoyo diagnóstico, descartar complicaciones y como control de evolución radiológica.(1) La radiografía de tórax (de preferencia antero-posterior y lateral) está indicada en:(4)
- Diagnóstico clínico incierto
- Neumonía grave o complicada
- Ingreso hospitalario por neumonía
- Neumonía recurrente
- Neumonía refractaria a tratamiento
Ningún otro examen complementario se recomienda en forma rutinaria en atención primaria, en pacientes leves que serán tratados de forma ambulatoria.(1)
Las pruebas de laboratorio servirán principalmente como complemento a la clínica y a la radiología para orientar un posible agente etiológico, bajo la premisa de que ninguna puede determinarlo de forma aislada. Algunos de las más importantes son:(5)
- Recuento de glóbulos blancos: en general se acepta que recuentos totales >15.000/mm3, neutrófilos >10.000/mm3 o bandas ≥5% se correlacionan aceptablemente con etiología bacteriana.
- Proteína C reactiva (PCR): su elevación es inespecífica. Valores >8mg/dL se han asociado a etiología bacteriana, pero aún por sí sola no tiene suficiente sensibilidad ni especificidad.
- Velocidad de sedimentación globular (VHS): pobre marcador de infección aguda con baja capacidad de diferenciar etiología viral de bacteriana. Valores >100mm/h podrían asociarse más confiablemente a esta última.
- Procalcitonina: valores ≥1ng/mL se ha correlacionado con etiología bacteriana (>2ng/mL específicamente neumocócica) con una especificidad de 80%. Sin embargo, este es un test aún escasamente disponible en nuestro medio.
En cuanto al diagnóstico microbiológico, la identificación específica del patógeno está indicada en casos de enfermedad grave, pacientes que requieren hospitalización, brotes en la comunidad o sospecha de agente inusual.(4) Algunas de las técnicas disponibles son:(5)
- Hemocultivo: bajo rendimiento pues no siempre existirá bacteremia. Suele ser positivo en menos del 10% de los casos y el uso previo de antibióticos disminuye su utilidad.
- Cultivo de secreción nasofaríngea o esputo: baja sensibilidad y especificidad, pues la colonización de microorganismos en vía aérea superior no indica infección de la vía área inferior (excepto en fibrosis quística). Como requisito las muestras deberían contener <10 células epiteliales por campo y >25 PMN para ser procesadas.
- Punción pulmonar: buen rendimiento diagnóstico pero altamente riesgoso por lo que sólo se debe realizar en casos seleccionados.
- Detección de antígenos bacterianos: la detección de antígenos de S. pneumoniae en orina puede ser un buen predictor negativo (su utilidad decae en portadores y los vacunados recientes contra neumococo). Por otro lado la detección en líquido pleural tiene una alta especificidad y sensibilidad (hasta 90%).
- Detección de antígenos virales: la técnica de ELISA tiene una sensibilidad del 60-80% y especificidad >90% para el diagnóstico rápido de influenza y VRS. La inmunofluorescencia también entrega resultados rápidos y confiables, pero requiere instrumental y profesionales capacitados en su ejecución.
- Técnicas moleculares de diagnóstico rápido: las pruebas de PCR múltiplex o basadas en microchips arrays, pueden identificar múltiples patógenos simultáneamente en pocas horas, con gran sensibilidad y especificidad.
- Métodos serológicos: la detección serológica por técnica de ELISA es elemental en el diagnóstico de neumonías atípicas. En el caso de los virus requiere análisis de sueros pareados (en fase aguda y de convalecencia) aunque aún así no siempre se podrá demostrar aumento significativo de anticuerpos o seroconversión.
TRATAMIENTO
Medidas generales
Según la guía clínica MINSAL de IRA Baja de Manejo Ambulatorio en Menores de 5 años, se recomienda para todo niño cursando una NAC:(1)
- Reposo relativo
- Alimentación fraccionada a tolerancia con líquido abundante
- Aseo nasal frecuente
- Farmacológico:
- Paracetamol 15 mg/kg/dosis (max c/6 hrs) o Ibuprofeno 10 mg/kg/dosis (max c/8 hrs) en caso de dolor o fiebre >38,5ºC
- Broncodilatadores (Salbutamol 2 puff max c/4 hrs) si es que existe obstrucción bronquial.
- Kinesiterapia Respiratoria: manejo de atelectasias e hipersecreción bronquial.
- Educación a los padres respecto a evolución esperable del cuadro: mejoría del estado general y afebril tras 48-72 hrs de tratamiento.
Indicación de hospitalización
La indicación de hospitalizar a un niño cursando una neumonía deberá ser realizada considerando edad, comorbilidad, factores clínicos y sociales. Será necesario hospitalizar a un niño que cumpla cualquiera de las siguientes condiciones:(1,15)
- Todo niño menor de 3 meses: riesgo de apnea y PCR
- Aspecto tóxico: sugiere gravedad y probable etiología bacteriana
- Necesidad de oxigenoterapia (saturación <93% o signos clínicos de hipoxemia)
- Dificultad respiratoria: frecuencia respiratoria elevada (>70 rpm en <12 meses, y >50rpm en mayores), aleteo nasal, quejido, retracciones.
- Comorbilidad: síndromes genéticos, cardiopatías congénitas, trastornos metabólicos, paciente inmunocomprometido, etc.
- Rechazo alimentario con riesgo de deshidratación e incapacidad de recibir tratamiento vía oral.
- Mala respuesta a tratamiento empírico (a las 48 hrs) o mala adherencia.
- Inestabilidad hemodinámica o compromiso de conciencia.
- Falta de condiciones familiares/sociales que permitan un adecuado cumplimiento de la terapia.
- Sospecha o presencia de complicaciones (derrame pleural, empiema, absceso, etc).
Tratamiento antibiótico específico
Como se mencionó anteriormente, la neumonía tiene una gran variedad de agentes bacterianos, aunque en la mayor parte estos casos corresponderán a infecciones por S. pneumoniae.
No se recomienda indicar antibioterapia de rutina en niños menores de 5 años, ya que a esta edad la mayoría corresponderán a causa viral.(1)
En la tabla a continuación se expone la terapia de elección según edad y sospecha de agente etiológico:(1,15)
|
Ambulatorio (VO) |
Intrahospitalario (EV) |
|
|
1-6 meses |
< 3 meses: hospitalizar |
Cefotaxima 150 mg/kg/día en 3-4 dosis Ampicilina 150-200 mg/kg/día en 4 dosis |
|
C. trachomatis: Eritromicina 50 mg/kg/día en 4 dosis x 14 días |
C. trachomatis: Azitromicina 10 mg/kg/día |
|
|
>6 meses |
Primera línea: Amoxicilina 80-100 mg/kg/día cada 8-12 hrs x 7 días |
PNC Sódica 150-200.000 UI/kg/día en 4-6 dosis Ampicilina 150-200 mg/kg/día en 4 dosis Cefotaxima 150 mg/kg/día en 3-4 dosis |
|
En alergia a β-lactámicos o sospecha de germen atípico: Azitromicina 10 mg/kg/día x 5 días (max 500 mg/día) Claritromicina 15 mg/kg/día en 2 dosis x 10 días (max 1 g/día) Eritromicina 15 mg/kg/día en 4 dosis x 10 días (max 2 g/día) |
En alergia a β-lactámicos o sospecha de germen atípico: Eritromicina 20 mg/kg/día en 4 dosis Levofloxacino 16-20 mg/kg/día en 2 dosis en <5 años, y 8-10 mg/kg/día en >5 años |
Tabla 6. Tratamiento antibiótico en NAC ambulatoria e intrahospitalaria
NEUMONÍA COMPLICADA
Las complicaciones de la neumonía se presentan preferentemente en neumonías bacterianas que en aquellas causadas virus o agentes atípicos. Se deben sospechar en pacientes con aspecto grave o evolución tórpida del cuadro clínico /falat de respuesta a tratamiento posterior a 48-72 hrs). Algunas de las más importantes son:(1,4)
- Derrame pleural: se analizará en detalle más adelante.
- Neumonía necrotizante: existe necrosis y licuefacción del parénquima pulmonar. Se caracteriza por presentar cavitaciones <1cm (TAC con contraste como técnica de elección) y es usualmente acompañado por derrame pleural o empiema. Las bacterias más frecuentemente implicadas son S. pneumoniae (más común), S. aureus, y S. pyogenes.
- Absceso pulmonar: acumulación de células inflamatorias que produce una o más cavidades en el pulmón de contenido necrótico. En la radiografía se observará una cavidad de paredes gruesas con nivel hidroaéreo. Su complicación más común es la hemorragia intracavitaria. Los microorganismos más frecuentemente involucrados son anaerobios (por aspiración) y S. aureus.
- Neumatocele: corresponden a quistes de paredes delgadas y contenido aéreo en el parénquima pulmonar, se asocian frecuentemente a empiema. En la mayor parte de los casos se resolverán de forma espontánea pero también pueden derivar en neumotórax. Se asocian clásicamente con S. aureus.
- Atelectasias
- Neumotórax
- Hiponatremia
- Septicemia
 Figura 7. Absceso pulmonar en TAC (izq) y Rx de Tx (der). Imagen original de Neumol Pediatr 2013; 8 (2): 79-85
Figura 7. Absceso pulmonar en TAC (izq) y Rx de Tx (der). Imagen original de Neumol Pediatr 2013; 8 (2): 79-85
Derrame Pleural Paraneumónico
El derrame pleural es el resultado del compromiso de la pleura en los procesos inflamatorios, lo que producirá un exudado que ocupará el espacio pleural. Se presenta en alrededor del 1% de los cuadros de neumonía, pero hasta en un 40% de aquellos que requieren hospitalización.(16)
El derrame paraneumónico simple se define como un exudado pleural asociado a neumonía. Usualmente en etapas tempranas es un fluido aséptico libre en la cavidad pleural. El derrame paraneumónico loculado se refiere a la aparición de tabiques proteicos que impiden la libre circulación del líquido. El término derrame paraneumónico complicado suele referirse a los cambios debidos a la invasión bacteriana del líquido pleural previamente estéril. Finalmente se denominará empiema al hallazgo de microorganismos en la tinción gran o bien a la presencia de pus en la cavidad pleural.(17)
En correlación con las definiciones recién mencionadas, el derrame pleural evoluciona siguiendo 3 o 4 fases (dependiendo de la fuente, en ocasiones la primera no es considerada):(16)
- Precolección o pleuritis sicca: hay extensión del proceso inflamatorio hasta la pleura (con inicio de dolor y roce pleural), sin exudado.
- Exudativa o efusión simple: aumenta la permeabilidad y hay exudado de un líquido claro y estéril de baja celularidad.
- Fibrinopurulenta o efusión complicada: incrementa el número de células; glóbulos blancos, bacterias y detritus. Comienza el depósito de fibrina.
- Organizativa: hay organización de la fibrina con engrosamiento pleural y formación de adherencias que pueden comprometer la dinámica ventilatoria (patrón restrictivo).
En cuanto a los hallazgos clínicos, se debe sospechar en caso de fiebre persistente en un paciente que recibe una antibioterapia adecuada por 48 hrs. Otros síntomas comunes son compromiso de estado general, rechazo alimentario, dolor torácico y disnea.(16,17) El clásico síndrome de derrame pleural se define por los siguientes hallazgos:
|
Inspección |
Abombamiento del hemitórax, disminución de la expansión respiratoria. En empiema puede haber edema localizado de la pared. |
|
Palpación |
Disminución de la elasticidad y expansión con abolición (o marcada disminución) de las vibraciones vocales. |
|
Percusión |
Matidez intensa con curva de Damoiseau. Otros signos son el triángulo de Grocco y el ángulo de Garland. |
|
Auscultación |
Roce pleural (inicial), abolición del murmullo pulmonar, respiración soplante (o soplo pleural), egofonía y pectoriloquia áfona. |
Tabla 7. Signos de derrame pleural en el examen pulmonar. Goic A, Semiología médica 3ra edición, 2010.
El estudio del líquido pleural entregará orientación para distinguir entre derrame paraneumónico (DPN) simple, complejo y empiema:(16,17)
|
Parámetro |
DPN Simple |
DNP Complejo |
Empiema |
|
pH |
>7,2 |
<7,2 |
<7,0 |
|
Glóbulos Blancos (/μL) |
<10.000 |
>10.000 |
>10.000-50.000 |
|
Glucosa (mg/dL) |
>40 |
<40 |
<40 |
|
LDH (UI/L) |
<1000 |
>1000 |
>1000 |
|
Gram o cultivo |
– |
+ |
+ |
Tabla 8. Estudio de líquido pleural en derrame paraneumónico
También se considerará empiema la salida de líquido visiblemente purulento en la toracocentesis.
En la imagenología habrá principalmente 3 técnicas que aportarán al estudio del derrame pleural:(17)
- Radiografía de Tórax: se debe tomar anteroposterior, lateral y en decúbito lateral (aumenta sensibilidad y distingue líquido libre del loculado). Algunos de los signos que se pueden encontrar son obliteración del ángulo costofrénico y signo del menisco. Algunas de sus limitaciones es que no puede diagnosticar empiema, requiere al menos 200mL, y un velamiento completo del campo no puede ser categorizado.
- Ecografía: modalidad de elección en derrame paraneumónico grande, loculado, o que produzca velamiento completo del campo pulmonar a la radiografía. Será útil para cuantificar el volumen del líquido (hasta 5 mL), guiar toracocentesis y tiene mayor sensibilidad que la TAC para detectar loculaciones tempranas. Otras ventajas, es que no requiere sedación y no expone a radiación. Su desventaja es que corresponde a una técnica operador dependiente.
- Tomografía Axial Computarizada: no tiene capacidad de identificar la naturaleza del líquido ni la presencia de empiema, y no se recomienda su realización en forma rutinaria. Sus mayores aportes están en la caracterización del compromiso parenquimatoso (por ejemplo absceso o necrosis) y como estudio anatómico previo a cirugía.
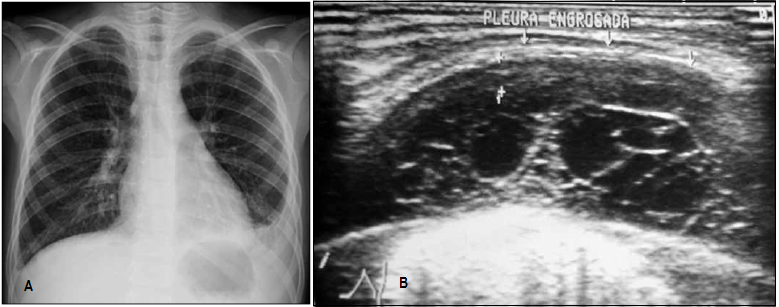
Figra 8. (B) Derrame pleural en Rx de Tx que muestra obliteración del ándulo costrofénico derecho y (B) Ecografía de Toax que muestra derrame pleural tabicado. Imágenes originales de (A) REV. MED. CLIN. CONDES – 2013; 24(1) 27-35 y (B) Neumol Pediatr 2013; 8 (2): 66-73
Manejo del derrame paraneumónico
El manejo médico consiste fundamentalmente en antibioterapia, recomendándose el uso de cefalosporina de 3ra generación (cefotaxima o ceftriaxona) asociada a vancomicina o clindamicina en empiema. Los empiemas causados por neumococo también muestran buena respuesta a penicilina. La duración de la terapia dependerá del paciente, pero en general se recomienda mantenerlo por lo menos 10 días desde la caída de la fiebre, lo cual se podría extender hasta por 4 semanas.(16,18) Éste tratamiento podría ser suficiente en derrames paraneumónicos simples y pequeños (<1cm o <¼ del hemitórax en la radiografía).
La pleurocentesis y el consecuente estudio de líquido pleural se deberá llevar a cabo en los derrames pleurales >1cm.
Respecto a la decisión de un eventual drenaje pleural será guiada principalmente por la radiología pero también por la clínica. Se recomienda realizar drenaje pleural en los siguientes casos:(18)
- Derrames pleurales grandes (>2cm en decúbito lateral u ocupación >½ del hemitorax en radiografía A-P)
- Compromiso de la función pulmonar (hipoxemia, hipercapnia, distrés respiratorio)
- Efusión loculada
- Empiema
- Efusión moderada (>1cm y <2cm en decúbito lateral u ocupación >¼ y <½ del hemitorax en radiografía A-P) asociada a ausencia de mejoría clínica.
El tubo de drenaje pleural debrá ser retirado sólo una vez que el paciente se encuentre afebril, se haya controlado el compromiso respiratorio y que el flujo de líquido sea <10mL/día.(16)
En el caso de los derrames tabicados existe la posibilidad de tratamiento con fibrinolíticos tales como la uroquinasa y estreptoquinasa, lo que podría disminuir la necesidad de cirugía y facilitaría el drenaje pleural.(18) Por último, en caso de falla en el tratamietno médico conservador o con drenaje pleural, existe la posibilidad de intervención quirúrgica, entre cuyas técnicas la VATS (Video Toracoscopía Asistida) es la que ha mostrado mejores resultados.(16)
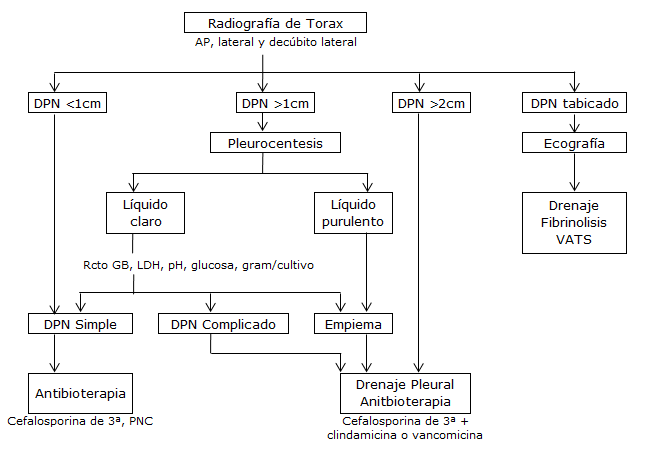
Figura 9. Algoritmo de manejo de derrame pleural paraneumónico (DPN)
Bibliografía
- Ministerio de Salud. Guía Clínica Infección Respiratoria Aguda baja de Manejo Ambulatorio en Menores de 5 años. MINSAL, 2013.
- Rudan I, Boschi-Pinto C, Biloglav Z, Mulholland K, Campbell H. Epidemiology and etiology of childhood pneumonia. Bulletin of the World Health Organization 2008;86:408–416.
- Mandell L, Wunderink R. Neumonía. En: Longo D, ed. Harrison Principios de la Medicina Interna. 18ª Edición. Editorial McGraw-Hill, 2012;2130-2141
- William J Barson, MD. Community-acquired pneumonia in children: Clinical features and diagnosis. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Oct 24, 2017)
- Libia L. Diagnóstico de neumonía adquirida en la comunidad en la población infantil. Neumol Pediatr 2013; 8 (2): 66-73
- Moenne K. Neumonías adquiridas en la comunidad en niños: Diagnóstico por imágenes. REV. MED. CLIN. CONDES – 2013; 24(1) 27-35
- Morales O, Durango H, González Y. Etiología de las neumonías adquiridas en comunidad en la población infantil. Neumol Pediatr 2013; 8 (2): 53-65
- Frederick E Barr, MD, Barney S Graham, MD, PhD. Respiratory syncytial virus infection: Clinical features and diagnosis. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Jul 28, 2017)
- Pedro A Piedra, MD, Ann R Stark, MD. Bronchiolitis in infants and children: Clinical features and diagnosis. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Oct 04, 2017)
- Phyllis Flomenberg, MD, Tsoline Kojaoghlanian, MD. Epidemiology and clinical manifestations of adenovirus infection. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Oct 24, 2017)
- Flor M Munoz, MD, MSc, Phyllis Flomenberg, MD. Diagnosis, treatment, and prevention of adenovirus infection. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Apr 15, 2016)
- Sepúlveda A, Castet A, Bertrand P. Neumonía por bacterias atípicas: Mycoplasma y Chlamydia pneumoniae ¿Qué elementos tenemos para hacer un diagnóstico adecuado y decidir cuándo tratar?. Neumol Pediatr 2015; 10 (3): 118 – 123
- Parra W. Neumonías atípicas. Neumol Pediatr 2013; 8 (2): 74-78
- Dori F Zaleznik, MD, Jesus G Vallejo, MD. Pneumonia caused by Chlamydia species in children. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Apr 12, 2017.)
- William J Barson, MD. Pneumonia in children: Inpatient treatment. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Dec 01, 2017.)
- Agudelo B. Neumonía complicada en pediatría, su manejo: un reto. Neumol Pediatr 2013; 8 (2): 79-85
- Ibrahim A Janahi, MD, Khoulood Fakhoury, MD. Epidemiology; clinical presentation; and evaluation of parapneumonic effusion and empyema in children. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Nov 03, 2017)
- Ibrahim A Janahi, MD, Khoulood Fakhoury, MD. Management and prognosis of parapneumonic effusion and empyema in children. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on Jul 06, 2017)
