1. Introducción
Definición
La falla hepática aguda (FHA) se define como el desarrollo de una injuria hepática severa manifestada inicialmente como ictericia que progresa encefalopatía dentro de las primeras 8 semanas y que además se asocia a alteración en la coagulación (INR ≥ 1.5) en un paciente sin antecedentes de cirrosis o enfermedad hepática preexistente. Para diferenciar de una falla hepática crónica, se distinguen las agudas (< 26 semanas) y las crónicas (> 26 semanas). Además, se consideran dentro del espectro de la FHA a dos situaciones clínicas: 1) en pacientes con enfermedad de Wilson, virus B adquirido verticalmente o hepatitis autoinmune no diagnosticada en quienes su cirrosis haya avanzado en < 26 semanas y 2) pacientes con hepatitis alcohólica severa que evolucionan con FHA aun cuando tengan un daño crónico previo. (1,2,3)
Epidemiología
La FHA suele afectar a individuos jóvenes y a pesar de ser infrecuente, conlleva una alta morbimortalidad. La mayoría de información epidemiológica de la FHA proviene de Estados Unidos, donde se reporta una incidencia anual de aproximadamente 2000 casos, siendo las causas más frecuentes la intoxicación por paracetamol (46%), reacciones idiosincráticas a medicamentos (11%), virus de hepatitis B (7%), autoinmune (5%) y virus de hepatitis A (3%). El 50% fueron catalogados sin una etiología identificable. Se ha descrito una mortalidad del 80% sin tratamiento, es decir, sin trasplante hepático ortotópico (THO). En Reino Unido se estima 1 – 8 casos por millón de habitantes. La sobrevivencia global a un año (incluyendo aquellos con y sin trasplante) es de un 65%. (2,3)
En Chile, no existen datos acerca de la incidencia de FHA. Sobre la etiología, históricamente era el virus de hepatitis A, sin embargo, ha ido disminuyendo por el aumento de otras patologías. Existe un estudio chileno que evaluó 168 casos entre 2001 y 2014, donde las etiologías más frecuentes fueron medicamentos (30%), autoinmune (20%), indeterminadas y otras causas (50%). (4) Además, la FHA explica el 10% de los THO en Chile. (5)
Clasificación
Existen diversas clasificaciones de FHA que datan de entre los años 1970 y 1986 como la clasificación de Trei 1970, de Bernau 1986 y Gimson 1986. (6) Sin embargo, la más relevante y que tiene valor pronóstico es la clasificación de O´Grady 1993 que se describe en la Tabla N°1: (2)
Sin embargo, es importante considerar que el factor pronóstico más relevante es la etiología de la FHA, por ejemplo cuando es hiperaguda, paradójicamente tienen mejor pronóstico, ya que en la mayoría de los casos se debe a una intoxicación por paracetamol, la cual es fácilmente pesquisable y tratable.
Etiología
Existen varias causas de la FHA, siendo algunas potencialmente tratables, otras que sólo se pueden manejar con soporte y THO y un gran número en donde no se pesquisa la etiología. La búsqueda de la etiología específica es muy relevante, ya que en hasta la mitad de los pacientes se puede realizar alguna intervención para evitar llegar al THO. En la tabla N°2 se enumeran las principales causas de FHA. (2,7) En la tabla N°3 se describe una mnenotecnia en inglés de las etiologías más frecuentes para sospechar en el Servicio de Urgencias (SU). (8) A continuación se discutirán las etiologías más frecuentes: (1-3,6,7).
1. Hepatitis virales: Se debe solicitar serología viral a todo paciente que ingrese por FHA, incluso si hay otra causa probable. Los virus de hepatitis A (VHA) y B (VHB) son los más frecuentemente asociados a FHA. En el caso de la infección por VHA, se manifiesta como FHA en el 0.35% de los casos, en cambio, en el VHB, en el 1% de los casos. Se ha descrito también la posibilidad de FHA por reactivación de VHE latente en pacientes inmunosuprimidos. La coinfección de VHB y virus de hepatitis D (VHD) se puede encontrar en hasta el 30% de los casos de FHA por VHB, por lo que también se debe solicitar. En el caso del virus de hepatitis E (VHE), debiera considerarse como principal etiología sólo en pacientes con antecedentes de viaje a Rusia, Pakistán, México o India, ya que no se han reportado casos endémicos en Chile. Otros virus como virus de hepatitis C, herpes virus y Epstein Bar son más raros, pero también deben estar dentro del diagnóstico diferencial y deben ser solicitados en todo paciente con FHA.
2. Intoxicación por paracetamol y otras drogas: La hepatotoxicidad inducida por drogas, en la mayoría de los casos es de características idiosincráticas. En particular, el caso de la intoxicación por paracetamol es ampliamente conocida, frecuente y con un tratamiento específico. Por lo anterior, cuando un paciente consulta al SU por FHA, se deben realizar todos los esfuerzos posibles en descartar esta etiología. Clínicamente se manifiesta en 4 fases: asintomática, flu-like, insuficiencia hepática (a las 72 horas) y finalmente resolución, si el paciente vive.
3. Hongos: Principalmente del tipo amanita phalloides. Se han reportado casos en Chile de FHA por esta especie. Usualmente se da en el contexto de consumo de hongos silvestres sin la instrucción adecuada. Es de mal pronóstico y su único tratamiento es el THO.
4. Hepatitis autoinmune: Para su diagnóstico es necesario medir anticuerpos y niveles de inmunoglobulina G. Si la sospecha existe y los anticuerpos son negativos, está recomendado tomar biopsia (generalmente por vía transyugular) para hacer el diagnóstico.
5. Enfermedad de Wilson: Se debe sospechar una FHA ante bilirrubina muy elevada (generalmente sobre 20 mg/d) asociado a Fosfatasas alcalinas muy bajas. La relación FA:Bilirrubina total menor de 2 es bastante sensible para hacer el diagnóstico en este escenario.
6. Hipoperfusión: Puede desencadenar isquemia hepática y FHA. Se puede sospechar por condiciones que se asocien a hipoperfusión como un cuadro séptico, insuficiencia cardiaca descompensada o drogas vasoconstrictoras hepáticas. En los exámenes de laboratorio destacan transaminasas muy elevadas entre 25 y 250 veces el valor normal.
2. Fisiopatología
La fisiopatología es diferente según la etiología de la FHA, pero en la mayoría de los casos, todas las vías de daño desencadenan una injuria caracterizada por necrosis que evolucionará posteriormente en fibrosis hepáticas. A continuación se expondrá brevemente la fisiopatología de las principales causas: (1,7,9).
1. Viral: Se explica directamente por la respuesta inmune del paciente, específicamente el sistema HLA, linfocitos T CD8+ y linfocitos Natural Killer, quienes inducen la destrucción de los hepatocitos infectados.
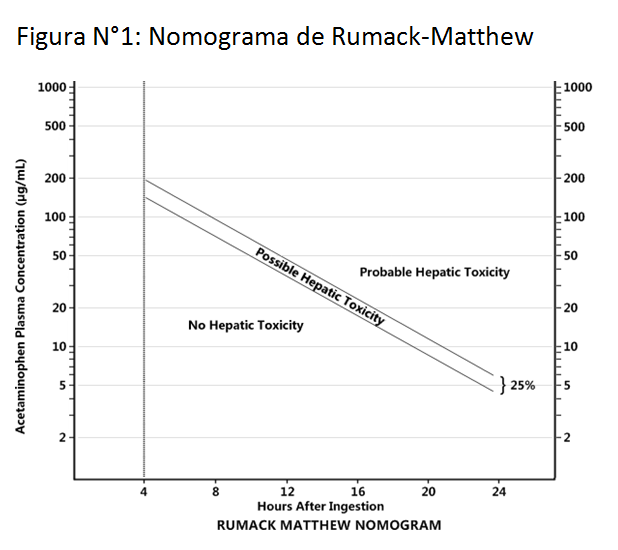
2. Paracetamol: En condiciones normales, el paracetamol es metabolizado por el hígado en un 90%. Del 10% restante, la mitad es excretada por los riñones y la otra, metabolizada por el citocromo P450 a N-acetyl-p-benzoquinoneimina (NAPQI), el cual se conjuga con glutatión para eliminarse por la orina. En el caso de una intoxicación, aumenta el porcentaje de metabolización vía citocromo P450 y, en la medida que el glutatión se agota, se acumula el metabolito tóxico (NAPQI), el cual genera el daño hepático. La dosis de riesgo descrita es entre 7.5-10 gramos de paracetamol en adultos y 150 mg/kg en niños. Para determinar la probabilidad de toxicidad por acetaminofeno se utiliza el nomograma de Rumack-Matthew, que considera el nivel plasmático y el tiempo desde la ingestión (Figura N°1).
3. Hongos: Presentan una toxina con la capacidad de inhibir la enzima RNA topoisomerasa II, lo que bloquea la transcripción genética a nivel del hepatocito.
4. Hepatitis autoinmune: La etiopatogenia de esta enfermedad no está del todo clara. La hipótesis más aceptada es un resultado de la combinación de factores ambientales, una susceptibilidad genética del huésped y alteraciones en la regulación del sistema inmunitario. Habría un agente ambiental que desencadena una cascada de hechos modulados por los linfocitos T citotóxicos dirigidos contra antígenos hepáticos en un huésped genéticamente predispuesto, dando lugar a un proceso progresivo de necroinflamación y fibrosis hepática.
3. Diagnóstico
Valoración inicial
Se debe iniciar con el ABCDE, tomando especial atención durante todo el examen en el estado neurológico del paciente:
A. Permeabilidad de vía aérea: evaluar si puede hablar, manejo de secreciones o presencia de estridor. Evaluar necesidad de intubación según nivel de vigilia.
B. Ventilación: Evaluar frecuencia respiratoria, oximetría de pulso, uso de musculatura accesoria, auscultación pulmonar.
C. Circulación: Evaluar frecuencia cardiaca, llene capilar, presión arterial y ritmo cardiaco. Recordar que las intoxicaciones son actualmente la principal causa de FHA y muchas veces son polimedicamentosas.
D. Déficit neurológico: Descripción detallada y seriada del nivel de lenguaje y conexión con el medio, movilidad de 4 extremidades, pupilas, Glasgow y velocidad de deterior.
E. Exponer: Solicitar un electrocardiograma (EKG) y hemoglucotest.
Manifestaciones clínicas
La presentación clínica de la FHA es muy variada, abarcando una importante constelación de síntomas como fatiga, malestar, letargia, anorexia, náuseas y vómitos, dolor en el cuadrante superior derecho, prurito, ictericia y ascitis. Sin embargo, la presentación más usual es como un síndrome ictérico que a las pocas semanas progresa hacia un compromiso de consciencia paulatino. (6) El diagnóstico diferencial del síndrome ictérico se divide en hiperbilirrubinemia directa e indirecta y está resumido en la tabla N°4. (10) Dentro de la anamnesis, se debe preguntar al acompañante la temporalidad de inicio de los síntomas generales, uso de alcohol, medicamentos, dosis, vías de administración, uso de drogas ilícitas, consumo de hongos silvestres, factores de riesgo de intento de suicidio, exposición ocupacional a toxinas, factores de riesgo para VHB y VHC, factores de riesgo de hipoperfusión como historia de sangrado, fiebre, insuficiencia cardiaca y antecedentes familiares de enfermedades hepáticas.
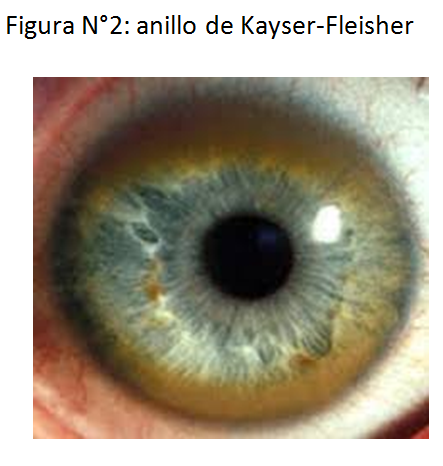
Al examen físico destacan signos inespecíficos como ictericia, mala apariencia, sopor, edema, equimosis y hematomas (coagulopatía). Más específicamente se deben buscar estigmas de daño hepático crónico (palma hepática, ascitis, dupuytren, hepatomegalia, telangectasias, etc), anillo de Kayser-Fleisher (presente en la enfermedad de Wilson) (Figura N°2), fiebre y lesiones vesiculares herpéticas y matidez hepática (signo ominoso). Se debe poner especial atención a la evaluación neurológica del paciente, ya que la encefalopatía puede progresar rápidamente, por lo que se sugiere registrar detalladamente el examen y repetirlo cada 4-6 horas. Además se deben buscar signos de hipertensión endocraneana tales como asimetría de pupilas, ausencia de reactividad de pupilas y de reflejos corneales, postura extensora, sin respuesta motora, Glasgow que se deteriora rápidamente, hipertensión sistólica, bradicardia y un patrón respiratorio anormal (Triada de Cushing). En la tabla N°5 se detalla los hallazgos al examen físico y clasificación de la encefalopatía hepática en FHA. (2) La presencia de alteraciones neurológicas facilita a diferenciar la FHA de su principal diagnóstico diferencial que es una hepatitis aguda severa, ya que esta última puede presentarse exactamente como una FHA, pero es extremadamente raro que se asocie a encefalopatía.
Pruebas diagnósticas y exámenes complementarios
Inicialmente para certificar el diagnóstico se deben solicitar:
– Tiempo de protrombina (INR): debe estar ≥ 1.5
– Glucosa, electrolitos plasmáticos, calcio, fósforo, magnesio, albúmina: Se espera encontrar hipoglicemia e hipoalbuminemia leve
– Pruebas hepáticas: se espera encontrar una hiperbilirrubinemia de predominio directo
– BUN y creatininemia
– Gases en sangre arterial
– Lactato
– Proteína C reactiva: se debe descartar sepsis, ya que este cuadro puede dar fiebre, compromiso de consciencia, síndrome ictérico e incluso disfunción hepática. La diferencia es que la instalación de los síntomas es mucho más aguda.
– Recuento hematológico automatizado
– Grupo ABO y Rh
Una vez certificada la sospecha diagnóstica, se deben solicitar exámenes complementarios con el objetivo de determinar la etiología de la FHA. Se recomienda solicitar todos los exámenes posibles, independiente de si existe alguna etiología más probable: (1)
– Serologías virales: Anti-VHA IgM, HBsAg, anti-HBc IgM, anti-VHE IgM, HSV1 (Herpes simplex) IgM VVZ (Varicela zoster)
– VIH
– Amilasa y lipasa
– Amonemia
– Anticuerpos Anti-nucleares (ANA), Anti-músculo liso (ASMA), Anti-mitocondriales (AMA) y niveles inmunoglobulinas
– Niveles de acetaminofeno
– Determinación de drogas de abuso
– Niveles de ceruloplasmina (ante la sospecha de enfermedad de Wilson)
– Doppler de eje portal y venas suprahepáticas
– Test embarazo (mujeres)
– *La biopsia hepática si bien aporta importante información etiológica (infiltrados malignos, hepatitis autoinmune, enfermedad de Wilson, hepatitis por Virus Herpes simplex o hígado graso del embarazo) y pronóstica, generalmente está contraindicada por la coagulopatía subyacente.
Criterios de ingreso
Todo paciente con sospecha de FHA debe ser evaluado en el SU hasta certificar el diagnóstico de FHA por clínica y exámenes de laboratorio. Posteriormente, invariablemente debe ser ingresado a una unidad de cuidados intensivos para el manejo de soporte y prevención de complicaciones, especialmente cuando tiene INR > 2 o estado mental alterado. Sólo aquellos pacientes con encefalopatía grado I que no progresan a grado II, puede mantenerse en una unidad más básica pero en donde se pueda realizar una observación al menos cada 2 horas. (1,2)
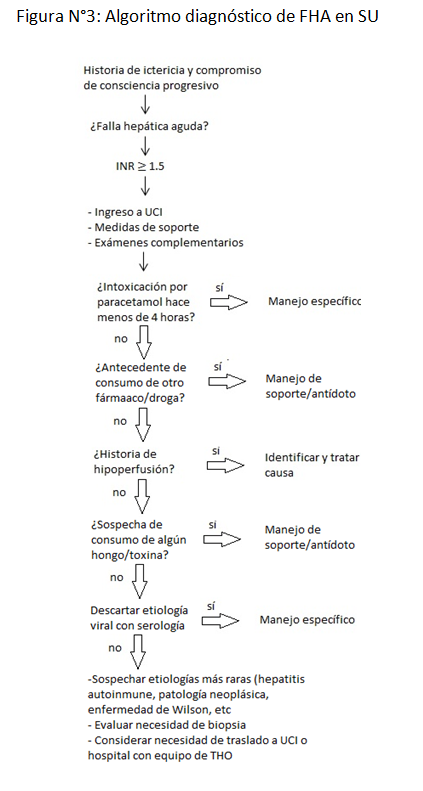
Algoritmo diagnóstico (Figura N°3)
4. Manejo
El manejo de pacientes con FHA es difícil e implica medidas de soporte, medidas específicas y esfuerzos administrativos para conseguir la evaluación por especialistas y traslado a un hospital con equipo de THO.
1. Soporte general:
a. Monitorización estricta: Medición de signos vitales horaria, diuresis, línea arterial y eventualmente medición de presión venosa central. Todas estas medidas son para pesquisar precozmente la falla orgánica múltiple (FOM) y preservar la vitalidad del medio interno hasta el THO.
b. Manejo de complicaciones: (1,2)
i. Metabólico: Por el alto riesgo de hipoglicemia, se debe administrar un aporte continuo de glucosa endovenoso con hemoglucotest seriado. Además, este cuadro se asocia a hipokalemia e hipofosfemia, las que deben ser cuidadosamente manejadas, ya que muchos de estos pacientes presentan falla renal asociada, que pudiera complicar las terapias de reposición hidroelectrolítica.
ii. Compromiso neurológico: La encefalopatía por FHA se asocia frecuentemente a edema cerebral. Se deben indicar medidas generales como elevación de cabecera 30°, favorecer sedación con propofol y control de fiebre. El monitoreo de la presión intracraneana (PIC) tiene indicación en pacientes con encefalopatía grado III o IV, particularmente en aquellos en ventilación mecánica o que estén en la espera de THO. Los objetivos deben ser tener una PIC < 20 mm Hg y una presión de perfusión cerebral (PPC) entre 60-80 mm Hg. En caso de pacientes con PPC < 40 mm Hg sostenida por más de 2 horas o PIC > 40, está contraindicado el THO por el importante daño neuronal persistente. En cuanto a las medidas específicas para el manejo de la hipertensión intra craneana se incluyen las siguientes: manitol, suero hipertónico, hiperventilación, hemofiltración, hipotermia, tiopental y fenitoína. No se conoce con certeza el mecanismo de acción de cada una y los estudios que hay al respecto son pequeños y escasos. Los únicos que pudieran tener mayor literatura a favor son el uso de manitol y de hipotermia.
iii. Infección: La sepsis está presente en hasta el 80% de las FHA, debido a la función inmunitaria alterada y a la alta instrumentalización de estos pacientes (sondas, catéteres, punciones). Se debe mantener un alto índice de sospecha y tener un muy bajo umbral para tomar cultivos. La etiología más frecuente son las cocáceas gram (+) y los sitios de infección son l tracto respiratorio, tracto urinario y sanguíneo. (11) De hecho, algunas guías recomiendan solicitar hemocultivos, urocultivo y cultivo de expectoración a todo paciente con FHA al ingreso, a pesar de que esta recomendación no tiene evidencia sólida. (1) En cuanto al uso de antibioterapia profiláctica, un estudio de 2014 demostró que no existía beneficio en su uso ni en mortalidad ni en reducción de infecciones, por lo que actualmente no se recomienda de rutina. (12)
iv. Coagulopatía: Antes de cualquier procedimiento, se debe corregir la coagulopatía con vitamina K, plasma fresco congelado (PFC) o crioprecipitados. Además, se deben transfundir plaquetas en caso de tener valores < 50.000 plq/uL si está en el contexto de un sangrado activo. Se puede realizar una aproximación más certera al estado de coagulación del paciente pidiendo niveles de fibrinógeno y un fibroelastograma. Sin embargo, si el paciente no requiere procedimientos ni tiene un sangrado activo, se ha demostrado que el uso de PFC profiláctico podría incluso ser dañino. (13) Adicionalmente se deben agregar inhibidores de la bomba de protones como profilaxis de hemorragia digestiva alta.
v. Insuficiencia renal: Está presente en hasta un 30% de los pacientes con encefalopatía grado IV. En su fase inicial es prerrenal secundario a hipoperfusión, por lo que se debe aportar, junto con la glucosa, cristaloides para asegurar una PAM > 75 mm Hg. En etapas posteriores se desarrolla necrosis tubular aguda o un síndrome hepatorrenal que es una indicación absoluta de THO. Constantemente se deben solicitar exámenes de función renal para evaluar posibles urgencias dialíticas. (3)
vi. Cardiorrespiratorio: Al igual que en el SIRS por otras causas, la repercusión cardiorrespiratoria en FHA puede ser importante y requerir uso de agentes cristaloides, vasoactivos e intubación. Se explica principalmente por disminución de la resistencia vascular periférica. Al igual que en el shock séptico, se ha estudiado el uso de corticoides en aquellos pacientes que no responden a las medidas iniciales con resultados muy controversiales. (14-16)
vii. Nutrición: Es un componente fundamental en el manejo de las complicaciones en la FHA, debido a que una adecuada nutrición previene de un estado de hipercatabolismo y disminuye el riesgo de sangrado. La recomendación actual es iniciar un régimen de 40-60 gramos de proteínas diarias. La vía de administración suele ser un tema de controversia en estos pacientes, dado por el compromiso de consciencia asociado al cuadro. La sonda nasogástrica puede aumentar la PIC, por lo que sólo debe ser indicada en pacientes sedados e intubados. Si la vía enteral no es una opción válida, se debe iniciar nutrición parenteral total. (2, 17)
2. Terapia específica:
a. Intoxicación por paracetamol: Se pueden utilizar dos agentes: el carbón activado y la N-acetil-cisteína: (1-3)
i. Carbón activado: Su principal fin es evitar su absorción. Primera dosis (1g/kg, máximo 100 gramos) debe ser en los primeros 60 minutos. Siempre pasar con vía aérea protegida.
ii. N-acetil-cisteína:
1. Es el antídoto: Ayuda a metabolizar el paracetamol por la vía del glutatión.
2. Se indica cuando existe el claro antecedente de consumo de paracetamol, niveles sanguíneos elevados o elevación de transaminasas.
3. La dosis de carga es de 140 mg/kg vía oral/SNG. Luego, 70mg/kg cada 4 horas por 17 veces.
a. Si se conoce el tiempo de ingesta: Desde las 4 horas se toman niveles de paracetamol para saber si requiere tratamiento con N-acetil-cisteína según normograma Rumack Matthew (medir niveles entre 4 a 24 hr). Si está arriba de la línea, dar tratamiento completo (al menos 3 días hospitalizado), si está abajo, se puede dar de alta. Si se inicia tratamiento con <8 horas de ingesta ha demostrado mejoría en la sobrevida. No hay diferencia al iniciarlo a las 4 u 8 horas.
4. Si no se conoce el tiempo de ingesta el uso del antídoto depende de los niveles de paracetamol: sobre 10 ng/mL se trata. También se inicia tratamiento con pruebas hepáticas alteradas (GOT alterada) o con síntomas de insuficiencia hepática.
b. Viral: Sólo algunas etiologías tienen manejo específico, aunque hay que considerar que la gran mayoría, independiente del virus en particular, requerirán THO. En el caso del VHB se pueden indicar antivirales con análogos de nucleótidos (lamivudina, entecvir), sin embargo, los estudios no han demostrado claramente prevenir la necesidad de THO con esta terapia. La terapia debe indicarse de todas maneras para disminuir el riesgo de enfermedad post trasplante. (18) En el caso del VHA, no existe terapia específica, por lo que sólo se deben iniciar las terapias de soporte y evaluar la necesidad de THO. (1) Finalmente si se sospecha que la etiología es el Herpes virus, se puede indicar aciclovir 15-30 mg/kg/día endovenoso por 7 días o hasta excluirla.
c. Intoxicación por hongos: Se describe el uso de carbón activado como beneficioso. Además como antídotos se han estudiado la silimarina y la penicilina G en dosis de 300.000 a 1.000.000 UI/kg/día, aunque los resultados no son concluyentes. (19-21)
d. Hepatitis autoinmune: Se ha propuesto el uso de prednisona 60 mg al día vía oral, pero la evidencia actual no es clara y se ha resaltado el riesgo de utilizar corticoides por el aumento del riesgo de complicación infecciosa. (22,23)
e. Enfermedad de Wilson: La terapia es el THO, aunque terapias que busquen remover rápidamente el contenido de cobre corporal se han evaluado, tales como hemodiálisis, peritoneo diálisis y hemofiltración. El recambio de plasma con PFC puede ser una terapia útil para ganar tiempo. (24)
f. Hepatitis isquémica: Se debe iniciar soporte cardiovascular. Se debe considerar también que algunas drogas pueden causar este cuadro como la cocaína o las metanfetaminas.
g. Síndrome de Budd-Chiari: Se han estudiado la derivación portosistémica intrahepática (TIPS), descompresión quirúrgica o trombolisis, pero las guías sólo recomiendan el THO como la única terapia válida en este caso.
h. Etiología indeterminada: En general, en los estudios se ha visto que son 3 las causas más probables en este contexto: intoxicación por paracetamol, hepatitis autoinmune o malignidad. Una opción es realizar una biopsia hepática transyugular. (25)
Trasplante hepático ortotópico
El THO es la única terapia que ha cambiado radicalmente el pronóstico de la FHA, logrando una sobrevida de hasta un 70% a dos años. El mejor momento del trasplante, en cambio, aún no se ha podido dilucidar bien dado a que los estudios no han podido validar un score predictor de mortalidad para este escenario. Sin embargo, actualmente se utilizan los criterios del King’s College (Tabla N°6) (26,27) En Chile, el primer trasplante se realizó el año 1985. Desde allí, la tasa de trasplantes anuales ha ido incrementando hasta llegar a ser de 10 trasplantes por millón de habitantes, aunque sigue siendo sólo la tercera parte de otros países de Europa. Hasta la fecha, durante el 2016 se han llevado a cabo 139 trasplantes en total, siendo 38 de ellos THO. (28)
Dentro de las principales indicaciones para el trasplante se encuentran la cirrosis hepática colestásica y no colestásica, enfermedades metabólicas, tumores hepáticas y la FHA, que explica un 10% de todos los THO. Son contraindicaciones para el procedimiento la presencia de FOM, infección no controlada, daño cerebral no reversible (PIC elevada sostenida) y neoplasia extrahepática. (27)
Finalmente, se han descrito una serie de terapias de sustitución hepáticas, dentro de los cuales se pueden nombrar al sistema de recirculación absorbente molecular (MARS) o el dispositivo de asistencia hepática extracorpórea, pero no han mostrado ningún beneficio, por lo que las guías no los recomiendan actualmente. (1,29)
5. Conclusiones
La FHA es una patología poco frecuente pero dada su alta morbi mortalidad, debe ser sospechada y manejada exitosamente desde el SU. La sospecha diagnóstica radica en una historia clínica de ictericia que progresa a alteración del estado mental en < de 8 semanas y que se acompaña de múltiples síntomas inespecíficos como letargia, fatiga, anorexia, náuseas y dolor en el cuadrante superior derecho. Además, en la anamnesis de deben consignar todos los antecedentes médicos del paciente, tomando especial atención en los fármacos, drogas, consumos recientes de hongos y factores de riesgo para intentos suicidas. La exploración física en general entrega poca información con respecto a la etiología de la FHA, sin embargo, es vital realizar una adecuada valoración primaria, pues la FHA puede progresar rápidamente a FOM.
Para certificar la sospecha diagnóstica se debe pedir un tiempo de protrombina (INR) el que debe ser ≥ a 1.5. Además de este examen se deben pedir otros exámenes generales para evaluar la funcionalidad de otros sistemas y rápidamente conseguir muestras para iniciar el estudio etiológico.
Las medidas de soporte y el manejo de complicaciones (metabólicas, neurológicas, infecciosas, coagulopatía, renales, cardiorrespiratorias y nutricionales) son uno de los pilares del manejo de la FHA que, si bien no han demostrado mejorar la sobrevida general o disminuir la necesidad de THO, dan una ventana de tiempo para conseguir un equipo de THO y la aparición de un potencial donante.
Referencias
(1) William M. Lee Anne M. Larson R. Todd Stravitz. AASLD Position Paper: The Management of Acute Liver Failure: Update 2011. 2011 The American Association for the Study of Liver Diseases. Disponible en http://www.aasld.org/publications/practice-guidelines-0
(2) Dr. Juan Carlos Weitz V. Dr. Zoltán Berger F. Dr. Samuel Sabah T. Dr. Hugo Silva C. Diagnóstico y tratamiento de las enfermedades digestivas. Sociedad Chilena de Gastroenterología, 2013, editorial iku, pág 377 – 389.
(3) Bernstein D, Tripodi J. Fulminant hepatic failure. Crit Care Clin. 1998 Apr;14(2):181-97.
(4) Zapata R, Sanhueza E, Gómez F, Contreras J, Uribe M, Humeres M, Rius M, Basaez AM, Ríos H, Delgado I, Hepp J. TLP3 – Utilidad clínica de índices pronósticos de mortalidad en 168 pacientes adultos consecutivos con insuficiencia hepática aguda en Chile (2001-2004). Gastroenterología Latinoamericana 2014;24;S116.
(5) Hepp J, Zapata R, Buckel E, Martínez J, Uribe M, Díaz JC, Ferrario M, Sanhueza E, Pérez RM, Hunter B, Ríos G, Humeres R, Poniachik J, Oksenberg D,Arrese M. General considerations, indications and contraindications for liver transplantation in Chile: a multicenter consensus development document. Rev Med Chil. 2008 Jun;136(6):793-804.
(6) Poniachik T, Jaime, Quera P, Rodrigo, & Lui G, Andrea. (2002). Insuficiencia hepática fulminante. Revista médica de Chile, 130(6), 191-198. Disponible en: http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0034-98872002000600014
(7) Dr. Arnoldo Riquelme, Dr. Marco Arrese, Dr. Alberto Espino, Dra. Danisa Ivanovic-Zuvic, Dr. Gonzalo Latorre. Manual de Gastroenterología Clínica. Segunda edición, 2015, pág 329-337.
(8) Eric Goldberg, MD, Sanjiv Chopra, MD, MACP. Acute liver failure in adults: Etiology, clinical manifestations, and diagnosis. In: UpToDate, Topic 3574 Version 24.0, accedido el 12 de septiembre de 2016.
(9) Manns MP, Czaja AJ, Gorham JD, Krawitt EL, Mieli-Vergani G, Vergani D, Vierling JM; American Association for the Study of Liver Diseases. Diagnosis and management of autoimmune hepatitis. Hepatology. 2010 Jun;51(6):2193-213.
(10) A. Naranjo Rodríguez, L. Jiménez Murillo, A Agustín Varas, C. Reyes Aguilar y F.J Montero Pérez. Ictericia, Urgencias del Aparato digestivo, sección 5, capítulo 53, pág 339-342.
(11) Mas A, Rodés J. Fulminant hepatic failure. Lancet. 1997;349(9058):1081.
(12) Karvellas CJ, Cavazos J, Battenhouse H, Durkalski V, Balko J, Sanders C, Lee WM, US Acute Liver Failure Study Group. Effects of antimicrobial prophylaxis and blood stream infections in patients with acute liver failure: a retrospective cohort study. Clin Gastroenterol Hepatol. 2014;12(11):1942.
(13) Gazzard BG, Henderson JM, Williams R. Early changes in coagulation following a paracetamol overdose and a controlled trial of fresh frozen plasma therapy. Gut. 1975 Aug;16(8):617-20.
(14) Harry R, Auzinger G, Wendon J. The effects of supraphysiological doses of corticosteroids in hypotensive liver failure. Liver Int. 2003 Apr;23(2):71-7.
(15) Harry R, Auzinger G, Wendon J. The clinical importance of adrenal insufficiency in acute hepatic dysfunction. Hepatology. 2002 Aug;36(2):395-402.
(16) Karkhanis J, Verna EC, Chang MS, Stravitz RT, Schilsky M, Lee WM, Brown RS Jr, Acute Liver Failure Study Group. Steroid use in acute liver failure. Hepatology. 2014 Feb;59(2):612-21. Epub 2013 Dec 24.
(17) Raff T, Germann G, Hartmann B. The value of early enteral nutrition in the prophylaxis of stress ulceration in the severely burned patient. Burns. 1997;23(4):313.
(18) Dao DY, Seremba E, Ajmera V, Sanders C, Hynan LS, Lee WM, Acute Liver Failure Study Group. Use of nucleoside (tide) analogues in patients with hepatitis B-related acute liver failure. Dig Dis Sci. 2012 May;57(5):1349-57. Epub 2011 Dec 25.
(19) Moroni F, Fantozzi R, Masini E, Mannaioni PF. A trend in therapy of Amanita phalloides poisoning. Arch Toxicol 1976;36:111-115.
(20) Hruby K, Csomos G, Fuhrmann M, Thaler H. Chemotherapy of Amanita phalloides poisoning with intravenous silibinin. Human Toxicology 1983;2:183-195.
(21) Enjalbert F, Rapior S, Nouguier-Soule J, Guillon S, Amouroux N, Cabot C. Treatment of amatoxin poisoning: 20-year retrospective analysis. J Toxicol Clin Toxicol 2002:40:715-757.
(22) European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Autoimmune hepatitis. J Hepatol. 2015;63(4):971.
(23) Yeoman AD, Westbrook RH, Zen Y, Bernal W, Al-Chalabi T, Wendon JA, O’Grady JG, Heneghan MA. Prognosis of acute severe autoimmune hepatitis (AS-AIH): the role of corticosteroids in modifying outcome. J Hepatol. 2014;61(4):876.
(24) Kiss JE, Berman D, Van Thiel D. Effective removal of copper by plasma exchange in fulminant Wilson’s disease. Transfusion. 1998;38(4):327.
(25) Khandelwal N, James LP, Sanders C, Larson AM, Lee WM and the Acute Liver Failure Study Group. Unrecognized acetaminophen toxicity as a cause of indeterminate acute liver failure. Hepatology, 2011; 53:567-76.
(26) OGrady JG, Alexander GJM, Hallyar KM, et a1 Early indicators of prognosis in fulminant hepatic failure. Gastroenterology 1997, 439-445, 1989.
(27) Hepp J, Zapata R, Buckel E, Martínez J, Uribe M, Díaz JC, Ferrario M, Sanhueza E, Pérez RM, Hunter B, Ríos G, Humeres R, Poniachik J, Oksenberg D,Arrese M. General considerations, indications and contraindications for liver transplantation in Chile: a multicenter consensus development document. Rev Med Chil. 2008 Jun;136(6):793-804
(28) Corporación Chilena de Trasplante. Estadística trasplante hepático. http://www.trasplante.cl/estadisticas/31-historica/388-estadisticas-1er-semestre-trasplante-y-lista-de-espera
(29) Watanabe FD, Demetriou AA: Nonsurgical management of fulminant hepatic failure. Current Opin Gastroenterol 12231-236, 1996
Anexos
Tabla N°1: Clasificación de O´Grady para FHA:
|
|
Hiperaguda |
Aguda |
Subaguda |
Duración (días) |
< 7 |
7 – 21 |
21 días – 26 semanas |
Pronóstico |
Moderado |
Malo |
Malo |
Encefalopatía |
Sí |
Sí |
Sí |
Tiempo entre ictericia – encefalopatía (sem) |
≤ 1 |
> 1 y ≤ 4 |
> 4 y ≤ 12 |
Edema cerebral |
Frecuente |
Frecuente |
Infrecuente |
Falla renal e hipertensión portal |
Infrecuente |
Infrecuente |
Frecuente |
Tiempo de protrombina |
Prolongado |
Prolongado |
Menos Prolongado |
Bilirrubina |
Menos Elevada |
Elevada |
Elevada |
Tabla N°2: Causas más frecuentes de FHA:
| Categoría | Causa |
| Hepatitis viral | Virus de hepatitis A, B, C, D, E, Herpes Simplex, Epstein Barr, Citomegalovirus, Herpesvirus 6, Influenza tipo B, Virus de fiebres hemorrágicas (Ebola, Lassa, Marburg) |
| Drogas |
Paracetamol (accidental o intento suicida) Antibióticos (isoniazida, nitrofurantoína, tetraciclina, ciprofloxacino, eritromicina, amoxicilina-ácido clavulánico), Ácido valproico, Lovastatina, Fenitoína, Tricíclicos, Halotano, Oro, Flutamida, Antabuz, Ciclofosfamida, Extasis, Loratadina, Propiltiouracilo, Diclofenaco, Amiodarona, etc. |
| Toxinas |
Amanita phalloides, Solventes orgánicos, Hierbas medicinales (ginseng, valeriana, etc.), Toxinas bacterianas (Bacillus cereus, cianobacterias) |
|
Misceláneas
|
Hígado graso agudo del embarazo, síndrome HELLP Hepatitis autoinmune Budd-Chiari, Trombosis portal, Insuficiencia cardíaca derecha, Isquemia Leucemia, Linfoma, Metástasis Malaria, Tuberculosis Síndrome de Reye, Enfermedad de Wilson |
| Indeterminadas o criptogénicas | |
Tabla N°3: Mnemotecnia sobre las etiologías más frecuentes de FHA
| Letra | Causa |
| A | Acetaminophen, hepatitis A, autoimmune hepatitis, Amanita phalloides (mushroom poisoning), adenovirus |
| B | Hepatitis B, Budd-Chiari syndrome |
| C | Cryptogenic, hepatitis C, CMV |
| D | Hepatitis D, drugs and toxins |
| E | Hepatitis E, EBV |
| F | Fatty infiltration – acute fatty liver of pregnancy, Reye’s syndrome |
| G | Genetic – Wilson disease |
| H | Hypoperfusion (ischemic hepatitis, SOS, sepsis), HELLP syndrome, HSV, heat stroke, hepatectomy, hemophagocytic lymphohistiocytosis |
| I | Infiltration by tumor |
Tabla N°4: Diagnóstico diferencial de síndrome ictérico en el adulto
| Predominio indirecto | Predominio directo | Otras causas de pigmentación amarillenta de la piel |
|
Aumento de la producción: – Hemólisis – Resorción de un gran hematoma – Eritropoyesis ineficaz – Ayuno prolongado |
Alteración de la excreción hepática: – Hepatitis aguda o crónica – Cirrosis hepática – Enfermedades hereditarias (síndrome de Rotor y de Dubin-Johnson) – Fármacos: Anticonceptivos, testosterona |
– Ingesta abundante de alimentos ricos en carotenos (zanahoria, tomates, naranjas) – Insuficiencia renal – Exposición a dinitrofenol o ácido pícrico – Anemia |
|
Disminución de captación: – Sepsis – Insuficiencia cardiaca – Fármacos: Rifampicina, probenecid |
Alteración de excreción biliar: – Colestasia intrahepática: Cirrosis biliar primaria, colangitis esclerosante, colestasia del embarazo, medicamentoso, enfermedad de Caroli – Colestasia extrahepática: Litiasis, tumores, estenosis |
|
|
Disminución de la conjugación: – Sepsis – Enfermedad hepatocelular grave – Enfermedades hereditarias (Gilbert, Criger-Najjar – Fármacos: Cloranfenicol |
Tabla N°5: Clasificación de encefalopatía en FHA
| Grado | Síntomas | Asterixis | EEG | Sobrevida |
| I | Bradipsíquico | Leve | Normal | 70% |
| II |
Conducta inapropiada (confusión, euforia) o somnolencia. Mantiene control de esfínteres |
Presente, fácil de obtener |
Anormal: lentitud generalizada |
60% |
| III |
Somnolencia permanente, lenguaje incoherente |
Presente si el paciente coopera |
Siempre alterado | 40% |
| IV | Coma | Ausente | Siempre alterado | 20% |
Tabla N°6: Criterios King’s College
| FHA inducida por paracetamol | Otras causas de FHA |
| pH arterial < 7.3 o | Tiempo de protrombina > 100 segundos o |
|
– Encefalopatía grado III o IV más – Tiempo de protrombina > 100 segundos más – Creatininemia > 3.4 mg/dL |
Al menos 3 de los siguientes: – Edad < 10 años o > 40 años – Etiología no VHA, VHB, inducida por halotano o por reacciones idiosincráticas a drogas – Duración de ictericia previo a encefalopatía > 7 días – Tiempo de protrombina > 50 segundos – Bilirrubinemia > 17,6 mg/dL |