CÁNCER PULMONAR
Epidemiologia e importancia
A nivel mundial el cáncer pulmonar constituye un problema importante. En 2012 hubo aproximadamente 1,8 millones de pacientes y causó un estimado de 1,6 millones de muertes.
El año 2004 murieron en Chile 2.222 personas, lo que constituye una tasa de mortalidad de 13.8 por 100.000 habitantes, siendo el 2.6% de las causas de mortalidad general. Estas cifras cambian de acuerdo al segmento etario analizado. Efectivamente, entre los 45 y 64 años murieron en el año analizado, 645 personas, lo que da una tasa de 22.9 por 100.000 habitantes y fue el 6% de las causas de mortalidad general; mientras que en el segmento entre 65 y 79 años murieron 1.098 personas con una tasa de 108.7 por 100.000 habitantes, lo que constituye el 8% entre las causas de mortalidad en ese grupo.
Etiología
En el 90% de los casos de cáncer pulmonar es debido al hábito tabáquico y hay una clara relación entre la intensidad del hábito y el riesgo de desarrollarlo. El riesgo de desarrollar cáncer de pulmón para un fumador actual de un paquete por día durante 40 años es aproximadamente 20 veces el de alguien que nunca ha fumado.
Aproximadamente el 20% de los grandes fumadores desarrollan cáncer broncogénico durante su vida.
Los fumadores pasivos tienen un riesgo aumentado de desarrollar la enfermedad en 1.2 a 1.5 veces con respecto a los no fumadores
Según la Encuesta Nacional de Salud de Chile (2009) se reporta una prevalencia de tabaquismo de 40.6%. Un 30% de las mujeres de 13-15 años fuman.
En las personas que dejan de fumar, el riesgo de desarrollar cáncer de pulmón cae en comparación con los que siguen fumando, siendo mayor el beneficio en aquellos que se detienen a los 30 años.
Otros factores de riesgo asociado son:
- La radioterapia: puede aumentar el riesgo de un segundo cáncer pulmonar primario en pacientes que han sido tratados para otras neoplasias malignas.
- Los factores ambientales se han asociado con un mayor riesgo de desarrollar cáncer de pulmón. Entre estos destacan exposición laboral a asbesto y arsénico (9-15%), radón responsable de la contaminación intradomiciliaria (10%) metales (arsénico, cromo y níquel), radiaciones ionizantes e hidrocarburos aromáticos policíclicos
- Fibrosis pulmonar – Varios estudios han demostrado que el riesgo de cáncer de pulmón se incrementa siete veces en pacientes con fibrosis pulmonar. Este aumento del riesgo parece ser independiente del tabaquismo.
- Infección por VIH: La incidencia de cáncer de pulmón entre los individuos infectados con el VIH aumenta en comparación con la observada en los controles no infectados.
- Factores dietéticos: La evidencia epidemiológica ha sugerido que varios factores dietéticos (antioxidantes, vegetales crucíferos, fitoestrógenos) pueden reducir el riesgo de cáncer de pulmón, pero el papel de estos factores no está bien establecido.
¿Screening para cáncer pulmonar?
El diagnóstico de cáncer de pulmón se basa principalmente en la evaluación de individuos con síntomas. La recomendación actual de la Sociedad Americana contra el Cáncer es la pesquisa precoz mediante TAC de tórax en aquellos pacientes sobre 55 años y con antecedente de tabaquismo importante (sobre 30 paquete/año).
Clasificación Histopatológica
Los cánceres pulmonares se dividen en dos tipos, con importancia en el pronóstico y el tratamiento a recibir:
- 1) Cáncer de células no pequeñas (75-90%): se origina de las células epiteliales de bronquios centrales hasta los alveolos terminales. Se pueden clasificar en 3 variedades:
- a) Carcinoma escamoso (35%)
- b) Adenocarcinoma (40%)
- c) Carcinoma de células grandes (10%)
- 2) Cáncer de células pequeñas (15-10%): Se origina de células endocrinas que están distribuidas en pequeña cantidad en el epitelio de la vía respiratoria Tienen la capacidad de secretar hormonas y presentar síndromes paraneoplasicos. Se presenta en la zona central del pulmón y con compromiso ganglionar mediastínico extenso. Generalmente se encuentra diseminado al diagnóstico en la gran mayoría de los casos. Se caracterizan por ser sensibles a la quimioterapia y radioterapia.
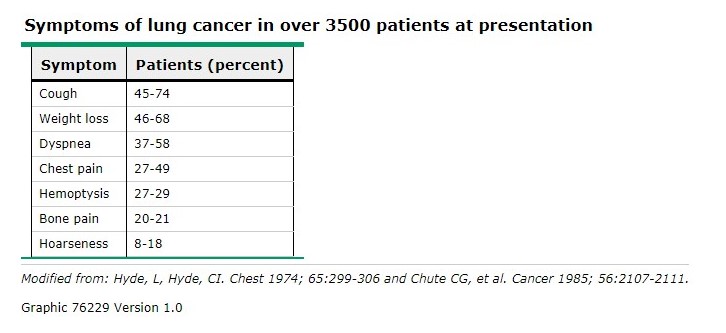
Manifestaciones clínicas
La mayoría de los pacientes con cáncer de pulmón tienen enfermedad avanzada en la presentación clínica.
Las manifestaciones clínicas se pueden agrupar de la siguiente forma:
- 1) Asintomático: Hasta en un 10% de los casos de cáncer broncogénico pueden presentarse como un hallazgo casual en un paciente asintomático
- 2) Intrapulmonares (generalmente por invasión de la vía aérea):
- Tos: La tos está presente en el 50 al 75 % de los pacientes con cáncer de pulmón al diagnóstico, siendo el síntoma más frecuente. Se produce más frecuentemente en pacientes con carcinomas de células escamosas y de células pequeñas debido a su tendencia a involucrar las vías aéreas centrales. El debut de la tos en un fumador o cambio en su patrón fumador debe hacer sospechar en cáncer pulmonar.
- Hemoptisis: La hemoptisis es reportada por 20 a 50% de los pacientes que son diagnosticados con cáncer de pulmón. Generalmente es leve-moderada. En un paciente con hemoptisis, la probabilidad de cáncer de pulmón varía de 3 a 34% en diferentes series dependiendo de la edad del paciente y el hábito tabáquico.
- Dolor torácico: El dolor torácico está presente en aproximadamente el 20 al 40% de los pacientes que presentan cáncer de pulmón. El dolor suele estar presente en el mismo hemitorax que el tumor primario. El dolor sordo, dolorido y persistente puede ocurrir por extensión mediastínica, pleural o de la pared torácica. Aunque el dolor pleurítico puede ser el resultado de una afección pleural directa, la neumonitis obstructiva o un émbolo pulmonar relacionado con un estado hipercoagulable también puede causar dolor torácico.
- Disnea: Se producen en aproximadamente 25 a 40% de los casos. Puede tener las siguientes causas: Compromiso de vía aérea principal extrínseca o intraluminal, Atelectasia, Linfangitis carcinomatosa, Embolia tumoral, Neumotórax, Derrame pericardico, Derrame pleural masivo.
- Neumonía a repetición: secundaria a la obstrucción parcial del bronquio afectado. Debido a esa razón, un paciente fumador cursando con una neumonía, debe ser dado de alta con la confirmación por imagenologica de ausencia de cáncer broncogénico.
- 3) Intratoracicas extrapulmonares:
- Invasión pleural y derrame pleural: La afectación pleural puede manifestarse como engrosamiento pleural sin derrame pleural o como derrame pleural maligno. Los pacientes con derrame pleural maligno subyacente a un cáncer pulmonar se consideran incurables y se manejan de forma paliativa.
Los derrames malignos son típicamente exudados y pueden ser serosos, serosanguinolentos o derechamente hemáticos. Sin embargo, no todos los derrames pleurales en un paciente con cáncer pulmonar son malignos, Un derrame pleural benigno puede ocurrir en un paciente con un cáncer de pulmón resecable debido a obstrucción linfática, neumonitis post-obstructiva o atelectasia. - Síndrome de vena cava superior: Los hallazgos físicos incluyen venas dilatadas del cuello, un patrón venoso prominente en el tórax, edema facial y una apariencia pletórica. La tomografía computarizada (TC) a menudo puede identificar la causa, el nivel de obstrucción y la extensión del drenaje venoso colateral.
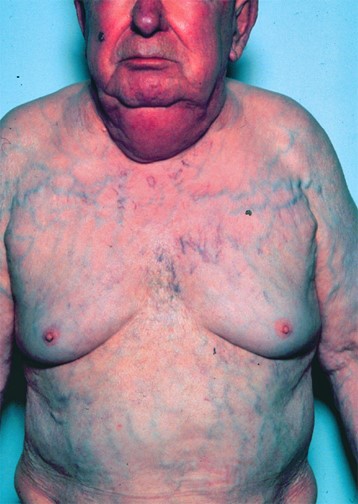 Un patrón venoso prominente en el pecho y edema facial en paciente con síndrome de VCS
Un patrón venoso prominente en el pecho y edema facial en paciente con síndrome de VCS
- Compromiso del nervio laríngeo recurrente: manifestado por ronquera
- Parálisis frénica: invasión mediastinica del nervio frénico. Los pacientes pueden ser asintomáticos o referir disnea. En una serie, el cáncer de pulmón fue la neoplasia más común que afectó el nervio frénico, aunque la malignidad representó sólo el 4 % de los pacientes con parálisis diafragmática.
- Disfagia: compresión esofágica por ganglios linfáticos mediastínicos infiltrados.
- Taponamiento cardiaco: invasión del saco pericardico.
- Síndrome de Claude-Bernard-Horner: miosis, ptosis, enoftalmo y anhidrosis. Se produce por tumor del ápice del lóbulo superior que compromete ganglio simpático cervical ipsilateral.
- Tumor de Pancoast: tumor del ápice del lóbulo superior que compromete el plexo braquial. Produce dolor neuropático de hombro con irradiación hacia el brazo.
- 4) Extratorácicas metastásicas: Hasta el 40% de los casos puede presentar metástasis al diagnóstico. Los sitios más frecuentes son:
- Cerebro: Aproximadamente el 20-30% de los pacientes con cáncer pulmonar de células no pequeñas tienen metástasis cerebrales al diagnóstico. Sospechar ante la presencia de cefalea, déficit del campo visual, alteración de los pares craneanos, convulsiones, vómitos, hemiparesia, accidentes vasculares encefálicos.
- Hueso: La metástasis del cáncer de pulmón al hueso es frecuentemente sintomática. El dolor óseo, fracturas en hueso patológico y los niveles elevados de fosfatasa alcalina sérica suelen estar presentes en pacientes con metástasis ósea. La hipercalcemia puede estar presente en contexto de una enfermedad ósea extensa. Aproximadamente el 20% de los pacientes con cáncer pulmonar de células no pequeñas tienen metástasis óseas al diagnóstico. A la radiografía es más frecuente el compromiso osteolitico, siendo los cuerpos vertebrales los sitios más afectados.
- Hígado: Las metástasis hepáticas sintomáticas son poco frecuentes en el curso de la enfermedad. Las metástasis hepáticas asintomáticas pueden detectarse en la presentación por elevación de las enzimas hepáticas o imagen compatible.
- Glándulas suprarrenales: Las glándulas suprarrenales son un sitio frecuente de metástasis, pero estas metástasis son raramente sintomáticas. Se debe sospechar en contexto de una masa adrenal unilateral detectada por TC en un paciente con un cáncer de pulmón conocido o sospechado. Sólo una fracción de las masas suprarrenales detectadas representan metástasis. Esto fue ilustrado por una serie de 330 pacientes con cáncer pulmonar de células no pequeñas, en el que 32 (10%) tenía una masa suprarrenal aislada. Sólo 8 de estos 32 (25%) eran malignos mientras que el resto tenía lesiones benignas. No obstante, un estudio negativo de imagen no excluye las metástasis suprarrenales. Un estudio de pacientes con cáncer pulmonar de células no pequeñas encontró que el 17% de las biopsias suprarrenales mostraron compromiso metastásico a pesar de tener una TC normal.
- 5) Extratorácicas no metastásicas o síndromes paraneoplasicos (10%): Desaparecen generalmente con la extirpación del tumor primario y no están relacionados con la invasión directa, obstrucción o metástasis. Pueden ocurrir en cualquier momento de la vida tumoral o anunciar su recurrencia. Entre los más frecuentes se encuentran:
- Hipercalcemia
- SIADH
- Síndrome de Cushing
- Síndrome de Eaton Lambert
- Dermatomiositis- Polimiositis
- Osteoartropatía hipertrófica
- Baja de peso-fiebre
- Anemia normocitica normocromica
- Coagulopatia
- Leucocitosis-eosinofilia
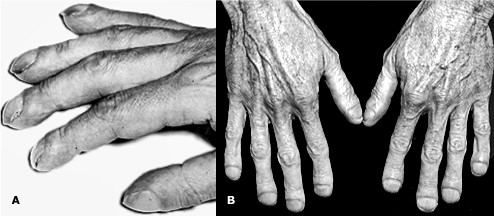
Hipocratismo Digital
Diagnóstico
Las herramientas diagnosticas son:
- 1) Radiografía de tórax: corresponde a la primera aproximación diagnostica. Tiene baja sensibilidad por lo que su normalidad no descarta la enfermedad.
- 2) TAC de tórax-Abdomen con contraste: posee mejor sensibilidad y especificidad que la Radiografía de tórax. Útil para caracterizar la lesión, identificar compromiso ganglionar mediastínico y metástasis hepáticas y suprarrenales.
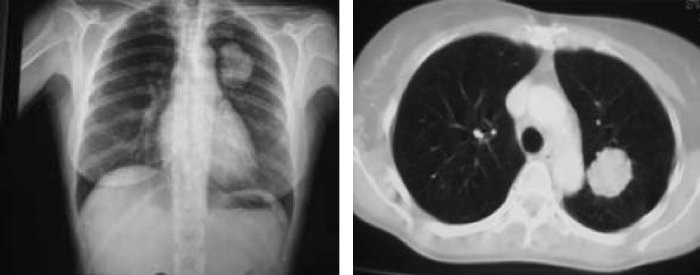 Carcinoma pulmonar de células no pequeñas
Carcinoma pulmonar de células no pequeñas
- 3) RNM de cerebro: útil en la búsqueda de metástasis cerebrales, principalmente en contexto de síntomas neurológicos. También es útil el TAC de cerebro, aunque con menor sensibilidad.
- 4) Cintigrafía ósea: útil en la búsqueda de metástasis óseas. Sospechar en contexto de dolor óseo, fractura en hueso patológico, hipercalcemia y aumento de las fosfatasas alcalinas.
- 5) Citología de la expectoración: Requiere que el paciente presente expectoración. También se puede obtener citología a través de punciones pulmonares percutáneas transtorácicas, de punciones de adenopatías superficiales que pueden aparecer en cánceres diseminados, o de punciones de otros órganos en enfermedades metastásicas.
- 6) Fibrobroncoscopia: Permite tomar muestras de aspiración de secreciones bronquiales, hacer cepillado de áreas sospechosas para estudiar la citología, hacer punciones transtraqueales o transbronquiales y obtener material para estudios citológicos, hacer lavados broncoalveolares con el mismo propósito y practicar biopsias ya sea endobronquial si el tumor es visible o transbronquiales apoyado por fluoroscopía si el tumor está más allá de la visibilidad endoscópica
- 7) Tomografía de emisión de positrones o PET con glucosa marcada: Se administra glucosa marcada que se acumula en los lugares de gran reproducción celular lo cual se demuestra a través de una Cintigrafía de todo el cuerpo pudiendo demostrarse la extensión del tumor y las posibles metástasis
- 8) Punción pleural: punción del espacio pleural con aguja fina, con anestesia local, en caso de derrame. El rendimiento de la citología del líquido pleural después de una toracocentesis única en pacientes con afectación pleural documentada es de aproximadamente 60%. Permite tomar citología del líquido pleural, y colaborar con la etapificación del cáncer pulmonar.
- 9) Punción pulmonar con aguja: procedimiento realizado bajo visión radioscópica o de TAC. Permite tomar muestras para estudio de citología o biopsia, de acuerdo al grosor de la aguja, de la lesión sospechosa. Puede confirmar la presencia de cáncer, su histología y etapificación.
- 10) Mediatinoscopía: consiste en la introducción de tubo rígido desde hueco supraesternal entre el esternón y la tráquea lo que permite tomar biopsias de ganglios mediastínicos sospechosos de tener compromiso tumoral. Confirma la presencia de cáncer, su histología y colabora en la etapificación.
- 11) Videotoracoscopía: introducción de tubo rígido en el espacio pleural. Permite tomar biopsias de la pleura y del pulmón. Se realiza en caso de derrame pleural cuyo estudio diagnóstico no se aclara con la punción pleural.
- 12) Toracotomía: Se utiliza en contexto de diagnostico dificultoso con medios menos invasivos y fuerte sospecha o confirmación de cáncer pulmonar, realizando en el mismo procedimiento la cirugía resectiva.
Tratamiento
Como parte del estudio previo al tratamiento, es fundamental realizar pruebas de función pulmonar (espirometria, test de caminata 6 minutos y DLCO), con tal de conocer la función pulmonar pre quirúrgico y compararlo con el estado post operatorio.
El tipo de tratamiento depende de la histología del cáncer;
- Cáncer de células pequeñas: se encuentra diseminado al diagnóstico en la gran mayoría de los casos por lo que no es quirúrgico, siendo en la quimio radioterapia el estándar del tratamiento. En general tiene una buena respuesta inicial al tratamiento, pero tiende a recaer en los meses siguientes. De no mediar tratamiento, la sobrevida promedio es de 2-4 meses y con tratamiento es de 18-24 meses. La radiación profiláctica cerebral se ha asociado a disminución de la recidiva en el SNC.
- Cáncer de no células pequeñas la cirugía es la única opción terapéutica, siendo curativa en etapas tempranas. En etapas localizadas (25% de los casos) la lobectomía mas linfadenectomia mediastinica radical es el tratamiento estándar. El tratamiento con radio quimioterapia puede ser una opción en pacientes no aptos para la cirugía en fases tempranas de su enfermedad o bien en pacientes con enfermedad avanzadas, antes o después de la cirugía. La técnica quirúrgica puede ser de dos tipos:
- Ø Toracotomía postero lateral a nivel del quinto espacio intercostal
- Ø Videotoracoscopia: consiste en el abordaje con 3 o 4 trocares a través de los cuales se introducen elementos de trabajo.
Pronóstico:
- Cáncer de células pequeñas: independiente del estadio, el pronóstico es malo. Pacientes con enfermedad localizada presentan una supervivencia entre 16-24 meses con las formas actuales de tratamiento.
- Cáncer de células no pequeñas: las estimaciones generales de supervivencia a 5 años, independientes del estadio, son de 10-15%
Seguimiento
El seguimiento es de por vida, clínico y con TC de tórax y estudio dirigido en cao de síntomas (cefalea, dolor óseo, etc) en busca de metástasis. Lo anterior, puesto que el riesgo de desarrollar un segundo primario pulmonar es de 1-2% luego de haber presentado un cáncer pulmonar.
Bibliografía
- Enfermedades respiratorias, 2da edición Juan Carlos Rodriguez, Alvaro Undurraga. Capítulos 52-53
- Up to date Overview of the risk factors, pathology, and clinical manifestations of lung cancer, David E Midthun, MD, Feb 03, 2017.
- Manual de Patología Quirúrgica PUC Christian Gallardo B, Patricio Salas V. Capitulo 40

