43. Prematurez
25/10/2016
Temas a tratar
- Prematurez: Definición y Epidemiología
- Prevención del parto prematuro e inducción de madurez pulmonar fetal
- Recién nacido prematuro, límites actuales de viabilidad y patologías asociadas: inmadurez pulmonar, apneas, hemorragia intracraneal, enterocolitis necrotizante, ductus persistente
- Uso de surfactante artificial
- Clínica y nociones generales del diagnóstico y la terapia de las complicaciones tardías del recién nacido prematuro: osteopenia del prematuro, displasia bronco, retinopatía del prematuro
1-. Prematurez: definición y epidemiología
Definición
Se define como prematuro a todo recién nacido (RN) menor a 37 semanas (según OMS), lo que corresponde al 6-10% de todos los partos. En neonatología, se usa la definición como RN menor de 38 semanas, pues los RN de 36-37 semanas tienen sutiles diferencias en su fisiología con respecto a los RN de término (RNT).
Según el peso de nacimiento, se pueden clasificar en:
– Bajo peso de nacimiento si pesa <2.500 g
– Muy bajo peso de nacimiento, si pesa <1.500 g, lo que equivale a las 32 semanas. Éste es el grupo al que van dirigidas las atenciones de salud del GES y representan el 0,99% de los partos, pero en hospitales de alta complejidad pueden llegar a ser el 3%. Actualmente su sobrevida es del 88% en HCUCH
– Extremo bajo peso si pesa <1.000 g Su pronóstico es ominoso
– Micronato, cuando su peso es entre 500 y 750 g. Su pronóstico es muy ominoso
Un feto de menos de 22 semanas, 500 gramos de peso o 25 cm de corona a rabadilla es considerado aborto y no RNP, pues es considera por la OMS el límite de la viabilidad.
Magnitud del problema
– La prematurez es la causa única más importante de morbimortalidad perinatal. Los prematuros de menos de 1.500 g representa el 25% de la mortalidad infantil y el 42% de la mortalidad neonatal; mientras que los sobrevivientes aportan el 4,47% de la mortalidad infantil tardía
– Excluidas las malformaciones congénitas, 75% de las muertes perinatales son atribuibles a prematurez. En globo, un RN prematuro (RNP) tiene un riesgo 20 veces mayor de muerte y 17 veces el de morbilidad que un RNT, mientras que un RNP de <1.500 g tiene un riesgo 180 veces mayor que un RNP de 2.500 g
– De los RN de muy bajo peso de nacimiento (RNMBP), la mitad presenta enfermedad de membrana hialina (EMH), prevenible en alrededor del 60% de los casos con el uso oportuno de corticoides
La mortalidad en los RNP ha ido disminuyendo, lo que se fundamenta en:
- Desarrollo de unidades de cuidados intensivos
- Uso rutinario de ventilación mecánica
- Monitorización intraparto
- Terapias de alto impacto: corticoides prenatales y surfactante exógeno (en presencia de enfermedad por membrana hialina (EMH))
etiología del parto prematuro
Se pueden agrupar en tres entidades clínicas, más o menos 1/3 cada una:
- Parto prematuro espontáneo con membranas íntegras (inicio espontáneo de contracciones uterinas (CU) con membranas íntegras
- Parto prematuro asociado a ruptura prematura de membranas (RPM)
- Parto prematuro iatrogénico (interrupción médica prematura del embarazo por causa materna <especialmente SHE y PE> o fetal)
El parto prematuro (PP) se considera un síndrome clínico de múltiples causas (infección intramaniótica, isquemia útero-placentaria, disfunción cervical, sobredistensión uterina, factores inmunológicos, hormonales, etc.) cuya expresión común es el inicio de dinámica uterina y dilatación cervical antes de las 37 semanas de gestación.
2-. prevención del parto prematuro e inducción madurez pulmonar fetal
prevención del parto prematuro
La prevención del parto prematuro se basa en el control antenatal, y ojalá preconcepcional, de inicio precoz, de forma de detectar factores de riesgo de PP, siendo los principales:
– Infecciones genitourinarias durante la gestación
– Gestación múltiple actual (50% gemelos son pretérminos y el 100% de los trillizos y más, factor de mayor riesgo de parto prematuro)
– Metrorragia de la segunda mitad del embarazo
– Polihidroamnios
– Parto pretérmino en embarazo anterior hasta 35 semanas edad gestacional (EG), aumenta 3-4 veces el riesgo y 2 PP 6 veces
– Antecedente de RPM en embarazo anterior
– Antecedente de incompetencia cervical (por ejemplo, secundario a uno cono)
– Antecedente de hospitalización por síntomas de parto pretérmino
– Embarazo con DIU
– Otros: menor nivel socioeconómico
Con esta lista de factores de riesgo, se pesquisan sólo el 50% de las mujeres que tendrán parto prematuro. De la misma forma, las pacientes catalogadas como de alto riesgo de PP tienen un 20% de riesgo de PP.
|
Amenaza de PP o síntoma de PP: dinámica uterina con 1 a 2 contracciones cada 10 minutos por 30 minutos más borramiento de 50% o más y/o dilatación de >1 cm. Trabajo de PP: dinámica uterina de 2 o más contracciones cada 10 minutos por 30 minutos más modificaciones cervicales (borramiento >80% o dilatación >3 cm) |
Prevención primaria
– Uso de ácido fólico 1 año antes de la concepción (disminuye riesgo PP en 50.70%)
– Búsqueda de factores de riesgo y de aparecer, derivar a nivel secundario
– Búsqueda de infección tracto urinario (ITU) y tratamiento en caso de ser hallada (nitrofurantoína 100 mg/8h, cefradina 500 mg/6h vo por 7-10 días en caso de bacteriuria asintomática)
– Medición de cérvix en ecografía de 22-24 semanas. Cérvix <15 mm detecta al 30% de las mujeres que tendrán PP, con <25 mm se identifica al 40% de los PP
– Doppler de arterias uterinas en ecografía 22-24 semanas para detectar riesgo de preeclampsia (asociado a necesidad de interrupción de parto a las 34 semanas)
Prevención secundaria
En pacientes de alto riesgo de PP:
– Administración de progesterona (17-OH progesterona caproato im 250 mg/semana o progesterona natural micronizada vaginal 200 mg/día) en población con cuello corto disminuye en 40% el riesgo de PP
– Búsqueda de vaginosis bacteriana. Tratamiento de elección es metronidazol 2 g una vez o 500 mg c/8h vo por 5 días
– En caso de antecedente de incompetencia cervical, debe sugerirse uso de cerclaje en caso de acortamiento cervical progresivo
Prevención terciaria
En caso de síntomas de PP o trabajo de PP, la paciente debe ser hospitalizada para observación y confirmar el diagnóstico. Si luego de 2 horas de observación y confirmado el diagnóstico, se procede a buscar etiología (fundamental descartar corioamnionitis), tocolisis e inducción de la madurez pulmonar, además de la prevención de infección por Streptococcus agalactiae (SGB). El tratamiento específico del PP fue tratado en el capítulo correspondiente.
inducción madurez pulmonar
Se deben usar en toda paciente en trabajo de parto prematuro entre 23 y 34 semanas de edad gestacional en forma paralela al uso de Tocolíticos. También están indicados en caso de interrupción prematura del embarazo por indicación médica o en casos de RPM, ambas también a ese rango de edad gestacional.
El beneficio máximo del corticoide se logra si éste se ocupa entre 48 horas y 7 días de la primera dosis, sin embargo, se ha demostrado algún beneficio clínico con tiempos menores, por lo que se indica de todas formas, por el contrario, el efecto se pierde más allá de 7 días por lo que se debe evitar su uso en caso de que el parto se postergue.
Betametasona 12 mg im cada 24 horas x 2 veces
No se recomienda la repetición rutinaria de los corticoides, pues 3 o más cursos han sido asociadas con mayor riesgo de restricción del crecimiento intrauterino. Sólo se recomienda una dosis de rescate de corticoides (idéntica a la primera) en caso de que exista alta probabilidad de parto inminente y han pasado más de 15 días del curso anterior de corticoides.
Los corticoides han mostrado ser útiles, disminuyendo riesgo de:
– Síndrome de distrés respiratorio neonatal (en un 50%)
– Apgar <3 a los 5 minutos
– Hemorragia intraventricular moderada a severa o Leucomalasia periventricular (LMPV)
– Más de 7 días de ventilación
– Mortalidad
– Riesgo de Enterocolitis necrotizante
neuroprotección
El sulfato de Magnesio ha mostrado ser neuroprotector en mujeres en trabajo de parto prematuro, reduciendo incidencia de parálisis cerebral o daño motor en los RN que sobreviven. La dosis recomendada es 4-10 g ev en infusión por 24 horas.
3-. patologías asociadas al recién nacido prematuro
A continuación, se presentan los principales problemas asociados al nacimiento prematuro, según la edad gestacional y según el sistema involucrado. Se profundizará en algunos de los problemas más importantes y que no son tratados en otros capítulos.
principales problemas según edad gestacional
| Edad Gestacional | Comentarios Generales | Principales Problemas |
|
Prematuros 34-36 semanas (Prematuros Tardíos) |
Es un grupo de mayor riesgo de rehospitalización, pero como no se hospitalizan, son “un poco olvidados”. Por ello es fundamental la educación sobre técnicas de lactancia y sobre los riesgos del bebé para que consulte precozmente |
-Succión difícil por menor actividad y tono -Termorregulación -Inmadurez pulmonar en algunos RN -Ictericia fisiológica del RN -Mayor prevalencia de ALTE |
|
Prematuros 32-34 semanas |
Pesan entre 1.500 y 2.00 g en promedio. Se hospitalizan siempre para evaluar capacidad de alimentación y pueden estar 15 a 30 días hospitalizados |
-Sin deglución -Termorregulación -Inmadurez pulmonar -Ictericia fisiológica del RN -Mayor prevalencia de ALTE |
|
Prematuros 28-31 semanas |
Grupo al que van dirigidos las políticas de estado para mejorar sobrevida, dado que son in grupo de alto riesgo y relativamente frecuente. |
-Inmadurez pulmonar -Termorregulación -Alimentación: baja capacidad gástrica, alto requerimiento y gravedad -Apneas -Riesgo patología grave del RNP como EMH, HIV |
|
Prematuros <28 semanas |
Requieren cuidados intensivos y sofisticados por lo que deben nacer en centro de alta complejidad. |
-Inmadurez global -Retinopatía, HIV, LPV, EMH, apneas, NET |
principales complicaciones por sistema
Las complicaciones del RNP derivan del binomio inmadurez más hipoxia, por el acortamiento de la edad gestacional y la ineficacia a la adaptación respiratoria postnatal
- Patología Respiratoria
Los problemas respiratorios derivan de 1) la inmadurez neurológica central, 2) debilidad de la musculatura respiratoria, 3) pulmón con menor desarrollo alveolar, déficit de surfactante y mayor grosor de membrana alveolocapilar, 4) menor desarrollo de la vasculatura pulmonar e 5) hiposensibilidad de los quimiorreceptores. Las principales patologías respiratorias son la Enfermedad de Membrana Hialina (principal causa de muerte neonatal, ver capítulo de síndrome de distrés respiratorio), apneas del prematuro y displasia broncopulmonar (ver en apartado siguiente). Otras manifestaciones respiratorias en el prematuro son el neumotórax, la hipertensión pulmonar, atelectasias, enfisemas, neumatocele, edema pulmonar y neumonía infecciosa y aspirativa.
Apneas del prematuro
Corresponde a la presencia de un ritmo respiratorio inestable (con pausas mayores a 20 segundos o menos tiempo si se acompaña de bradicardia o desaturación) reflejo de una inmadurez en los sistemas de control respiratorio que se resuelve típicamente con la maduración del RNP y que se espera cese al cumplir las 40 semanas de edad gestacional corregida. Por otro lado, otros cuadros inflamatorios, infecciosos, congénitos, cambios en la presión intracerebral y otros pueden tener como primera manifestación clínica una apnea o agravar su presencia si esta ya existía; por lo que deben ser descartados y no asumir que toda apnea en RNP se debe a su inmadurez.
En el 70% de los RNP menores de 34 semanas se presenta al menos un evento de apnea, siendo el riesgo inversamente proporcional a la edad gestacional. Varios estudios han mostrado que el desarrollo de apneas se asocia con peores resultados neurológicos.
Dentro de las medidas terapéuticas se encuentran:
– Posición prona
– Uso de presión positiva continua sobre vía aérea superior (CPAP)
– Metilxantinas. Su mecanismo de acción es poco claro. Los fármacos más usados de este grupo son la cafeína (primera línea, 20 mg/kg iv en bolo por 30 minutos seguido por 5 mg/kg iv día) y la teofilina
– Doxapram
– Otras: flujo nasal, ventilación convencional (en casos refractarios al CPAP), estimulación sensorial, inhalación de CO2
Se ha observado que el uso de la cafeína mejora las apneas de pretérmino.
- Patología Neurológica
Existe una inmadurez del SNC, siendo lo más relevante la fragilidad de la vasculatura a nivel de matriz germinal que predispone al desarrollo de hemorragia intraventricular (HIV) e infarto hemorrágico. La leucomalacia periventricular representa el daño hipóxico de la sustancia blanca y que también se ve más frecuentemente en RNP. La sintomatología neurológica en el RNP es vaga, sutil e inespecífica, por lo que debe ser buscada dirigidamente y en este sentido, la incorporación de la ecografía cerebral como tamizaje es muy útil.
Hemorragia Intraventricular (HIV)
Es la lesión cerebral más frecuente en el RNP y se produce en el 50% de los RN con peso <750 g y en el 2-30% de los <1.500g. Si bien su incidencia no ha disminuido significativamente, si han disminuido las formas graves (III y IV), así como la lesión parenquimatosa asociada (infarto hemorrágico periventricular <IHP>). En el prematuro, la HIV se producen en la matriz germinal subependimaria en el 90% de los casos y menos frecuentemente en los plexos coroideos (a diferencia del RNT) y suele ocurrir dentro de las primeras horas de vida.
En su origen, participarían factores anatómicos derivados de la fragilidad capilar de la matriz germinal, factores hemodinámicos por fluctuaciones del flujo cerebral y aumento de la presión venosa cerebral y alteraciones de la coagulación.
Los grados leves suelen ser asintomáticos, las repercusiones clínicas aparecen en casos severos e incluyen shock, acidosis metabólica, anemia y manifestaciones neurológicas. Por esto, el diagnóstico es con ultrasonografía cerebral (la que debe ser realizada como screening en el RNP), con la cual además se puede clasificar la HIV en 4 grados:
- Grado I: hemorragia localizada sólo en matriz germinal subependimaria
- Grado II: contenido de sangre intraventricular ocupa menos del 50% de la cavidad
- Grado III: la sangre ocupa más del 50% de la cavidad ventricular
- Grado IV: A lo anterior se asocia sangrado intraparenquimatoso
La ultrasonografía cerebral debe ser realizada durante las primeras 48 horas de vida, repetida a la semana y luego al mes de vida.
No hay tratamiento específico para la HIV, sólo se dispone de manejo paliativo con un manejo óptimo de la hemodinamia y el manejo de las convulsiones. Sí existen formas de prevenirlas:
– Prevención del parto prematuro
– Corticoides antenatales
– Manipulación cuidadosa del RNP (evitar procedimientos invasivos)
– Evitar infusión rápida con agentes osmóticos
– Mantención de hemodinamia estable
– Uso de Indometacina para cierre del ductus
– Evitar asincronía con el ventilador
Los casos leves de HIV (tipos I y II) suelen no tener secuelas, sin embargo, cuando aparece hemorragia intraparenquimatosa o cuando se produce ventriculomegalia post-hemorrágica o hidrocefalia post-hemorrágica (en este último hay aumento de presión intracerebral a diferencia del anterior), sí hay riesgo.
Leucomalacia Periventricular (LPV)
Corresponde a la necrosis de la sustancia blanca periventricular. Tiene asociación importante con la HIV, pues se asocia a prematurez, daño hipóxico e inmadurez vascular del cerebro y se ve en el 4-10% de los RNP de 1.000 g. Su diagnóstico se realiza con ultrasonografía cerebral, siendo signos sugerentes la hiperecogenicidad periventricular persistente (más de 15 días), ensanchamiento ventricular y contorno irregular o bien la clásica forma quística. Su prevención se realiza evitando el parto prematuro, manteniendo perfusión cerebral en forma adecuada y con un tratamiento adecuado de la ventriculomegalia post hemorrágica.
En las fases iniciales, la LPV es asintomática, para luego dar las clásicas alteraciones del tono muscular y secuelas, siendo la principal, la diplegia espástica, pero también se ha asociado a déficit intelectual, y otros trastornos del neurodesarrollo.
- Cardiovascular
Los fenómenos observados incluyen:
– Hipotensión: producida por incapacidad del sistema autonómico de mantener el tono y otros factores como sepsis, hipovolemia o disfunción cardíaca. El tratamiento es monitorización estricta, reposición de volumen con solución fisiológica 10-20 ml/kg y drogas vasoactivas (aunque estas últimas de uso controvertido)
– Persistencia del ductus arterioso: como se mencionó, el cierre del ductus depende del aumento de la pO2 y de la disminución de la presión pulmonar, sin embargo, en RNP estos fenómenos son menos marcos y/o hay insensibilidad a estos cambios, impidiendo el cierre. El ductus, genera un shunt izquierda-derecha (contrario al fetal). Se manifiesta como un soplo sistólico de eyección con manifestaciones en distinto grado de insuficiencia cardíaca. Es clásica la historia de un RNP con SDR que empieza a empeorar luego venir en mejoría. El tratamiento es con inhibidores de prostaglandinas (Indometacina o ibuprofeno) o bien un cierre quirúrgico
- Gastrointestinales
Algunos problemas son:
– La maduración de la succión y deglución se alcanza entre las 32 y 34 semanas, antes de este período la alimentación debe ser parenteral o enteral. Debe considerarse además que hay una baja capacidad gástrica y alta susceptibilidad al reflujo
– La absorción intestinal madura rápidamente si es potenciada por la presencia de sustrato, por lo que el uso de alimentación precoz con leche materna fortificada (o fórmula especial) son un pilar básico del manejo del RNP
Enterocolitis Necrotizante (NET)
La prematuridad es el factor de riesgo individual más importante para enterocolitis necrotizante (NET), especialmente cuando ha habido uso de fórmula por vía enteral. Esta entidad mezcla múltiples factores tanto madurativos, como hipoxémicos, vasculares, infecciosos e incluso genéticos.
Se estima una incidencia entre 0,5 y 5 por cada 1.000 nacidos vivos y del 7% en los niños de bajo peso de nacimiento. Se presenta en un RNP de 1 a 3 semanas de vida como un cuadro de distensión abdominal, sangre en las heces, aspecto séptico que tienden a empeorar progresivamente. Es característica la presencia de neumatosis intestinal (gas dentro de las paredes intestinales) y gas portal en los exámenes radiológicos.
El tratamiento es médico con régimen 0, uso de antibióticos de amplio espectro, monitorización clínica y de laboratorio, soporte cardiorrespiratorio y hematológico, y aspiración suave e intermitente por sonda nasogástrica. Cuando el proceso es severo, debe sugerirse tratamiento quirúrgico con drenaje peritoneal y/o resección intestinal (con anastomosis término-terminal o colo-enterostomía).
La mortalidad es alta (15-30%) siendo la edad gestacional y el peso de nacimiento los factores que determinan el pronóstico. Un porcentaje elevado presentará secuelas como estenosis o síndrome de intestino corto (en caso de resolución quirúrgica). Por otro lado, la NET es un signo de mal pronóstico neurológico en el RNP.
- Inmunológicos
El RNP posee una inmunidad innata ineficaz, con vulnerabilidad de las barreras (piel y mucosas), incompleta fagocitosis, menor inmunidad específica (por menos traspaso de IgG y ausencia de IgA e IgM) esto predispone a infección y cuando esto ocurre, se produce una sepsis. Si a todo esto se suma la manipulación invasiva del RNP y la estadía hospitalaria, el riesgo de infección aumenta. Este tema se tratará en los capítulos correspondientes.
Las vacunas deben ser administradas en los RNP según el mismo protocolo que los RNT.
- Metabolismo y Nutrición
– Termorregulación: La producción de calor está disminuida a consecuencia de 1) menor producción de calor por el metabolismo basal, 2) menores reservas de grasa, especialmente grasa parda, 3) aumento de la superficie corporal, 4) deficiente control vasomotor y 5) menor aislamiento cutáneo. Todo esto predispone al desarrollo de hipotermia
– Hipocalcemia
– Hipoglucemia (por escaso depósito) e hiperglicemia (en RNP extremos por alteración en la regulación de la insulina)
– Hiperbilirrubinemia: existe una inmadurez hepática más marcada que predispone al desarrollo de ictericias más severas que en los RNT
– Riesgo nutricional: existe un requerimiento calórico aumentado, lo que sumado a las mayores pérdidas por deposiciones, aumenta el riesgo de desnutrición. Por otro lado, las dificultades en la succión y deglución, la tendencia al íleo y el riesgo de enterocolitis necrotizante ha obligado a generar normas estrictas con respecto a la alimentación del RNP tanto en vía de administración, volumen a administrar, aumento diario y fecha de inicio de la alimentación
- Hematológicos y Endocrinológicos
– Anemia del prematuro: Se acentúa la anemia producida por la hemólisis fisiológica sumada a la extracción repetida. Esto aumenta el riesgo de necesidad de transfusión
– Se producen signos de hiperfunción tiroidea que pueden encubrir un hipotiroidismo subyacente
4-. complicaciones tardías del rn
4.1 Displasia Broncopulmonar (DBP)
Enfermedad crónica producida por la inmadurez del sistema respiratorio y que se traduce en requerimientos de oxígeno >21% por más de 28 días en RNP de menos de 32 semanas de edad gestacional y/o menos de 1.500 g. Se plantea que su origen estaría en el daño de la vía aérea y el alveolo secundario a la hiperoxia local y el barotrauma asociado a la oxigenoterapia y ventilación mecánica.
|
DBP leve: sin necesidad de O2 a las 36 semanas de edad o al alta DBP moderada: necesidad de ½ litro o menos de O2 a las 36 semanas de edad o al alta DBP severa: necesidad de más de ½ litro de O2 y/o apoyo ventilatorio a las 36 semanas de edad o al alta |
Prevención:
– Prevención del parto prematuro
– Uso de corticoide antenatal
– Uso de surfactante precoz
– Aporte nutricional óptimo
– Preferir CPAP con surfactante precoz o ventilación mecánica gentil
– Oxigenoterapia controlada
– Cierre farmacológico o quirúrgico precoz del ductus arterioso persistente
– Tratamiento precoz y oportuno de las infecciones sistémicas y pulmonares
– Uso de vitamina A im
Tratamiento y seguimiento
Incluye oxigenoterapia, aporte nutricional adecuado (140-180 kcal/kg/día), restricción de fluidos, uso de diuréticos, teofilinas (cafeína), kinesioterapia respiratoria y broncodilatadores en caso de coexistir hiperreactividad bronquial. Otras medidas pueden plantearse según necesidad
Los pacientes candidatos a oxigenoterapia deben, previo al alta, deben tener una radiografía de tórax, una ecocardiografía y saturometría por 12 horas. Además deben tener profilaxis con Palavizumab® y las vacunas anti-neumocócica y anti-influenza. El seguimiento incluye un control a los 15 días del alta y luego semestral con broncopulmonar hasta los 6 años de edad (controles más frecuentes en casos especiales)
4.2 retinopatía del prematuro
Es una enfermedad angioproliferativa de la retina incompletamente vascularizada del prematuro de muy bajo peso de nacimiento o menor a las 32 semanas que se caracteriza por la aparición de anormalidades visibles en fondo de ojo y que constituye la principal causa de ceguera infantil. Su incidencia llega al 11% en embarazos pretérmino de menos de 1.500 g, pero sólo requieren tratamiento quirúrgico 4,4%.
Entre los factores de riesgo asociados se encuentran la hipotensión y el shock, la oxigenoterapia prolongada, la ventilación mecánica prolongada, necesidad de transfusiones, apneas, deficiencia de vitamina E y acidosis.
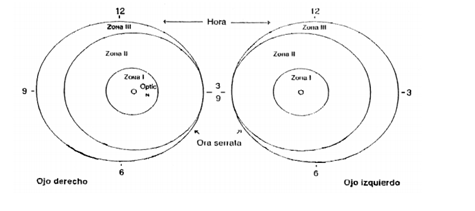
La clasificación internacional evalúa:
– Localización: 3 zonas à zona I (central, peor pronóstico), zona II, a la periferia de la zona I, y zona III a la periferia de la zona 2
– Severidad: considerando 5 etapas
– Extensión: medida según husos horarios
– Presencia de enfermedad plus: dícese de la dilatación progresiva y tortuosidad de los vasos en al menos 2 cuadrantes del polo posterior, a veces con opacidad y hemorragia vítrea. Es un factor de mal pronóstico
Enfermedad umbral: aquella que produce ceguera en el 50% de los pacientes. Se considera aquellos casos en que se comprometan 5 husos horarios contiguos u 8 alternos con ROP en etapa 3 y enfermedad plus.
Además de los factores anteriores, el desprendimiento de retina y la aparición precoz de enfermedad son también factores de mal pronóstico.
La base del tratamiento está en la detección precoz mediante fondo de ojo por oftalmólogo a partir de las 4 semanas de edad postnatal a todo prematuro <32 semanas de edad gestacional y/o <1.500 gramos. El examen debe ser repetido hasta alcanzar la vascularización completa de la retina. La decisión del tratamiento y seguimiento depende del especialista, pero a grandes rasgos se considera indicación de tratamiento la presencia de enfermedad umbral y el tratamiento de elección es la fotocoagulación láser.
4.3 osteopenia del prematuro
Deficiencia de la mineralización ósea post natal del RNP, con alteración de la remodelación ósea y potencial reducción de la tasa de crecimiento. Se desarrolla en forma progresiva en las primeras semanas de vida que puede llevar a la aparición de signos de raquitismo (displasia epifisiaria y deformidad esquelética, fractura en hueso patológico) a los 2-4 meses de vida. El riesgo es inversamente proporcional a la edad gestacional y se puede observar en el 30% de los RN <1.500 g y 50% de los <1.000 g que no han recibido suplemento de Calcio, Fósforo y Vitamina D (mediante leche materna fortificada o fórmula suplementada).
Su etiología es multifactorial, siendo el menor depósito mineral óseo en comparación a un RNT el principal factor. A esto se suma el déficit de calcio y fósforo y de vitamina D, que son de baja concentración en la leche matera con respecto a las necesidades y cuyas pérdidas están elevadas (Hipercalciuria)
Su diagnóstico debe ser por laboratorio, pues la clínica es tardía. Para ello se pueden utilizar las fosfatasas alcalinas (FA; si son sobre 500 es diagnóstico de osteopenia leve, sobre 800 moderada y sobre 1.000 se asocia a talla baja) y la fosfemia (la cual disminuye [< 5mg/dl] antes que aumenten las FA). Puede apoyarse además de imágenes como radiografías (que comprueban osteopenia y constatan fracturas y otras alteraciones óseas) y fotodensitometría/fotoabsorciometria que es más sensible en etapas precoces.
Deben controlarse seriadamente las FA desde la 3° semana de vida y cada 15 días hasta el alta o las 40 semanas corregidas. Controles más frecuentes y exámenes adicionales se evaluarán caso a caso.
El manejo es la prevención mediante el suplemento con:
– Vitamina D 400-500 UI/día hasta el año de edad gestacional corregida
– Calcio 120-200 mg/kg/día y Fósforo 80-120 mg/kg/día hasta los 3 kg, 40 semanas de edad corregida o normalización de FA. Esto en caso de lactancia materna exclusiva, en caso de fórmula exclusiva, usar fórmula enriquecida con Ca y P
4.4 secuelas neurológicas
Las más frecuentes son la discapacidad motora, los trastornos de aprendizaje y los sensitivos como ceguera y sordera. Debe recordarse que hay un riesgo del 10% de parálisis cerebral en RNP de muy bajo peso de nacimiento
4.5 Otras
– Problemas nutricionales
– Infecciones a repetición y síndrome bronquial obstructivo recurrente (SBOR). Se destaca el mayor riesgo de infección y enfermedad grave por VRS, por lo que al RNP se le administra Palavizumab®, anticuerpos contra este virus para evitar el riesgo de enfermedad grave causada por él
– Mayor prevalencia de hernias inguinoescrotales
– Mayor prevalencia de deformidad craneal escafocefálica, hipoplasia maxilar y paladar ojival
– Hospitalizaciones más frecuentes
Referencias
- Clase Dr Jorge Burgos. Prematurez, Riesgos y Complicaciones 2015
- Guía Clínica Prevención Del Parto Prematuro 2010
- Rellan S, García C, Aragon M. EL Recién Nacido Prematuro. Protocolos de Diagnóstico Terapéuticos de la AEP: Neonatología. 68-77.
- Demestre X, Raspall F. Enterocolitis Necrotizante. Protocolos de Diagnóstico Terapéuticos de la AEP. Neonatología 405-410
- Guía Clínica Displasia Bronquiopulmonar Del Prematuro 2009. MINSAL, Gobierno de Chile
- Solari F, Pavolv J. Síndrome Apneico en el Recién Nacido Prematuro. 2013. Rev Med Clin Condes 24(3): 396-402
- Cabañas F y Pellicer A. Lesión Cerebral en el Niño Prematuro. Protocolos de Diagnóstico Terapéuticos de la AEP. Neonatología 253-269
- Guías Nacionales de Neonatología 2005, MINSAL, Gobierno de Chile
- Guía Clínica Retinopatía del Prematuro. 2010. MINSAL, Gobierno de Chile.
Guillermo Lorca Ch
