XXI. ROTURA PREMATURA DE MEMBRANAS
1. Introducción
La rotura prematura de membranas (RPM) se define como la solución de continuidad espontánea de las membranas ovulares antes del inicio del trabajo de parto.
La prevalencia de la RPM es de un 8 -10%; de éstas, 80% son en embarazos de término y un 20% en embarazos de pretérmino.
En Chile, la prematurez es la principal causa de morbimortalidad perinatal. Un tercio de los partos prematuros (27%) son debido a la Rotura Prematura de Membranas.
Los factores de riesgo (FR) para RPM pueden estar dados por condiciones maternas, genéticas o ambientales. La mayoría de los FR se comparten con los de parto prematuro, sin embargo, una historia de RPO de pretérmino en embarazos previos, infecciones de tracto genital (vaginosis bacteriana), metrorragia de II y III trimestre y el tabaquismo tienen una asociación más fuerte.
Otros FR son: cuello corto de < de 25 mm en II trimestre, antecedente de incompetencia cervical, fibronectina > a 50 ng/dL, PHA severo, embarazo gemelar, la presencia de DIU, hipertensión arterial, DM, anemia, consumo de café, la presencia de vaginosis bacteriana, N. gonorrea o C. tracomatis en tracto genital, así como algunas malformaciones uterinas.
En cuanto a los iatrogénicos, son importantes, la amniocentesis genética (riesgo de 1-2%), la fetoscopía (riesgo de 6-10%) y el cerclaje electivo y de urgencia (2% y 65% respectivamente).
2. Complicaciones de la RPM
Al romperse las membranas, comienza el período de latencia para iniciar en trabajo de parto, aumentando así el riesgo de infección materno-fetal y la posibilidad de compresión del cordón umbilical.
Podemos dividir las complicaciones en: Maternas:
- Infección intraamniótica y corioamnionitis clínica. A menor edad gestacional, y menor cantidad de líquido amniótico, mayor es la probabilidad de estas complicaciones.
- Endometritis puerperal (2-13%).
- Desprendimiento previo de placenta normoinserta 4-12%.
- Sepsis materna.
Fetales:
- Aumenta la morbimortalidad perinatal en globo, dependiendo principalmente de la edad gestacional al momento de la RPM.
- Síndrome de respuesta inflamatoria sistémica fetal (FIRS): 30 % de las mujeres con RPM de pre-término tienen bacteremia fetal.
- Deformaciones esqueléticas.
- Hipoplasia pulmonar.
- Aumenta el riesgo de cesárea por presentación distócica y alteraciones en la monitorización fetal intraparto.
- Muerte fetal: 33% en embarazos menores de 24 semanas, 3.8 a 22 % en embarazos de 16-28 semanas, 0 a 2% en embarazos de 30-36 semanas.
- Prolapso de cordón.
3. Diagnóstico de RPM
La historia clínica clásica de pérdida incontenible de líquido claro, transparente en abundante cuantía por genitales, tiene una sensibilidad del 90%. La historia clínica junto con el examen físico, es suficiente para el diagnóstico en el 53% de los casos.
Test adicionales que se pueden utilizar:
- – Test de Cristalización: bajo microscopía se observa la cristalización de las sales de sodio en forma de La muestra debe ser obtenida del fondo de saco o pared vaginal y se debe secar por 10 minutos antes de ser observada. Sensibilidad 51-98% y especificidad 70-88%. Falsos positivos de 5 a 10%.
- – Prueba de la Nitrazina: se basa en el viraje en el color (a azul) que sufre una cinta reactiva de nitrazina, cuando es expuesta a un pH mayor de El pH normal de la vagina durante el embarazo es de 4 a 5.5, mientras que el líquido amniótico tiene normalmente un pH de 7 a 7.5. Sensibilidad de 90%, falsos positivos hasta un 20%.
- – Amnisure®: test rápido que identifica la glicoproteína PAMG-1 (alfa 1 microglobulina placentaria), que se encuentra normalmente en las secreciones cervicovaginales, Es positiva para RPM si se encuentra en valores sobre 5 ng/ml. Sensibilidad 98-99% y especificidad de 88-100%.
- – Ecografía Obstétrica: puede observarse líquido amniótico disminuido. Por si solo, no hace diagnóstico. Es útil para confirmar edad gestacional, vitalidad fetal, presentación, diagnosticar malformaciones y localización placentaria.
- – Inyección intraamniótica de índigo carmín, asociado a la presencia de un tampón vaginal estéril para documentar la salida del colorante hacia el tracto genital inferior; es el Gold Standard para el diagnóstico de Se debe diferenciar la RPM, principalmente de leucorrea, pérdida de tapón mucoso e incontinencia urinaria. Otras causas son rotura de quiste vaginal e hidrorrea decidual.
4. Manejo de RPM
Para enfrentar el manejo de las mujeres con RPM, se debe individualizar los riesgos y beneficios del manejo conservador versus la interrupción del embarazo. Existen condiciones que justifican la interrupción inmediata de embarazo: corioamnionitis clínica, desprendimiento prematuro de placenta normoinserta, muerte fetal, compromiso de la unidad feto-placentaria y trabajo de parto avanzado.
Evaluación inicial:
- Confirmar edad gestacional con FUR y Eco precoz.
- Control de signos vitales.
- Control Obstétrico: latidos cardiofetales y dinámica uterina.
- Examen Físico: enfrentamiento debe minimizar riesgo de infección.
- − Inspección de los genitales externos (genitales húmedos y pérdida de líquido espontánea o con maniobras de Valsalva).
- − Especuloscopía (pérdida de líquido por OCE espontánea o con maniobras de Valsalva, observar cuello y presencia de partes fetales incluido cordón umbilical).
- − Test de cristalización.
- Ultrasonido Obstétrico: evaluar líquido amniótico, biometría y anatomía fetal.
Una vez confirmada la RPM, esta puede ser dividida: Según la situación infecciosa y la edad gestacional en la que ocurre el evento.
Manejo según la situación infecciosa:
Infección Intraamniótica (IIA): se observa en el estudio de líquido amniótico, > 50 leucocitos, <14mg/dl de glucosa, LDH >400 U/L. La Infección intraamniotica se confirma con cultivo o PCR positivo.
Si con menor edad gestacional, se debe utilizar antibióticos de amplio espectro, se sugiere esquema:
Clindamicina 600 mg cada 8 horas ev + Gentamicina 240 mg/día VO + Eritromicina 500 mg cada 6 horas VO.
El uso de tocolíticos está contraindicado en caso de IIA.
RPM ≥ 34 semanas:
En rotura prematura de membranas >34 semanas, se sugiere interrupción inmediata.
Disminuye el riesgo de infección materna, sin diferencias en el outcome neonatal ni la tasa de cesáreas. El uso de corticoides, por lo que no está indicado.
RPM entre 24 y 34 semanas:
El uso de antibióticos, aumenta el período de latencia al parto. El uso de corticoides en embarazos de pretérmino, disminuye el riesgo de muerte, distress respiratorio, hemorragia intracerebral, enterocolitis necrotizante. Los Tocolíticos no sirven para prolongar la latencia al parto.
Los pilares del manejo expectante son: Inducción de Madurez Pulmonar y Antibioticoterapia.El objetivo de los antibióticos en la conducta expectante es aumentar el período de latencia, prevenir la infección decidual ascendente para prolongar el embarazo, reducir la morbilidad asociada a la edad gestacional y la patología infecciosa del neonato. El esquema propuesto es, manejo agresivo endovenoso por 48 horas (ampicilina 2 gr cada 6 horas y eritromicina 250 mg IV cada 6 horas), seguido por 5 días de esquema oral (amoxicilina 500 mg cada 8 horas VO + eritromicina 500 mg cada 6 horas VO).
El uso de terapia con corticoides: betametasona 12 mg cada 24 horas intramuscular por 2 veces o dexametasona 6 mg cada 12 horas.
En RPM el uso de tocolíticos está contraindicado.
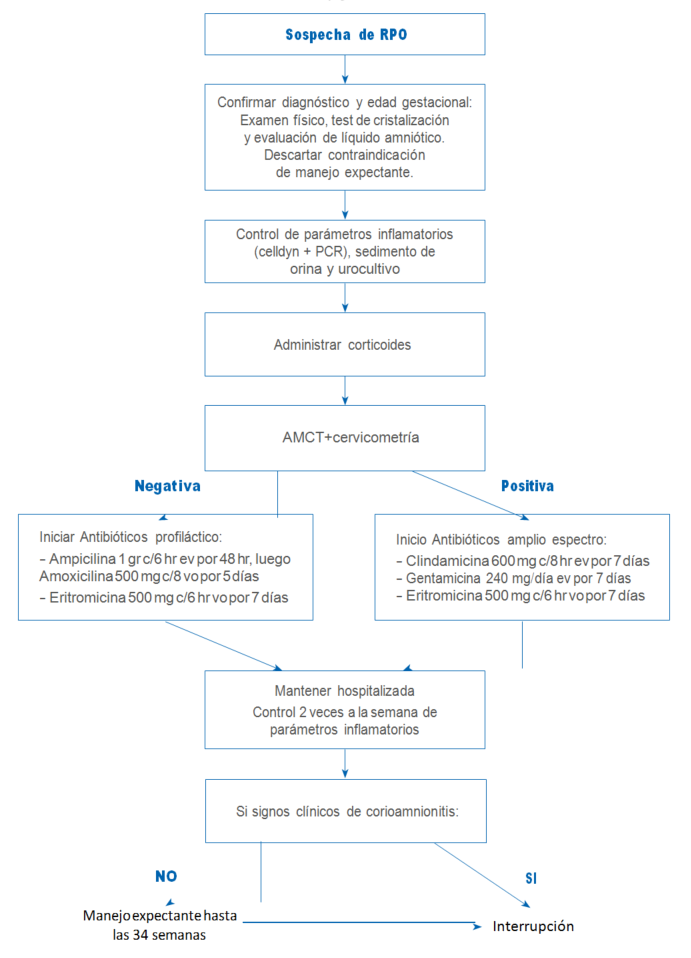
Esquema de manejo, ver flujograma 1
|
Conducta: • Hospitalizar en Unidad de Alto Riesgo Obstétrico. • Descartar contraindicaciones de manejo expectante. • Tomar parámetros inflamatorios: hemograma VHS, PCR, sedimento de orina y urocultivo. • Amniocentesis de la muestra de líquido amniótico. Evaluar gram, glucosa, leucocitos, LDH, cultivos para aerobios, anaerobios, Mycoplasma y Ureaplasma. En mujeres portadoras de DIU, realizar cultivo para hongos. Si no es posible realizar amniocentesis, iniciar antibióticos profilácticos. • Control de signos vitales y obstétricos cada 6 horas. • Corticoides: betametasona 12 mg cada 24 horas intramuscular por 2 veces o dexametasona 6 mg cada 12 horas. • Iniciar antibióticos profilácticos (ampicilina 2 gramos cada 6 horas ev por 48 horas, luego amoxicilina 500 mg cada 8 horas VO por 5 días + eritromicina 500 mg cada 6 horas VO por 7 días). • Parámetros inflamatorios 1 o 2 veces a la semana, según evolución clínica y establidad de parámetros. • Control de unidad feto placentaria. • Evaluar momento de la interrupción: − En mujeres estables sin evidencia de infección ni inflamación intraamniótica, interrupción a las 34 semanas. − Ante inflamación o infección intraamniótica se discutirá momento de interrupción de manera individual, a partir de las 28 semanas, según germen aislado, presencia de OHA, y otros. |
RPM < a 24 semanas:
Esta complicación obstétrica es de baja incidencia, ocurre en el 0.35% de los embarazos, sin embargo está asociada a una alta tasa de morbimortalidad materna y perinatal.
Las complicaciones maternas se relacionan al riesgo de corioamnionitis, descrita los primeros días posterior a la RPM. Su incidencia disminuye drásticamente luego de los 7 primeros días y existiría un mayor riesgo de corioamnionitis al estar asociado a oligohidroamnios. Otras complicaciones descritas son el desprendimiento prematuro de placenta normoinserta y sepsis materna.
Flujograma 1