XIV. INFECCIONES
1. INFECCIONES CÉRVICOVAGINALES
En forma genérica, las infecciones vaginales pueden definirse clínicamente como una alteración de la ecología microbiológica vaginal que habitualmente resulta en uno o más de los siguientes síntomas y signos:
- Flujo vaginal o leucorrea (término usado comúnmente).
- Mal olor.
- Ardor.
- Prurito.
- Dolor.
Desde el punto de vista microbiológico, la infección cérvico-vaginal ha sido definida por la presencia de:
- Vaginosis bacteriana sintomática.
- Vaginitis aeróbica.
- Vaginitis por Trichomona vaginalis.
- Vulvovaginitis micótica.
- Infecciones cervicales: Chlamydia trachomatis, Neisseria gonorrhoeae.
- Micoplasmas genitales.
1.1 Vaginosis bacteriana (VB)
Se caracteriza por ausencia o escasa cantidad de Lactobacillus y su reemplazo por una microbiota compleja y abundante dominada por Gardnerella vaginalis, Bacteroides spp., Prevotella spp., Peptostreptococcus spp., Mobiluncus spp. Y Mycoplasma hominis, lo que produce una alcalinización del pH vaginal.
Puede ser sintomática (con flujo vaginal) en la mitad de los casos y asintomática, razón por la que se llama vaginosis y no vaginitis. La causa de la VB y de la ausencia de respuesta inflamatoria local es desconocida, pero puede ser considerada como una condición de desorden microbiano e inmunológico de la mucosa. La VB con respuesta inflamatoria aumentada, se asocia con parto prematuro.
Frecuencia
Su frecuencia en nuestro medio varía dependiendo del grupo estudiado: embarazadas normales 26 %, rotura prematura de membranas de pretérmino 35 %, parto prematuro con membranas intactas 43 %, pielonefritis aguda del embarazo 32%.
Tabla 1: Criterios clínicos para el diagnóstico de vaginosis bacteriana
|
• Flujo vaginal grisáceo, adherente, flocular, de mal olor, con escaso componente inflamatorio. • Olor a pescado descompuesto al mezclar 1 gota de secreción con 1 gota de KOH al 10% (prueba de KOH o de aminas) • pH vaginal > 5 • Presencia de bacterias tapizando la superficie de células epiteliales de la vagina (células guía o clue cells) al observar microscópicamente una muestra de secreción al fresco. |
Diagnóstico microbiológico
El diagnóstico definitivo de VB se realiza mediante la tinción de Gram de secreciones vaginales. Se utiliza una escala de 1 a 10. Cuando el valor calculado es de 7 o más, se establece el diagnóstico de vaginosis bacteriana (criterios de Nugent).
Complicaciones obstétricas
La importancia de la VB en el embarazo, es su asociación con parto prematuro. Las mujeres con VB tienen 2 a 3 veces más riesgo de desarrollar un parto prematuro e infecciones puerperales. Las bacterias asociadas a VB, Prevotella, Bacteroides spp., Mobiluncus producen mucinasas que degradan el moco cervical, con la pérdida de la barrera mucosa y acción directa sobre las membranas ovulares favoreciendo su rotura. Al mismo tiempo favorece la adherencia, colonización y multiplicación bacteriana.
Sin embargo, el desarrollo de estas complicaciones se concentra en mujeres con factores de riesgo (Ovalle y cols.) tales como:
- Parto prematuro previo.
- Historia de abortos de segundo trimestre.
- Historia de infecciones del tracto urinario o bacteriuria asintomática.
- Episodios repetidos de infección cervicovaginal (3 o más).
- Diabetes pre o gestacional.
Consideraciones Clínicas
- Cuál es el manejo de la VB durante el embarazo?
Las mujeres sin factores de riesgo, debieran tratarse para mejorar su sintomatología vaginal. Las mujeres con factores de riesgo, deben tratarse por vía oral porque es posible que el tratamiento, especialmente con clindamicina, reduzca la tasa de partos prematuros, si es iniciado antes de las 20 semanas.
- Mujeres sin factores de riesgo
- − Tratamiento local con metronidazol (ovulos vaginales de 500 mg al día, por 1 semana) o clindamicina (crema vaginal, 1 aplicación por 1 semana u oral, ver más adelante).
- − No se requiere tratamiento de la
- Mujeres con factores de riesgo
- − Tratamiento sistémico oral con metronidazol (250-500 mg c/8-12 horas x 7 días) o Clindamicina (300 mg cada 8 horas x 7 días).
- − No se requiere tratamiento de la
- − Salvo excepciones, la desaparición de la sintomatología puede ser considerada suficiente como índice de curación terapéutica.
Durante el primer trimestre, el tratamiento puede realizarse primariamente con clindamicina, pero existe un acuerdo creciente de que el metronidazol también puede administrarse en forma segura.
• Es recomendado el tamizaje universal para VB durante el embarazo?
Se recomienda el tamizaje sólo en mujeres con antecedente de parto prematuro espontáneo
1.2. Vaginitis Aeróbica (VA)
Cultivo (+) para bacterias cocáceas gram positivas, bacilos gram negativos, bacilos gram positivos gruesos, aeróbicos, asociadas con aumento de leucocitos polimorfonucleares > 10 por campo, 400x al examen microscópico al fresco y ausencia o escasa cantidad de Lactobacillus.
Streptococcus agalactiae (Estreptococo beta-hemolítico Grupo B)
El estreptococo grupo B (EGB) es una bacteria gram positivo de alta frecuencia. Coloniza frecuentemente el tubo digestivo distal y el aparato genital inferior de la mujer.
El diagnóstico se realiza tomando un cultivo en el tercio inferior de la vagina y región ano-perineal. Recordar que la mujer portadora es habitualmente asintomática y no debe esperarse la presencia de flujo vaginal
Además del riesgo neonatal, el EGB se ha asociado con bacteriuria asintomática, infección intrauterina, parto prematuro, muerte perinatal, aborto de segundo trimestre e infecciones puerperales.
El diagnóstico se realiza tomando un cultivo selectivo (el más utilizado es el cultivo de Todd- Hewitt) en el tercio inferior de la vagina y región ano-perineal. La toma de la muestra no necesita de la colocación de un espéculo. La toma de la muestra debe realizarse a las 35-37 semanas. En las embarazadas con factores de riesgo se recomienda toma de muestra a las 15 (para evitar el aborto), 28 (para evitar el parto prematuro) y 35-37 semanas (para evitar la infección perinatal). Los test rápidos no se recomiendan en la actualidad dada su baja sensibilidad.
Consideraciones Clínicas
- Manejo en mujeres con vaginitis bacteriana por EGB
Los fármacos de elección son ampicilina y clindamicina v.o.
- El tratamiento depende de la condición de riesgo de la mujer.
- Mujeres sin factores de riesgo:
- − Tratamiento sistémico oral con ampicilina (500 mg cada 6 horas x 7 días) o local con clindamicina (crema vaginal, 1 aplicación por 1 semana).
- − No se requiere tratamiento de la
- Mujeres con factores de riesgo:
- − Tratamiento sistémico oral con ampicilina (500 mg cada 6 horas x 7 días) o clindamicina (300 mg cada 8 horas x 7 días), asociado con tratamiento local con clindamicina (crema vaginal, 1 aplicación por 1 semana).
- − No se requiere tratamiento de la
- − Solicitar cultivo y Gram de
• Es útil el tratamiento intraparto en mujeres portadoras de EGB, en reducir el riesgo de sepsis neonatal?
El tratamiento intraparto de estas mujeres, disminuye el riesgo de sepsis neonatal por SGB, por lo que debe tratarse a todas las mujeres portadoras o con factores de riesgo.
Cada servicio debe evaluar la factibilidad de realizar cultivos para EGB. De no ser posible, el manejo puede basarse exclusivamente en la presencia de factores de riesgo, los que están presentes en un 70% de los niños que desarrollan la enfermedad y en un 25% del total de partos.
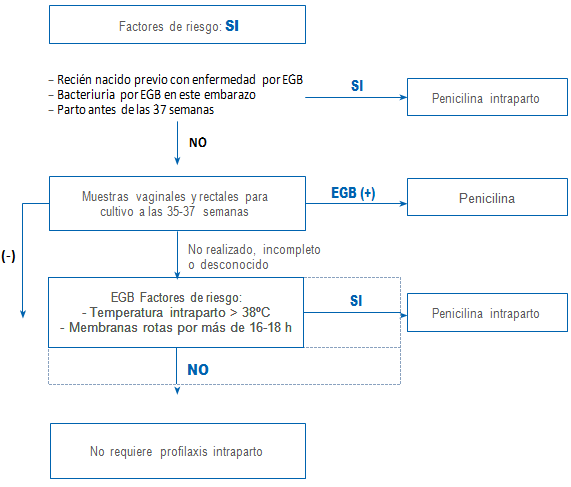
- Administrar profilaxis antibiótica intraparto SIEMPRE en los siguientes casos:
- Antecedentes de sepsis neonatal o muerte neonatal precoz por infección en embarazos previos.
- Bacteriuria asintomática a EGB en el embarazo actual.
- Trabajo de parto prematuro (dilatación cervical >3 cm, tocolisis fracasada, u otro signo de parto inminente).
- 1,2 y 3 no requieren la toma de cultivos porque SIEMPRE debe administrarse profilaxis intraparto.
- Si la norma local utiliza el cultivo de EGB a las 35-37 semanas
- Profilaxis antibiótica intraparto si el cultivo es positivo.
- No requiere tratamiento si el cultivo es negativo.
- Si la norma local NO utiliza el cultivo de EGB a las 35-37 semanas
- Administrar profilaxis intraparto siempre, si existe alguna de las condiciones descritas en A.
- Administrar profilaxis intraparto si durante el trabajo de parto se produce fiebre > 38 oC y rotura prematura de membranas por más de 16-18 horas.
- Si la mujer no tiene los factores de riesgo mencionados en A y B, no requiere profilaxis intraparto para EGB.
- Antibióticos utilizados en la profilaxis intraparto, en orden de preferencia:
- Penicilina sódica 5 millones iv de carga, luego 2 millones iv cada 4 horas hasta el parto.
- Ampicilina 2 gr iv de carga, luego 1 gr iv cada 4 horas hasta el parto.
- Eritromicina 500 mg iv cada 6 horas hasta el parto.
- Clindamicina 900 mg iv cada 8 horas hasta el parto.
Recordar que la profilaxis es sólo durante el trabajo de parto. No se justifica administrar antibióticos antes del inicio del trabajo de parto (riesgo de recurrencia y resistencia), ni después de ocurrido el nacimiento. La cesárea de rutina no reduce el riesgo de infección neonatal
Tabla 2: Administración de antibióticos para la profilaxis intraparto de la enfermedad neonatal por estreptococo del grupo B
|
Esquemas sugeridos |
|
• Penicilina sódica 5 mill endovenoso, luego 2 mill cada 4 horas, hasta la resolución del parto. • Ampicilina 2 gr endovenoso, luego 1 gr cada 4 horas, hasta la resolución del parto. Esquemas alternativos • Clindamicina 900 mg endovenoso cada 8 horas, hasta la resolución del parto. • Eritromicina 500 mg endovenoso cada 6 horas, hasta la resolución del parto. |
1.3. Vaginitis por Trichomona Vaginalis
Es producida por el protozoo Trichomona vaginalis (TV), que puede infectar el aparato genitourinario de hombres y mujeres. Es una enfermedad de transmisión sexual. En la mujer causa un cuadro vaginal inflamatorio caracterizado por flujo vaginal verdoso, ardor, prurito y disuria.
El diagnóstico se realiza ante la presencia de:
- Descarga vaginal purulenta, verdosa o cremosa.
- Ardor, dolor vaginal, prurito y disuria.
- Eritema vaginal, cérvix inflamatorio.
- Observación de TV en el examen al fresco o Pap.
Las complicaciones obstétricas asociadas a la infección por TV son parto prematuro y bajo peso de nacimiento.
Consideraciones Clínicas
- Tratamiento de la TV
El tratamiento de elección es metronidazol y tinidazol.
- − Se aconseja tratamiento a la pareja y abstinencia sexual durante el tratamiento
- − Tratamiento farmacológico:
> Metronidazol 2 gr oral x 1 dosis.
> Tinidazol 2 gr x 1 dosis.
> Metronidazol 250 mg oral cada 12 horas x 7 días.
> El uso de metronidazol durante el primer trimestre del embarazo no se ha asociado con anomalías fetales. Alternativa, clotrimazol óvulos de 100 mg por 6 días.
• El tratamiento de la TV reduce el riesgo de parto prematuro?
El tratamiento de la TV puede incluso incrementar la incidencia de parto prematuro. Se postula que la muerte del parásito, liberaría gran respuesta inflamatoria y un virus de RNA, albergado en la T. vaginalis, que aumentaría el parto prematuro. El tamizaje y tratamiento de la tricomoniasis asintomática no se recomienda, por no relacionarse con parto prematuro. TV incrementa el riesgo de infección por VIH y su tratamiento permite disminuir la transmisión vertical.
1.4 Vulvovaginitis micótica
La infección por hongos afecta frecuentemente a la embarazada, produciendo un cuadro caracterizado por flujo vaginal blanco y prurito intenso. El agente causal más frecuente es la Candida albicans, el cual coloniza el 30% de las embarazadas, mientras que la infección sintomática (vulvovaginitis micótica), tiene una frecuencia promedio de un 10-15%.
Tabla 3: Diagnóstico de la vulvovaginitis micótica
|
• Flujo vaginal blanco o cremoso, con grumos. • Prurito muy intenso. • Eritema vaginal y vulvar. Puede haber lesiones producidas por grataje y sobreinfecciones. • Puede aparecer disuria y dispareunia. • Observación microscópica de hongos en una preparación fresca de secreciones vaginales tratada con hidróxido de potasio al 10%. |
La infección vaginal por candida albicans, no se asocia con un aumento de las complicaciones obstétricas. En raras ocasiones el recién nacido desarrolla una infección micótica, de preferencia en la piel y cavidad oral. La característica más importante de la enfermedad es la intensidad de la sintomatología que produce. Si el cuadro es persistente o recurrente, deben descartarse condiciones subyacentes tales como: diabetes, inmunodepresión y administración concurrente de antibióticos.
Consideraciones Clínicas
- Cuál es el manejo de la vulvovaginitis micótica durante el embarazo?
El tratamiento puede ser tópico u oral.
Tratamiento antifúngico. Tópico (intravaginal profundo y sobre la piel vulvar) u oral
- Clotrimazol, 1 óvulo vaginal (100 mg) en la noche por 6 días; crema 2 veces al día por 6 días.
- Nistatina, 1 óvulo vaginal (100.000 UI) cada 12 horas por 6 días; ungüento 2 veces al día por 6 días.
- Fluconazol, 1 cápsula (150 mg) por una vez.
- Clotrimazol 1 óvulo vaginal de 500 mg en la noche por 1 vez.
- Otras alternativas: miconazol, butoconazol, y otras.
- Durante el primer trimestre, preferir clotrimazol, nistatina y miconazol ya que se han utilizado por muchos años, sin que exista evidencia de teratogénesis.
En la candidiasis recurrente, se aconseja tratamiento a la pareja y abstinencia sexual durante el tratamiento.
A. Infección por Chlamydia Trachomatis
Chlamydia trachomatis (CT) es una causa frecuente de enfermedad en hombres y mujeres. Cuando infecta el tracto genital, puede transmitirse sexualmente y producir infecciones del tracto genital bajo, enfermedad inflamatoria pélvica, infertilidad conyugal, conjuntivitis neonatal y neumonía del recién nacido.
La frecuencia en nuestro medio es: rotura prematura de membranas de pretérmino 3.8%, parto prematuro con membranas intactas 4,8%, embarazadas de Alto Riesgo 5.9%.
CT tiene varios serotipos. Los serotipos D hasta K causan infecciones urogenitales. En Chile el más frecuente es el E. Este serotipo causa generalmente infecciones asintomáticas. Esto explicaría su mayor diseminación en la población.
Diagnóstico
Sospechar cuando se constata cervicitis mucopurulenta y en mujeres con riesgo de ITS. Estudiar gonococo en forma simultánea.
Muestra endocervical (1 a 3)
- Inmunofluorescencia directa (IFD).
- Ensayos inmunoenzimáticos (Elisa).
- Cultivo celular (celulas McCoy).
- Reacción de polimerasa en cadena.
Complicaciones Obstétricas
Actualmente se acepta que CT produce aborto retenido y parto prematuro. Al menos la mitad de los recién nacidos expuestos a una infección materna por CT pueden colonizarse. Un tercio del ellos desarrolla conjuntivitis y un 10% puede padecer neumonia por CT en los siguientes 3 meses.
Consideraciones Clínicas
- Cómo se maneja la infección por CT durante el embarazo?
El tratamiento de elección es la Azitromicina.
Se aconseja tratamiento a la pareja y abstinencia sexual durante el tratamiento.
Tabla 4: Terapia antibiótica para Chlamydia trachomatis, en orden de preferencia
|
• Azitromicina 1 gramo oral x 1 vez. • Amoxicilina 500 mg oral cada 8 horas x 7 días. • Eritromicina (base) 500 mg oral cada 6 horas x 7 días. |
B.Infección por Neisseria Gonorrhoeae (NG)
Es una enfermedad que se transmite sexualmente con una elevada tasa de contagio. La gonorrea afecta primariamente el tracto genitourinario de hombres y mujeres. En la mujer se localiza de preferencia en el canal cervical en forma asintomática.
Tabla 5: Diagnóstico gonorrea en la mujer
|
• Sospechar en mujeres de alto riesgo de ITS (contacto de un caso, presencia de otras infecciones de riesgo, múltiples parejas sexuales y otras) e infección vaginal recurrente. • Flujo vaginal purulento verdoso, resistente a tratamiento habitual. • Cervicitis mucopurulenta. • Descarga uretral purulenta (exprimir si hay duda). • Disuria. |
Diagnóstico microbiológico:
- Cultivo en medio de Thayer – Martin.
- Tinción de Gram que muestra diplococos gram negativos intracelulares (sensibilidad de sólo 60%).
Complicaciones obstétricas
La presencia del gonococo en el tracto genital inferior, aumenta 2 veces el riesgo de trabajo de parto prematuro y rotura de membranas de pretérmino. Además, las mujeres portadoras pueden transmitir el microorganismo al recién nacido, favoreciendo la instalación de una oftalmopatía que puede conducir a la ceguera.
Consideraciones clínicas
- Manejo de la infección por NG durante el embarazo
El tratamiento de elección es la ceftriaxona IM.
Se aconseja tratamiento a la pareja y abstinencia sexual durante el tratamiento Tratamiento farmacológico durante el embarazo
- Ceftriaxona, 250 mg IM por una vez.
- Cefotaxima, 500 mg, IM por una vez.
- Ceftizoxima, 500 mg, IM por una vez.
El gonococo ha adquirido una importante resistencia a las penicilinas, por lo que se desaconseja su uso.
1.5. Micoplasmas genitales
Son las bacterias más pequeñas descritas. No tienen pared celular, se rompen con la tinción de Gram y son resistentes a antibióticos b-lactámicos. Especies: Mycoplasma: M.hominis, M. genitalium Ureaplasma spp: U.urealyticum, U. parvum
Frecuencia
M. hominis se aisla en el 60% de mujeres con VB y en 10 a 15% de mujeres con microbiota normal, mientras que la colonización por ureaplasmas varía entre 40% y 80%.
Diagnóstico
Es habitualmente por cultivo. Las muestras de secreción vaginal tienen un mejor rendimiento que las del endocervix. El cultivo de los micoplasmas genitales incluye una combinación de caldos diferenciales y agar A7. La PCR con alta sensibilidad y especificidad se usa en muestras respiratorias de prematuros. M. genitalium crece lentamente en cultivos y se prefiere la PCR como método diagnóstico.
Complicaciones obstétricas
Su aislamiento a nivel vaginal se relaciona con parto prematuro. La infección intraamniótica por esta bacteria se asocia con enfermedad crónica pulmonar en niños prematuros menores de 1500 g de peso al nacer. M. hominis es componente de la microbiota de VB y produce signos inflamatorios y se asocia con parto prematuro. M. genitalium se ha asociado con cervicitis mucupurulenta. No se ha demostrado que se relacione con parto prematuro.
Consideraciones Clínicas
- Cuál es el tratamientode la infección por Micoplasma genitalis durante el embarazo?
- . Ureaplasma: Eritromicina (base): 500 mg oral cada 6 horas x 7 días.
Mycoplasma hominis: Clindamicina: 300 mg oral cada 6 horas x 7 días.
- El tratamiento de la infección por ureaplasma spp reduce el riesgo de prematurez? No se ha observado reducción del riesgo de parto prematuro con el uso de antibióticos.
- El tamizaje y tratamiento posterior de la infección por ureaplasma spp no reduce el nacimiento prematuro, por lo que no se recomienda el tamizaje universal.
2. INFECCIONES URINARIAS
Generalidades
La infección del tracto urinario (ITU), es la enfermedad infecciosa más frecuente durante el embarazo. Existen tres formas de presentación: la bacteriura asintomática (BA), la cistitis o infección urinaria baja (IUB) y la pielonefritis aguda (PNA) o infección urinaria alta.
Diagnóstico
El diagnóstico se hace por los síntomas y signos y se ratifica por el sedimento de orina y el urocultivo. El urocultivo se obtiene de la muestra de segundo chorro de orina de la mañana.
Condiciones que favorecen la aparición de ITU: La mujer desarrolla fácilmente ITU porque el meato uretral tiene cercanía anatómica con recto y vagina, con exposición a la colonización de patógenos urinarios provenientes de la flora rectal, Escherichia coli, Klebsiella pneumoniae y Proteus mirabilis. El elevado nivel de progesterona existente relaja la fibra muscular lisa, contribuyendo al hidrouréter e hidronefrosis del embarazo. Además relaja la vejiga, aumenta el residuo urinario y disminuye su vaciamiento.
Factores de riesgo:
- Historia de infecciones del tracto urinario.
- Episodios repetidos de infección cervicovaginal (3 o más).
- Historia de abortos de segundo trimestre o parto prematuro de causa no precisada.
- Existencia de litiasis o malformación de la vía urinaria.
- Actividad sexual frecuente.
- Bajas condiciones socioeconómicas y culturales.
- Diabetes durante el embarazo.
Se distinguen 3 tipos de presentación de las infecciones urinarias:
2.1 Bacteriuria asintomática (BA)
Se define como la infección de la vía urinaria baja sin sintomatología y urocultivo con recuento de colonias > de 100.000/ml. Su incidencia es 3 a 10%.
2.2 Infección urinaria baja o cistitis (IUB)
Corresponde a la infección de la vía urinaria baja con polaquiuria, disuria, malestar pélvico de grado variable, habitualmente afebril y con orinas turbias de mal olor, asociado a un sedimento de orina (leucocitos aumentados, bacterias presentes y nitritos positivos) y el cultivo de orina con recuento de colonias >100.000/mL. Puede haber hematuria. Se presenta en un 2-6% de los embarazos.
2.3 Pielonefritis aguda (PNA)
Corresponde a la forma más grave de ITU y se constituye la causa de muerte materna por infección más frecuente de los países desarrollados, debido a las complicaciones médicas que la acompañan. Se presenta en el 2 a 3% de los embarazos y representa el 5% de las hospitalizaciones en una Unidad de Alto Riesgo Obstétrico.
El cuadro clínico se caracteriza por la presencia de fiebre hasta 39-40ºC, calofríos intensos, dolor en región costolumbar y molestias urinarias. El diagnóstico se realiza en base a un cuadro clínico compatible y ratificado por el urocultivo.
El útero grávido al crecer comprime y dilata ambos uréteres. El derecho se dilata más por la mayor compresión ejercida por el útero rotado hacia la derecha. Como consecuencia, la orina permanece en el tracto urinario superior más tiempo que lo habitual favoreciendo la infección de los riñones. Es más común durante la segunda mitad del embarazo, presumiblemente por el incremento de la obstrucción ureteral y estasia urinaria en la medida que el embarazo progresa. Usualmente es unilateral, predominando en el lado derecho como resultado de la dextrorotación uterina.
Consideraciones Clínicas
- ¿Cuáles son las complicaciones obstétricas asociadas a la presencia de infecciones urinarias durante el embarazo?
Se asocian a parto prematuro y complicaciones sépticas maternas.
La BA no tratada evoluciona en un tercio de los casos a PNA. Se relaciona además, con prematurez y RN de bajo peso de nacimiento. La infección urinaria baja no manejada puede originar PNA si no se trata. Los episodios repetidos y mal tratados pueden producir daño renal. La pielonefritis aguda se asocia con prematurez en el 7%.
Manejo de las infecciones urinarias durante el embarazo
Se debe realizar tratamiento antibiótico con el fin de prevenir las complicaciones sépticas, además del aborto y parto prematuro.
En el embarazo, se usan antimicrobianos beta lactámicos y especialmente cefalosporinas. La nitrofurantoína tiene un uso más restringido, debido al riesgo potencial, extremadamente bajo de anemia hemolítica en poblaciones susceptibles, cuando se utiliza cercana al término. La ampicilina no debiera utilizarse, porque su uso masivo ha generado tasas inaceptables de resistencia. Se reserva la ampicilina para el tratamiento de la BA e IUB por Streptoccus agalactiae.
Manejo de BA:
- Cefradina (cefalosporina de primera generación) oral 500 mg cada 6 horas x día x 7-10 días.
- Cuando no se dispone, usar nitrofurantoína 100 mg c/8h x 7-10 días.
- Hacer cultivo control a los 2-3 días de terminado el antibiótico. Con resistencia, se usará el antibiótico según antibiograma. Con fracaso del tratamiento y bacteria sensible, repetir la terapia con cefradina o nitrofurantoína en las dosis señaladas y por 10 días. Con nuevo fracaso, usar gentamicina intramuscular 160 mg (2 a 4 mg x kg día) por 7 días.
Manejo de infección urinaria baja:
- Con síntomas y sedimento urinario alterado, se comenzará tratamiento con cefalosporinas de 1ª generación. Se recomienda cefradina oral 500 mg cada 6 horas x día x 10 a 12 días. Cuando no se dispone, usar nitrofurantoína 100 mg c/8 horas x día x 10 a 12 días.
- Con resistencia, se usará el antibiótico según antibiograma. Se hará cultivo control a los 2 y 28 días de terminado el antibiótico. Si es positivo, se tratará nuevamente según antibiograma.
- Con fracaso del tratamiento gentamicina intramuscular 160 mg (2 a 4 mg x kg día) por 8 a 10 días. Tratar infecciones cérvicovaginales si están presentes.
- Se dejará tratamiento antibiótico profiláctico después de la segunda infección tratada, luego de curación microbiológica, con nitrofurantoína 100 mg/día o cefradina 500 mg/día hasta las 36 semanas.
Manejo de pielonefritis aguda:
- Hospitalización y realización de los siguientes exámenes de urgencia: hemograma, sedimento de orina y urocultivo. En casos graves solicitar hemocultivo, gases en sangre, pruebas hepáticas y electrolitograma.
- El tratamiento adecuado permite disminuir los fracasos en la erradicación del agente etiológico, evitando las complicaciones médicas, como asimismo los costos elevados y la prolongación de la hospitalización.
- Con tinción de Gram positiva y piocitos en el examen microscópico de orina, se inicia tratamiento de inmediato con cefradina o cefazolina sin esperar el urocultivo:
- − Cefazolina: 1 g cada 6 horas intravenoso x día x 3 a 7 días. Luego se sigue con cefradina oral 500 mg cada 6h oral x día hasta completar 14 días.
- − Las cefalosporinas de segunda generación (cefuroxima) son de mayor costo pero son más eficientes y de menor resistencia bacteriana: cefuroxima 750 mg cada 8h intravenoso x día por 3 a 7 días (bacteremia). Luego 250 mg cada 12 horas oral x día hasta completar 14 días.
- Con resistencia o fracaso clínico (persistencia de los síntomas y signos al cuarto día), se indican en este orden, ceftriaxona o cefotaxima (cefalosporinas de tercera generación) o gentamicina (con creatinina <de 1.4 mg/dl).
- − Ceftriaxona: 1 g cada 12 horas intravenoso x día x 3 a 7 días, luego cefixima 400 mg oral x día hasta completar 12 días.
- − Cefotaxima: 1 g cada 6 horas intravenoso x día x 3 a 7 días, luego cefixima 400 mg oral x día hasta completar 12 días.
- − Gentamicina (2 a 4 mg x kg día) 160 mg intravenoso x 3 días, luego 160 mg intramuscular por 7 días.
- La resistencia de E.coli a los antimicrobianos en la PNA es: ampicilina 39%, trimetoprim sulfametoxazol 31%, cefradina 14% y cefuroxima 1%. (Ovalle y cols)
- Con la terapia intravenosa, el 85% de las mujeres se hace afebril en 48 horas y el 97%, en 96 horas.
- Solicitar cultivo control a los 2 y 28 días de terminado el antibiótico. Si el cultivo es positivo, se tratará nuevamente según antibiograma.
- Tratamiento antibiótico profiláctico sólo después de la segunda infección tratada, luego de curación microbiológica, como se señaló anteriormente.
- Criterios de evaluación del tratamiento realizado:
- Curación o erradicación: desaparición del patógeno inicial en el urocultivo a las 48 horas de finalizado el tratamiento y a los 28 días.
- Fracaso o persistencia de la infección: persistencia del patógeno inicial en el urocultivo a las 48 horas de finalizado el tratamiento.
- Reinfección: desaparición del patógeno inicial en el urocultivo a las 48 horas de finalizado el tratamiento y urocultivo positivo a los 28 días a la misma bacteria.
- Recurrencia: aparición de nuevo episodio de ITU luego de urocultivo (-) a los 28 días de terminado el tratamiento, a la misma bacteria u otra de especie diferente.
Frente a repetición de ITU solicitar ecografía renal (observar litiasis, malformación renal o absceso).
Restricciones para el uso de ciertos antibióticos durante el embarazo
Tetraciclinas son teratogénicas. Ejercen acción sobre la coloración y crecimiento de la dentadura por lo que no se usan durante el embarazo.
Quinolonas producen alteración del cartílago de crecimiento en animales, aunque esto no se ha observado en fetos humanos expuestos inadvertidamente.
Trimetropin sulfa. No deben usarse en el primer trimestre.
Aminoglucósidos pueden ser nefrotóxicos en dosis > de 4mg/kg peso día y por más de 15 días. Dado que su utilización considera dosis menores y por 10 días o menos, su administración con creatinina <de 1.4 mg/dl no está contraindicada.
Esquema de prevención para la enfermedad neonatal por estreptococo grupo B mediante la pesquisa rutinaria a las 35-37 semanas de gestación (Center for disease control, 1996)
3. INFECCIONES DE TRASMISIÓN VERTICAL
La importancia de este tema, recae en que el manejo adecuado de las gestantes con Sífilis o VIH ha demostrado, según la evidencia científica disponible, ser la intervención más costo efectiva para evitar la transmisión de estas patologías a los recién nacidos.
3.1. VIH (VIRUS DE INMUNODEFICIENCIA HUMANA)
El VIH se transmite entre las personas a través del contacto sexual, sanguíneo y vertical (de una gestante que vive con el VIH a sus hijos/ as durante la gestación, parto o lactancia) y que afecta el desempeño del sistema inmunológico del ser humano.
La transmisión vertical del VIH, se produce en un 35% de los casos durante el embarazo y aproximadamente en un 65% durante el parto, por exposición del recién nacido a sangre materna, secreciones cervicovaginales o líquido amniótico. La lactancia materna agrega un riesgo adicional de 14% hasta 29%.
El diagnóstico de VIH en la embarazada y la aplicación del protocolo completo para la prevención de transmisión vertical, permiten reducir la tasa de transmisión de entre 13 a 48% hasta menos de 2%.
¿A quién se debe aplicar el estudio de tamizaje?
- Acceso universal del test de VIH a gestantes sin diagnóstico conocido de VIH en el primer control prenatal. En caso de denegación, continuar orientando, educando y ofreciendo el examen en los controles posteriores, con énfasis en los beneficios del protocolo de prevención de transmisión vertical.
- Si el resultado del examen es negativo, se debe repetir entre la semana 32-34 de gestación en aquellas mujeres que tengan mayor riesgo de adquirir el VIH: por antecedentes de abuso de alcohol o drogas, parejas nuevas durante la gestación o multiparejas (mujeres en situación de calle, trabajadoras sexuales y otras), portación de ella o de su pareja de Hepatitis B, Hepatitis C, Tuberculosis, Sífilis u otra ITS y en casos conocidos de serodiscordancia y su pareja sea VIH (+).
- En gestantes que ingresan en trabajo de parto con serología desconocida, se debe indicar test VIH urgente. Si éste resultara reactivo, aplicar de inmediato el protocolo de prevención de transmisión vertical, incluyendo suspensión de la lactancia hasta que se obtenga resultado de confirmación del ISP, para determinar conducta definitiva a seguir.
Manejo de las mujeres VIH (+)
Todas las gestantes con test VIH positivo deben ser derivadas en el sistema público, al Centro de Atención de VIH y a la Unidad de Alto Riesgo Obstétrico y a los especialistas correspondientes en el sistema privado.
- Aquella gestante con examen reactivo, obtenido desde la semana 20 en adelante, debe ser derivada de inmediato al médico tratante de VIH, sin esperar la confirmación del ISP para la aplicación del protocolo de terapia.
- Debe existir coordinación entre las diferentes instancias de atención de la gestante, en favor del bienestar del binomio madre-hijo(a).
¿Cuándo debe iniciarse el tratamiento?
- Iniciar Terapia antiretroviral (TAR) para la prevención de la transmisión vertical del VIH en embarazadas sin tratamiento previo, a partir de la semana 20 de gestación.
- La TAR debe iniciarse en la semana 14 cuando la Carga Viral es mayor de 100.000 copias/ mL.
- La TAR debe iniciarse de inmediato si la embarazada tiene criterios clínicos o inmunológicos de inicio de TAR.
- Si la seroconversión se produce durante la gestación, deberá iniciarse TAR de inmediato.
¿Cuáles son las características del seguimiento del tratamiento?
Se debe controlar la carga viral a las 6 semanas de iniciada TAR durante la gestación y posteriormente en forma mensual hasta la semana 34.
- Carga Viral de semana 34 de gestación, define la conducta obstétrica y TAR adicional al binomio mujer-hijo.
¿Cuál es el manejo del parto propuesto a toda embarazada VIH (+) sin terapia previa?
Si es posible deben tomarse muestras basales para CD4 y CV e iniciar inmediatamente Zidovudina endovenosa según esquema, más una dosis única de 200 mg de Nevirapina.
En estos casos la resolución del parto es por cesárea.
¿Cuál es la vía de parto recomendada para estas mujeres?
Indicar cesárea en las mujeres con infección por VIH sin TAR durante el embarazo, en aquellas que no tienen resultado de CV a la semana 34 o si ésta es > 1.000 copias/mL.
- Puede permitirse parto vaginal en mujeres con TAR desde las 24 semanas de gestación o antes, con CV < 1.000 copias/mL en la semana 34 y que además cumplan con las siguientes condiciones:
Edad gestacional mayor de 37 semanas, feto único en presentación cefálica, condiciones obstétricas favorables y atención por médico especialista.
- Evitar maniobras invasivas amniocentesis, biopsia de vellosidades coriales, monitorización interna, rotura artificial de membranas, parto instrumental (fórceps, espátulas).
Esquema farmacológico a indicar durante el trabajo de parto
- Evitar el uso de Metilergonovina si la mujer utiliza inhibidores de proteasa.
- Usar AZT de 200 mg/mL intravenoso intraparto:
- − Dosis de carga 2 mg/kg, a pasar en 1 hora, iniciar 4 horas antes de cirugía o inicio del trabajo de
- − Dosis de mantención: 1 mg/kg/hr., hasta la ligadura del cordón.
- En caso de no disponer de AZT de 200 mg/mL, se indica AZT/3TC (300-150 mg), al inicio del trabajo de parto o 4 horas antes de la cesárea programada, repetir cada 3 horas hasta la ligadura del cordón.
- Asociar Nevirapina en dosis de 200 mg por 1 vez antes de la cesárea, en caso de ausencia o inicio tardío de protocolo, y/o CV de semana 34 > 1.000 copias/mL
Sobre la lactancia materna:
Suspender la lactancia materna, en TODAS las mujeres VIH (+) confirmadas o en proceso de confirmación por el ISP, dado que los riesgos potenciales a los que se expone un RN hijo de mujer VIH (+), especialmente al calostro, superan ampliamente las desventajas de la suspensión de la lactancia materna.
- Prohibir SIEMPRE, la lactancia materna exclusiva o mixta en mujeres VIH (+) o en proceso de confirmación por el ISP, la alimentación por nodrizas y por leche proveniente de bancos de leche. Reemplazar por sustitutos de leche materna.
- Interrumpir la lactancia con Cabergolina 0,25 mg cada 12 hrs. Por dos días o Bromocriptina en dosis de 2,5 mg cada 12 horas por 7 – 10 días inmediatamente en el posparto.
3.2 SIFILIS
La Sífilis es una enfermedad sistémica causada por el Treponema pallidum, espiroqueta de reservorio humano exclusivo.
La evolución natural de la enfermedad tiene un curso variable, algunos de los infectados evolucionan espontáneamente hacia la recuperación total sin tratamiento, un porcentaje importante permanece en etapas latentes de la enfermedad, que se evidencia solamente con test serológicos reactivos/positivos. La enfermedad se manifiesta en etapas latentes (latente precoz y latente tardía) y etapas con signología clinica (Sífilis Primaria y Secundaria), pudiendo evolucionar en forma excepcional hacia la etapa destructiva (Sífilis Terciaria).
Riesgo de transmisión de la Sífilis durante la gestación:
- Sífilis primaria, secundaria y latente precoz (menos de un año de evolución) 75% a 95%.
- Sífilis latente tardía y terciaria (más de un año de evolución): 10 % a 35 %.
Si la gestante con Sífilis es tratada en forma oportuna y adecuada se evitará la enfermedad en el 100% de los recién nacidos.
Diagnóstico
- El tamizaje de Sífilis en gestantes, se realiza con exámenes no treponémicos en tres momentos de la gestación: al ingreso, a las 24 y entre las 32 y 34 semanas.
- Todo tamizaje que presente un resultado reactivo, debe ser confirmado con prueba reagínica (FTA-ABS, MHA-TP). Los laboratorios deben informar siempre al clínico la técnica utilizada.
Tratamiento
Toda gestante con serología reactiva para Sífilis debe recibir tratamiento con Penicilina benzatina en 2.400.000 UI por vía intramuscular, repitiendo semanalmente de acuerdo a etapificación de la enfermedad.
- La gestante alérgica a Penicilina debe recibir tratamiento con Eritromicina en dosis de acuerdo a etapificación de la enfermedad.
- Toda gestante mayor de 24 semanas con sospecha diagnóstica de Sífilis secundaria, debe ser derivada dentro de las 24 horas, para evaluación de la unidad feto placentaria y prevención de parto prematuro.
- Los contactos sexuales de la gestante deben ser estudiados y tratados siempre.
Debe realizarse seguimiento serológico con VDRL mensual hasta el parto, a la gestante para evaluar respuesta a tratamiento y detectar reinfecciones.
¿Cómo se realiza el diagnóstico en el recién nacido?
El diagnóstico de Sífilis congénita se realiza con el análisis de los antecedentes maternos, análisis de la serología neonatal, examen físico del niño/a y el resultado de exámenes radiológicos y de laboratorio.
- Ningún Recién Nacido debe ser dado de alta sin conocer el estado serológico para Sífilis de la madre.
Conclusión:
La importancia del tamizaje universal de VIH y Sífilis a toda embarazada, es la posibilidad de realizar el diagnóstico y tratamiento oportuno de estas patologías, lo que permitirá reducir la trasmisión vertical.
3.3 VIRUS HEPATITIS B y EMBARAZO
La hepatitis B durante el embarazo tiene implicancias tanto para la madre como para el hijo, debido a las consecuencias que tiene el embarazo sobre el curso de la enfermedad y también al riesgo de transmisión de la infección al recién nacido.
Pueden identificarse las siguientes situaciones:
Hepatitis aguda por virus B durante el embarazo: El diagnóstico de la hepatitis B aguda durante el embarazo, es similar al de la mujer no embarazada. El tratamiento es de soporte general y el tratamiento antiviral no es necesario en la gran mayoría de los casos. No se requiere interrupción del embarazo. La posibilidad de transmisión vertical aumenta hasta un 60% cuando la hepatitis B aguda se presenta durante el tercer trimestre de la gestación.
Hepatitis crónica por virus B en la mujer embarazada: El embarazo es generalmente bien tolerado en las mujeres con hepatitis B crónica, que no tienen cirrosis descompensada. El embarazo no se considera contraindicado en estas mujeres.
El tratamiento de la hepatitis B, en una mujer en período fértil, requiere discutir la posibilidad y planes de embarazo. En general, si la mujer tiene una enfermedad leve, tiene la opción de elegir embarazarse y diferir la terapia antiviral o de considerar un tratamiento con peginterferón antes del embarazo. Si se decide terapia antiviral, el antiviral de elección es tenofovir (droga en categoría B de uso en embarazo). Si una mujer en tratamiento antiviral oral se embaraza, se debe discutir con la mujer los riesgos y beneficios de las siguientes opciones: mantener tratamiento (si es tenofovir), cambiar a tenofovir (si está recibiendo otro antiviral) o de suspender terapia durante el primer trimestre (lo que conlleva un riesgo de reactivación de la hepatitis). El peginterferón es categoría C, pero no se recomienda su uso durante el embarazo.
Prevención de la transmisión vertical
La transmisión vertical, de la mujer infectada con hepatitis B (HBeAg positivo) al hijo, puede ser de hasta 90% en ausencia de profilaxis.
Los pilares de la prevención de la transmisión vertical de la hepatitis B, son el tamizaje universal de la hepatitis B en mujeres embarazadas y la administración de inmunoglobulina de hepatitis B (IgHB) seguida de una vacunación (3 dosis) al recién nacido. Esta estrategia logra reducir de un 90% a un 5-10% la posibilidad de transmisión vertical.
La IgHB debe administrarse por vía intramuscular antes de las 12 horas de edad, en dosis de 0,5 mL por una vez. La primera dosis de la vacuna contra la hepatitis B debe administrarse también antes de las 12 horas de edad en un sitio diferente al usado para la inyección de IgHB. La segunda dosis debe administrarse al mes y la tercera dosis a los 6 meses de edad.
Uso de antivirales orales para prevenir la transmisión vertical
Se debe hacer énfasis en que la prevención de la transmisión vertical de la hepatitis B, se realiza primariamente con la administración de la IgHB y la vacunación en forma precoz a todo recién nacido de una mujer con HBsAg positivo. Dado que aún con esta estrategia queda un 5 a 10% de riesgo de transmisión, se ha estudiado el uso de profilaxis durante el tercer trimestre con antivirales. Dado que la carga viral elevada es uno de los principales factores de riesgo para la transmisión, la situación de mayor riesgo se da en mujeres en fase de inmunotolerancia, que habitualmente tienen cargas virales mayores. Se debe recordar que esta situación no es la más frecuente en nuestro país.
La elección del análogo de nucleósido a emplear, debe considerar su categoría de riesgo en el embarazo, la experiencia existente y la posibilidad de desarrollo de resistencia si se planifica un uso prolongado del antiviral. Los antivirales contra hepatitis B están en categoría C, excepto el tenofovir y la telbivudina, que son categoría B (más seguros).
Lactancia
La lactancia materna no aumenta el riesgo de transmisión del virus de la madre al hijo que ha recibido IgHB y vacuna al nacer. No se requiere completar la serie de vacunas para iniciar la lactancia. Se aconseja aumentar los cuidados para prevenir sangrado por agrietamiento del pezón. Hay poca experiencia de uso de antivirales orales durante la lactancia, pero los datos disponibles sugieren que el tenofovir se encuentra en concentraciones menores al 2% de la dosis teórica para un recién nacido, con mala absorción oral, por lo que probablemente su uso sea seguro.
Seguimiento del recién nacido
El riesgo de desarrollar una hepatitis B crónica en un niño en que se han seguido las indicaciones anteriores es bajo. Sin embargo, se recomienda realizar una determinación de HBsAg a los 12 meses de edad, ya que las determinaciones más precoces corren el riesgo de detectar falsos positivos.
Resumen de las recomendaciones en VHB y embarazo
Se recomienda el tamizaje universal de hepatitis B a todas las mujeres embarazadas durante el primer trimestre del embarazo.
No se recomienda cambiar la vía del parto en mujeres embarazadas para disminuir la posibilidad de transmisión vertical, pero sí evitar procedimientos invasivos como amniocentesis.
La prevención de la transmisión vertical se realiza administrando IgHB 0,5 mL im al recién nacido de toda mujer con HBsAg positivo antes de las 12 hrs del parto, simultáneamente con la primera dosis de vacuna de hepatitis B en un sitio diferente.
Se recomienda la determinación de carga viral en mujeres embarazadas con hepatitis crónica por VHB entre las 28-30 semanas de embarazo, para poder evaluar la necesidad potencial de terapia antiviral en el tercer trimestre. En mujeres con HBsAg y HBeAg que además tengan alta carga viral (mayor de 100.000.000 IU/mL) pueden beneficiarse de uso de tenofovir 300 mg/d comenzando 6 a 8 semanas antes de la fecha probable del parto.
- La lactancia materna no se debe suspender en las mujeres con hepatitis B si el hijo recibió profilaxis con IgHB y vacuna al nacer.
- El uso de tenofovir es seguro durante la lactancia materna.
- A los recién nacidos de una mujer HBsAg positivo se debe determinar HBsAg al año de edad, independientemente de haber recibido profilaxis.
3.4 EMBARAZO Y ENFERMEDAD DE CHAGAS
Antecedentes
El agente etiológico es el protozoo Trypanosoma cruzi (T. cruzi), se encuentra en el vector Triatoma infestans, que tiene presencia endémica en 21 países de América. Sin embargo, actualmente los casos humanos también están presentes en otros continentes debido a las migraciones, luego hoy la enfermedad de Chagas es una causa de morbilidad y mortalidad a nivel mundial.
La prevalencia estimada de enfermedad de Chagas para mujeres en edad fértil es 0,52% a nivel nacional, pero para zonas endémicas se ha reportado prevalencias entre 1 y 10% para este grupo, cifra que puede llegar hasta 20% en algunas regiones del norte del país.
Las medidas de detección y diagnóstico de la enfermedad de Chagas en las gestantes, y de tratamiento a estas mujeres, una vez concluido el período de lactancia, están ampliamente justificadas pues se ha comprobado la mayor tolerancia y eficacia del tratamiento farmacológico antichagásico en las edades tempranas de la vida y en los casos de infecciones recientes.
Transmisión madre-hijo
La transmisión de la infección al feto ocurre por vía hematógena, cuando el T. cruzi alcanza la circulación fetal vía transplacentaria, principalmente a través del seno marginal. Como resultado de ello, se produce una placentitis (focos inflamatorios agudos y crónicos), áreas de necrosis, células gigantes y parasitismo de células trofoblásticas, vellositis e intervellositis de distinta intensidad, corioamnionitis y funiculitis.
En Chile, la prevalencia observada de la transmisión madre-hijo varía de un 3 a un 10%. No obstante, es necesario tener presente que la infección del hijo puede producirse durante la evolución de la etapa aguda o crónica de la infección por T. cruzi materna.
La infección por T. cruzi puede provocar aborto, mortinato y parto prematuro. Puede existir infección congénita en embarazos sucesivos o aislados, y en los casos de gemelos infectarse uno, ambos o ninguno. Incluso se ha documentado la transmisión transplacentaria en segunda generación (desde la abuela a la mujer y de la mujer a sus hijos).
La Estrategia de prevención de la enfermedad de Chagas congénita Objetivo:
Pesquisar y tratar oportunamente los recién nacidos con infección por T. cruzi, hijos de mujeres con enfermedad de Chagas.
Para el logro del dicho objetivo se debe realizar la confirmación diagnóstica oportuna de la infección por T. cruzi en las gestantes.
Diagnóstico de la infección por T. cruzi en la gestante
El tamizaje de la infección por T. cruzi, se realiza a través de la prueba serológica IgG anti-T. cruzi (técnica ELISA), establecida en el flujograma de diagnóstico de laboratorio que indica la normativa vigente, el cual se incluirá en el conjunto de pruebas de laboratorio que se realizan al ingreso del control prenatal de las gestantes residentes en la zona endémica del país, es decir, desde la Región de Arica y Parinacota hasta la Región de O`Higgins, incluida la Región Metropolitana.
En las gestantes residentes en zonas no endémicas, no es obligatorio el tamizaje. Sin embargo, el médico y/o la matrona (ón) deberán realizar la anamnesis dirigida, la cual se refiere a la búsqueda activa de la población diana, mediante la identificación de uno o más factores de riesgo personal y familiar o antecedentes clínicos.
Los factores de riesgo que se buscan en esta anamnesis son los siguientes: De la historia personal:
- Haber vivido, anterior o recientemente, habitual o esporádicamente en regiones geográficas de alta endemia donde existe o haya existido la infestación vectorial domiciliaria, tenga o no antecedentes clínicos compatibles con enfermedad de Chagas aguda, o contacto real o presuntivo con vector.
En Chile el área endémica va desde la Región de Arica y Parinacota hasta la Región de O’Higgins, incluida la Región Metropolitana.
- Haber estado expuesto o en contacto real o presuntivo con el vector en cualquier momento de su vida (presencia del triatomino en el domicilio, peri domicilio o haber sido picado por éste).
- Haber trabajado en forma esporádica en zonas rurales de la zona endémica, especialmente faenas mineras o agrícolas.
- Haber tenido o tener síntomas o signos clínicos compatibles con infección por T. cruzi (cardiopatía, megacolon, megaesófago).
- Haber recibido transfusiones de sangre o hemoderivados o haber sido trasplantada, antes del año 1996 en cualquier parte de Chile, o antes del 2008 desde la Región del Maule al sur. Se incluye el haber recibido transfusiones de sangre en el extranjero, en países endémicos.
- Tener antecedentes de abortos a repetición, mortinatos, niños de bajo peso y prematuros.
- Ser hija o nieta de mujer con enfermedad de Chagas en cualquiera de sus etapas de evolución (aún sin haber manifestado síntomas).
- Haber ingerido alimentos sospechosos de estar contaminados con deyecciones del vector (vinchucas) en países americanos, donde se haya reportado casos por infección adquirida vía alimentaria (ejemplo Brasil, Venezuela, Perú, Colombia).
- Presentar antecedentes de uso de drogas inyectables.
De la historia familiar:
- Tener abuela, mujer o hermanos maternos positivos para la infección por T. cruzi.
- Tener otros familiares consanguíneos directos cercanos como padres, hermanos, primos tíos, hijos, con o sin antecedentes clínicos compatibles con enfermedad de Chagas aguda o crónica, que hayan tenido niños de bajo peso de nacimiento, que hayan presentado hepatoesplenomegalia, portadores de epilepsia no convencional, o bien, Síndrome TORCH en período neonatal.
- Tener familiares que residen en zona endémica, con antecedentes de presencia del vector intradomiciliario en caso de haber compartido la misma vivienda.
Si de la anamnesis realizada, resulta la pesquisa de uno o más factores de riesgo, el profesional solicitará la prueba de tamizaje de laboratorio (IgG anti –T. cruzi).
En caso de que el tamizaje resulte no reactivo, se deben realizar las siguientes acciones:
- El resultado se registra en la historia clínica y en la agenda salud de la mujer-control prenatal.
- Se entrega copia del resultado y se informa a la mujer para su registro personal.
En caso de que el tamizaje resulte reactivo, se debe continuar el algoritmo de confirmación diagnóstica, según lo indica la Norma General Técnica (Anexo Nº 1). El ISP o los Laboratorios reconocidos por éste son los encargados de la confirmación diagnóstica.
En caso de confirmar el diagnóstico, las acciones a seguir serán las siguientes:
- Información y consejería a la gestante de su condición de infección por T. cruzi y de los pasos a seguir.
- Notificación ENO en el formulario correspondiente.
- Derivación al nivel secundario de atención de Alto Riesgo Obstétrico para su seguimiento de especialidad.
Consideraciones relevantes:
Si la embarazada llega al momento del parto, presenta un aborto a cualquier edad gestacional, o si proviene de un traslado de cualquier otro establecimiento, y no cuenta con la anamnesis realizada o el tamizaje indicado, se debe efectuar uno u otro, según corresponda, durante su hospitalización en la maternidad.
Manejo de la gestante
La gestante con diagnóstico confirmado de infección por T. cruzi continúa su seguimiento médico en el nivel secundario (policlínico ARO) del establecimiento correspondiente, y con el referente clínico de Chagas definido por el Servicio de Salud. La gestante será sujeto de las siguientes atenciones:
- Educación, orientación e información respecto del diagnóstico, los posibles riesgos, los cuidados de la mujer y del hijo (a), y el seguimiento posterior al puerperio y la lactancia para evaluación del eventual tratamiento antiparasitario.
- Anamnesis y examen clínico dirigido para la pesquisa de complicaciones.
- Electrocardiograma (ECG), el que se complementará con el estudio ecocardiográfico cuando se considere indicado.
La detección de cardiopatías durante la gestación es de especial importancia debido a las posibles repercusiones durante el tercer trimestre y el parto.
Finalmente, es imprescindible mantener los registros necesarios de estas atenciones en la ficha clínica y la agenda salud de la mujer- control prenatal.
Conducta intra-parto y posparto o aborto
Debido a la contraindicación absoluta de farmacoterapia durante la gestación y la lactancia, se recomienda el seguimiento sistemático bajo control de las puérperas nodrizas, para que al momento de finalizar la lactancia, se pueda dar inicio al tratamiento farmacológico, si corresponde.
|
El diagnóstico de infección crónica por T. cruzi en toda mujer en edad fértil, obliga al estudio y evaluación de toda su descendencia consanguínea. |
Lactancia
La infección por T. cruzi de la mujer no constituye una contraindicación para la lactancia.
Diagnóstico y tratamiento de la infección por T. cruzi en el recién nacido, hijo de mujer con enfermedad de Chagas
Objetivo
Realizar la detección y tratamiento oportuno de la infección trasplacentaria por T. cruzi en el recién nacido, hijo de mujer con enfermedad de Chagas.
Considerando que la mayoría de los niños con infección por T. cruzi son asintomáticos, todos los recién nacidos, hijos de mujer con enfermedad de Chagas deben ser estudiados al momento del parto, para descartar una eventual infección congénita.
Como ya se describió, en la mayoría de los recién nacidos infectados vía transplacentaria (60 a 95%) las manifestaciones clínicas están ausentes (asintomáticos) y sólo un pequeño porcentaje presentará signos que delatan la infección. Cuando existen hallazgos clínicos, frecuentemente son inespecíficos y diversos: bajo peso al nacer, prematurez, síndrome de trastorno respiratorio, anasarca, test de Apgar inferior a 7, hepatoesplenomegalia, miocarditis y/o meningoencefalitis y otros. El recién nacido sintomático, presenta manifestaciones clínicas similares al síndrome de TORCH y debe considerarse esta infección en su diagnóstico diferencial.
|
La infección por T. cruzi de la mujer, es responsable en la génesis de un caso de Chagas congénito, por lo que las medidas de prevención y control de la enfermedad deben aplicarse idealmente en el período preconcepcional de las mujeres en edad reproductiva. |
En caso de sospecha de enfermedad de Chagas en un niño (a) mayor de nueve meses de edad no diagnosticado precozmente, se aplicará el mismo algoritmo de diagnóstico que indica la Norma.
Anexo Nº 1
Algoritmo de diagnóstico de la infección por T. cruzi en mujeres gestantes
inmunocompetentes
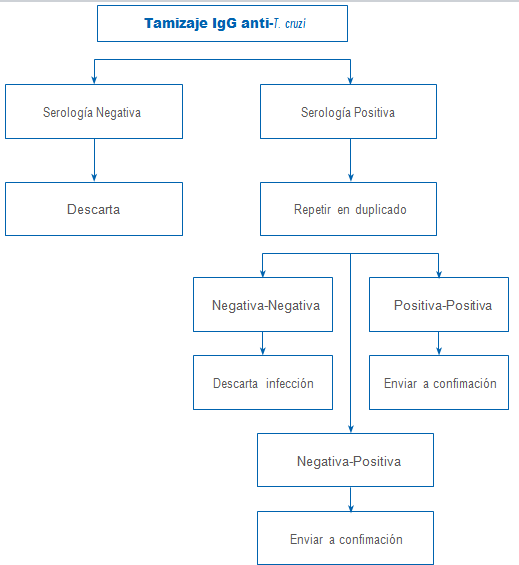
Ministerio de Salud. Departamento Enfermedades Transmisibles.
Anexo Nº 2
Algoritmo de diagnóstico de la infección por T. cruzi en el recién nacido menor de 9 meses, hijo de mujer con enfermedad de Chagas
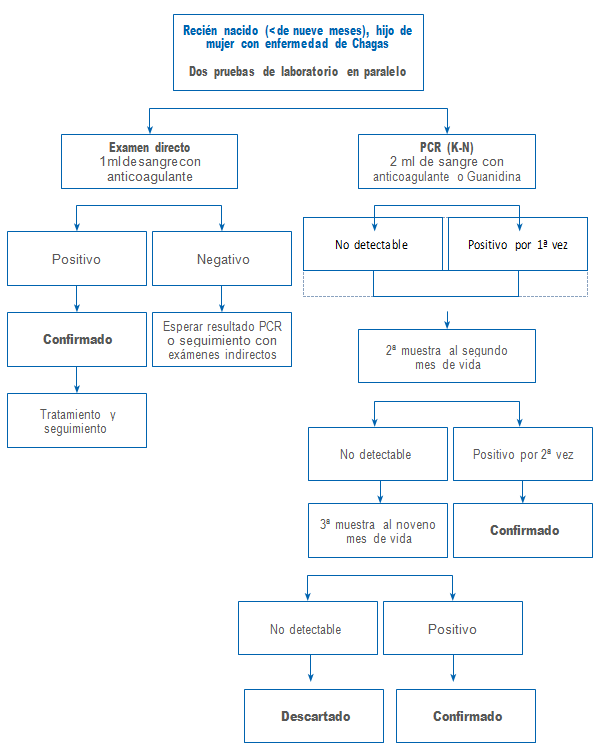
Ministerio de Salud. Departamento Enfermedades Transmisibles.

