ACLS-Asistolia/AESP
Introducción
El paro cardiorrespiratorio (PCR), se define como el cese súbito de actividad cardíaca con el consiguiente colapso hemodinámico (1). Corresponde a una de las principales causas de muerte en el mundo y en nuestro país. Ocurre principalmente producto de arritmias, como la taquicardia ventricular (TV) y la fibrilación ventricular (FV), pero también puede ocurrir debido a ritmos no desfibrilables como la asistolia y actividad eléctrica sin pulso (AESP).
La asistolia se define como la ausencia total de actividad electro-mecánica a nivel cardiaco, mientras que la AESP se define como un grupo heterogéneo de ritmos electrocardiográficos organizados; sin contracción mecánica suficiente del corazón para producir pulso palpable o presión arterial medible. Por definición, la asistolia y la AESP son ritmos donde no existe perfusión, por lo que requieren el inicio de RCP de forma inmediata. El tratamiento efectivo depende de compresiones efectivas, tratamiento vasopresor (ej.: epinefrina) y rápida reversión de las causas subyacentes (hipoxia, hiperkalemia, intoxicación y hemorragia). (2)
Epidemiología
1. Realidad internacional:
Se estima que el número de personas que sufre un PCR en USA varía entre 180000-450000 personas. Estos valores disminuyen en américa del norte y Europa donde la incidencia estimada es de 50-100 por 100000 personas.
Pese al avance en la reanimación cardiovascular, las tasas de sobrevida son bajas. Estudios han reportado que en el ambiente extra hospitalario, las tasas de sobrevida fluctúan entre 1-6%. En el caso de PCR extra hospitalarios atendidos por personal especializado, estudios han reportado una sobrevida de 5-10% y de un 15% en aquellos casos que existía fibrilación ventricular. En al caso de PCR intrahospitalarios se ha reportado un 17% de sobrevida al alta. (3)
La incidencia de PCR aumenta drásticamente con la edad y con la presencia de enfermedad cardiacas subyacente. Los hombres tienes 2-3 veces más riesgo de experimentar un PCR que las mujeres. El riesgo de presentar un PCR aumenta 6-10 veces en la presencia de enfermedad cardiaca diagnosticada y 2-4 veces en la presencia de FR para cardiopatía coronaria. La muerte súbita es el mecanismo de muerte en cerca del 60% de los pacientes con enfermedad coronaria. Adicionalmente, el PCR es la manifestación clínica inicial en aprox. 15% de los paciente con cardiopatía coronaria. (1)
2 . Realiadad Nacional:
El paro cardiaco respiratorio (PCR) es la causa de muerte más importante en Chile, afectando a cerca de 24.000 individuos al año. (4). En Chile no existe un registro nacional exacto, sin embargo un estudio de paros cardiacos extra hospitalarios en la Región Metropolitana atendidos por el SAMU durante el año 1995, pudo constatar una mortalidad cercana al 98%. (5)
En cuanto al PCR extra hospitalario, en un estudio que realizó por el SAMU publicado el año 2009 que incluyo a 221 pacientes, se reportó que en 58,1% el PCR ocurrió en el domicilio. El primer ritmo monitorizado fue asistolia en 52,2%, fibrilación ventricular en 32,4%, y actividad eléctrica sin pulso en 14,0%. Un 28,1% retornó a circulación espontánea durante las maniobras. El 16,4% fue hospitalizado y 3,3% fue dado de alta vivo. (6)
En cuanto al PCR intrahospitalario, en un estudio realizado en la UCH acerca de los PCR perianestesicos publicado el año 2009, se analizaron los eventos ocurridos en 37.718 cirugías. Se observó que ocurrieron 19 PCR con una incidencia de 5,03/10.000. El ritmo inicial fue desfibrilable en 5 casos (27,7%) y no desfibrilable en 13 (72,3%): actividad eléctrica sin pulso en 6, asistolia en 6 y bradicardia extrema en 1. Del total de pacientes, 13 sobrevivieron al evento (72,2%), 12 estaban vivos a las 24 horas (66,6%), 8 sobrevivieron al alta hospitalaria (44,4%) y 1 aún se encontraba hospitalizado. Después del alta se siguió a 6 pacientes; todos ellos estaban vivos y sin daño neurológico a los 6 y 12 meses. (7)
3. Etiología
Dentro de las causas más frecuentes de muerte súbita en el ambiente extra hospitalario se encuentran:
- Enfermedad coronaria: La principal etiología del PCR corresponde a arritmias letales producto de enfermedad cardiovascular isquémica, donde 60-70% de todas las muertes súbitas son atribuibles a enfermedad coronaria.
- Enfermedades cardiacas estructurales (ej.: anomalías coronarias congénitas, miocarditis, cardiopatía hipertrófica, cardiopatía arritmogenica del ventrículo derecho): 10% de las muertes súbitas se deben a casusas de este tipo. La frecuencia es mucho mayor en sujetos menores de 30 años.
- Arritmias en ausencia de enfermedad cardiaca estructural (ej.: QT largo, sd Brugada, TV catecolaminergica polimórfica): 5-10% se producen por esta causa.
- Origen no cardiaco (trauma, sangrado, intoxicaciones, hemorragias intracraneaneas, embolismo pulmonar, accidentes pos inmersión y obstrucción de la vía aérea) corresponde a al 15-25% de los PCR
- ICC: La muertes súbita se observa en 30-50% de los pacientes con ICC y la incidencia de muerte súbita aparentemente aumenta en los periodos de descompensación de la ICC. Es por ello que todos los pacientes con ICC sobrevivientes de muerte súbita recibe un DAI
Existen causas transitorias y reversibles que pueden precipitar arritmias, de modo que su identificación y manejo son fundamentales para tratar la enfermedad subyacente y prevenir la recurrencia de muerte súbita. Dentro de los gatillantes de este tipo se encuentran;
- Isquemia cardiaca aguda e infarto al miocardio.
- Medicamentos como por ejemplo drogas que prolongan el QT, toxinas, drogas ilícitas
- Alteraciones electrolíticas, principalmente hipokalemia, hiperklamia e hipomagnesemia
- Alteraciones de pH, especialmente acidemia
- Activación del sistema nervioso autónomo, especialmente de estímulos simpáticos(8)
| 5H | 5 T |
| Hipovolemia | Taponamiento cardíaco |
| Hiopoxia | Neumotórax a Tensión |
| Ion Hidrógeno(acidosis) | Tóxicos |
| Hipokalemia/Hiperkalemia | Trombosis pulmonar |
| Hipotermia | Trombosis coronaria |
Fig 1. Causas reversibles de PCR(9)
Fisiopatología
El PCR se refiere al cese súbito de la actividad cardiaca con el subsiguiente colapso hemodinámico. La magnitud del daño producido dependerá de la condición previa del paciente y del tiempo que tome retornar a la circulación normal. Los órganos más tempranamente afectados por el colapso circulatorio son el cerebro y corazón. El daño producido a estos órganos, especialmente al cerebro, determinan el pronóstico del paciente que ha sufrido un PCR.
La detención de la circulación significa un abrupto corte en el aporte de O2 y glucosa a las células de los diferentes tejidos. El aporte de O2 depende de la mantención de un adecuado flujo tisular, cuya suma total se conoce como gasto cardiaco, y de un nivel de Hb que actúe como transportador del O2. En el caso del PCR el problema surge mayoritariamente de la inexistencia de gasto cardíaco más que de un déficit en la saturación con O2 de la Hb. Pese a que la consecuencia final es la misma, ya que una detención de la circulación lleva a una detención de la ventilación y viceversa, el hecho de que el fenómeno circulatorio sea mucho más frecuente nos lleva a priorizar este aspecto en las medidas de reanimación. Si la causa del PCR es de tipo circulatoria, en general el nivel de saturación de la Hb previo al evento será normal, por lo que la real necesidad tisular será que se genere un flujo sanguíneo adecuado que lleve el O2 a las células. (5)
Dentro de los desencadenantes de PCR, la taquicardia ventricular y la fibrilación ventricular son responsables de la mayoría de los episodios. Las causas son distintas en pacientes usuarios de DAI, donde la muerte por arritmias alcanza un 20-35%, y la AESP se convierte en una causa más frecuente. Esto también cambia en pacientes no monitoreados en el ambiente extra hospitalario, donde la TV/FV son responsables de un 25-35% de los episodios, y la AESP es responsable de hasta 25% de los casos. En casos como estos, donde los paciente que colapsan en un ambiente no monitoreado y no se sabe el momento exacto en que se inició el cuadro ni la arritmia que lo origino, la asistolia es el ritmo más frecuentemente observado. La asistolia se correlaciones con la duración del PCR y puede ser el resultado de una FV que estuvo presente por varios minutos y que posteriormente conlleva a la perdida de actividad eléctrica como resultado de la hipoxia, acidosis y muerte del tejido miocárdico.
En aproximadamente un 80% de los pacientes con TV/FV, la arritmia ventricular sostenida es precedida por una ectopia ventricular y el desarrollo de una arritmia ventricular repetitiva, particularmente repeticiones de una taquicardia ventricular no sostenida. Estas arritmias espontaneas están presentes por un periodo de tiempo variable previo a la TV/FV.
- Las TV monomorfas sostenidas pueden acelerarse y alcanzar una frecuencia elevada, para luego degenerar en una FV. Sin embargo, la relación entre TV monomorfa y muerte súbita ha sido discutida, ya que algunos estudios sugieren que esta arritmia se presenta solo en una minoría de pacientes con muerte súbita.
- Una TV polimorfa sostenida puede degenerar en una FV. Esto comúnmente es resultado de isquemia, aunque puede ser producto de una prolongación adquirida o congénita del QT. Una causa muy rara de TV polimorfa sin prolongación del QT es una anormalidad genética asociado a la TV polimorfa catecolaminergica(anormalidad del gen de la rianodina o de la calsecuestrina)
- La FV se puede producir como evento primario.
En aprox. 1/3 de los casos, la taquiarritmia se inicia como un R sobre T en un latido ventricular prematuro. En los 2/3 restante la arritmia se inicia en un ciclo tardío de un latido ventricular prematuro.
- Las bradiarritmias y la asistolia, son causas menos comunes de muerte súbita, siendo observadas solo en aprox. el 10% de los casos documentados en monitoreos ambulatorios. La bradiarritmia está asociada principalmente con cardiopatía no isquémica, mientras que la AESP o la asistolia son los ritmos más comúnmente observados en embolismos pulmonares. En algunos casos, la bradiarritmia puede resultar en una taquiarritmia ventricular como mecanismo de escape.(8)
Diagnóstico y diagnósticos diferenciales
1. Valoración rapida inicial
El reconocimiento oportuno del PCR es el primer paso para una reanimación exitosa. Se debe sospechar PCR ante el colapso de una persona, falta de respuesta, respiración débil/ausente o imposibilidad para palpar el pulso dentro de 10 seg.
De acuerdo a las guías de la AHA, lo primero que se debe hacer es evaluar que el área sea segura, luego acercarse y evaluar la falta de respuesta del paciente, tocándole el hombro y gritándole:»¿esta Ud. Bien?». Si la persona no responde se debe pedir ayuda, activar el sistema de emergencia e iniciar compresiones cardiacas.
Personal entrenado puede evaluar el pulso carotideo, sin embargo no debe tardar más de 10 seg en determinar la ausencia de pulso. De forma simultanea se debe evaluar la respiración, si el paciente no está respirando normalmente, se debe asumir apnea. La clave es no demorara el inicio de reanimación en las personas que lo requieran. (3)
2. Pruebas diagnosticas
a) ECG: su evaluación es fundamental en el diagnóstico y manejo del PCR. Se evalúa principalmente mediante un monitor cardiaco y permite distinguir si el ritmo es desfibrilable (FV/TV) o no desfibrilable (AESP/Asistolia), y continuar con el manejo correspondiente. (2)
b) Ecocardiografía: Su principal utilidad es diagnostica, especialmente en paciente con AESP. El ecocardiograma distingue la AESP que genera contracción cardiaca de la que no. Informa del estado de volumen intravascular (valorando el volumen ventricular), el estado de la contractilidad cardiaca del VI y defectos de movilidad locales de la pared miocárdica (9). También es útil en el diagnóstico de las causas mecánicas de la AESP, tales como neumotórax a tensión, taponamiento pericárdico y TEP. Además, es útil para guiar la pericardiocentesis.
En el periodo post PCR, la ecocardiografía puede ayudar a definir la necesidad de intervenciones postparo o asistencia mecánica en el caso de un corazón que no funcione de forma adecuada. (10)
Exámenes complementarios
Los exámenes de laboratorio que se pueden solicitar, incluyen monitoreo intermitente de GSV y GSA y exámenes bioquímicos, pero su utilidad es limitada. Los hallazgos habituales corresponden a acidosis respiratoria en los gases venosos y alcalosis respiratoria en los arteriales. La sat O2 es usualmente mayor al 94% durante la reanimación y es de poca utilidad, excepto en el caso de embolismo pulmonar masivo o intubación esofágica no detectada. La Savo2 indica la realización correcta de la reanimación cardiopulmonar, sin embargo una sola medida no es de tanta utilidad como lo es la monitorización continua mediante oximetría. Otros exámenes de laboratorio que se pueden realizar durante la reanimación sirven principalmente para confirmar diagnósticos asociados al PCR, sin embargo sus resultados generalmente están disponibles de forma tardía. Los ELP se pueden solicitar para descartar hiperkalemia, hipokalemia, hipomagnesemia, hipercalcemia e hipocalcemia, sin embargo el tratamiento empírico debe ser administrado inmediatamente si se tiene una alta sospecha clínica de alguno de estos trastornos. También se puede medir el nivel de hemoglobina para evaluar la presencia de hemorragia. Sin embargo, se debe recordar que inicialmente el nivel de hemoglobina puede estar normal en hemorragias agudas, debido a una ausencia de equilibrio entre los compartimientos intersticial y vascular. (10)
Criterios de ingreso
Dado que es una emergencia médica, siempre requiere ingreso en una unidad de cuidados intensivos para administrar los cuidados post reanimación (9). Estas medidas incluyen:
- Hipotermia terapéutica: se debe mantener una temperatura menor a 34°C en paciente con coma profundo, evidencia de edema cerebral o que presenta patrones malignos en el EEG. En pacientes que no cumple con los criterios anteriormente descritos, se debe mantener una temperatura inferior a 36°C. (10) Para alcanzar estas temperaturas se aplican compresas frías en el cuello, ingle y axila, ventiladores con aire humedecido, mantas enfriadoras bajo y sobre el paciente, bolos de SF a 4°C de 1-2 L y sistema endovasculares de enfriamiento que requieren la instalación de un CVC. Se deben mantener la hipotermia por 24 hrs , con el posterior recalentamiento en las siguiente 8-12 hrs a 0.25°C/ hora.(10-12)
- Reperfusión coronaria: se debe realiza un ECG de 12 derivaciones con derivadas derechas y posteriores. Si existe elevación del ST o nuevo bloqueo de rama izquierda se debe realizar reperfusion coronaria mediante angioplastia de preferencia, pero en ausencia de su disponibilidad también es útil la fibrinólisis (contraindicada ante neumotórax, tórax volante, contusión pulmonar con hemorragia). Se ha observado que la reperfusion coronaria aumenta la sobrevida post PCR.
- Tratamiento antiplaquetario y terapia anticoagulante: en todos los pacientes, a menos que exista evidencia de hemorragia o exista hipertensión marcada.
- Marcapasos: se debe instalar en pacientes con nuevo bloqueo de rama izquierda, bloqueo de rama derecha y hemibloqueo anterior o posterior, bloqueo de segundo grado tipo II o bloqueo de tercer grado.
- Medición de lactato y de SvO2: el lactato es una medida indirecta de si existe una entrega adecuada de O2 a los tejidos al igual que la SvO2. La combinación de un lactado elevado con una SvO2 baja indica una entrega inadecuada de O2. La combinación de un lactato elevado con una SvO2 normal o elevada indican la existencia de un cortocircuito severo. El tratamiento de estas alteraciones incluye la reducción de la infusión continua de vasopresores y mayor administración de volumen.(10)
Algotirmo diagnóstico
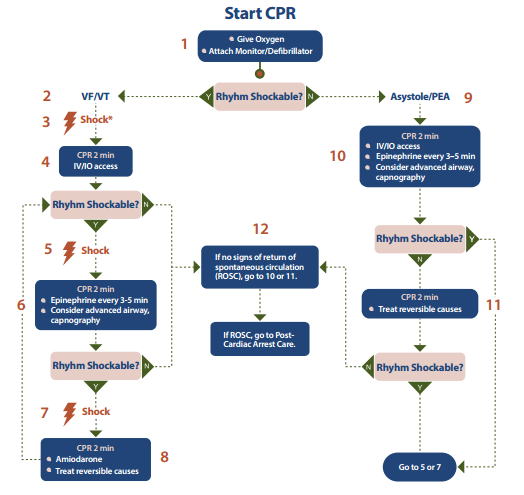
Fig.2 Algoritmo de diagnóstico y manejo de paro cardiorrespiratorio con ritmo no desfibrilable.
PCR: paro cardiorrespiratorio RCP: Reanimación cardiopulmonar O2: oxigenoterapia IV: intravenosa IO: Intraósea AESP: actividad eléctrica sin pulso
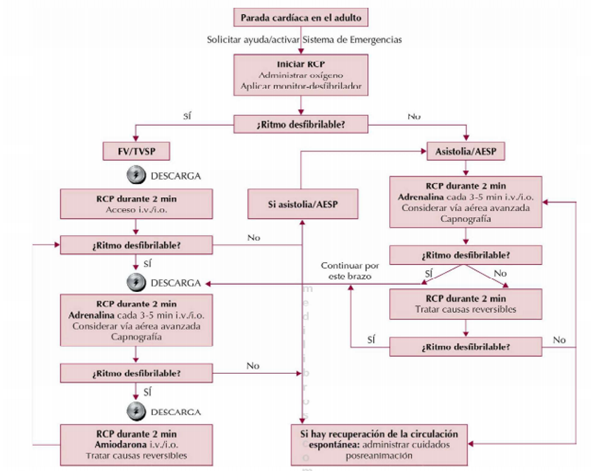
Fig.3.Recomendaciones en soporte vital avanzado para profesionales de la salud (9)
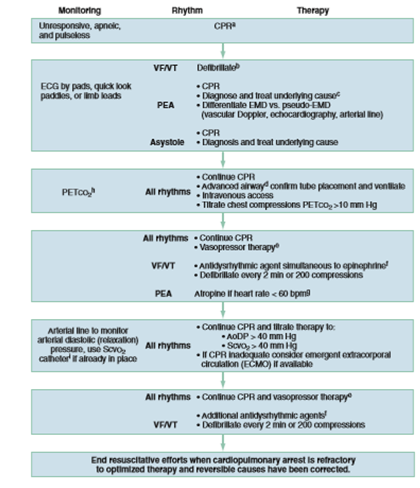
Fig. 4. Algoritmo de tratamiento de PCR en urgencia (10)
Manejo
El inicio de compresiones torácicas de calidad es el primer paso para mejorar la entrega de oxígeno a los tejidos. Este es el fundamento detrás del enfoque compresiones-vía aerea-ventilacion(C-A-B) para enfrentar el PCR. A continuación se describirán en detalle, las características más importantes de cada etapa del proceso de reanimación.
1. Compresiones torácicas
Realizar compresiones torácicas es el elemento más importante de la reanimación cardiopulmonar. La perfusión coronaria y el retorno a la circulación espontanea se maximizan cuando se realiza compresiones torácicas de calidad. Las características compresión torácica de calidad son las siguientes:
- Mantener una frecuencia de compresiones torácicas entre 100-120 compresiones por minuto. Una frecuencia inadecuada de compresiones torácica reduce la probabilidad de ROSC y de sobrevida neurológicamente intacta.
- Comprimir al pecho al menos 5 cm, pero no más de 6 cm
- Permitir que el pecho se expanda completamente después de cada compresión para mejorar la precarga y aumentar la presión de perfusión coronaria
- Minimizar la frecuencia y duración de las interrupciones
- Mantener al paciente posición adecuada: el paciente debe estar recostado sobre una superficie firme.
- Ubicación del reanimador adecuada: el reanimador debe posicionar la base de su mano en la parte inferior del esternón y apoyar la base de la otra mano sobre la primera. El pecho del reanimador debe estar directamente sobre sus manos para usar su peso corporal para realizar las compresiones.
- Los reanimadores deben cambiarse cada 2 min cuando hay más de una persona presente. Las interrupciones son minimizadas realizando los cambios cuando se evalúe el ritmo y el paciente sea desfribrilado de ser necesario.
- En caso de que se disponga de vía aérea avanzada, las compresiones deben ser continuadas y solo interrumpidas cada 2 min para evaluar ritmo y ROSC.
- Minimización de interrupciones: Las interrupciones en las compresiones torácicas provoca un deterioro en la presión de perfusión cerebral y coronaria, empeorando los resultados para los pacientes. De esta forma la verificación del pulso y el análisis de ritmo cardiaco deben ser realizadas cada 2 minutos solamente y no deben durar más de 10 segundos, excepto para intervenciones específicas como desfibrilación. Cuando se está realizando la preparación para la desfibrilación los reanimadores deben continuar las compresiones de calidad mientras se está cargando el desfibrilador hasta justo antes de aplicar el shock eléctrico y se deben reasumir las compresiones inmediatamente posterior a la descarga, sin perder tiempo en evaluar pulso ni respiración. No deben pasar más de 3-5 seg entre que se detienen las compresiones y se da la descarga eléctrica. (3)
2. Ventilaciones:
Durante la fase inicial del PCR, cuando los vasos pulmonares y el corazón contienen todavía suficiente sangre oxigenada para satisfacer la demanda, la importancia de las compresiones es superior a las de las ventilaciones. En consecuencia, el inicio de compresiones torácicas de calidad es el primer paso para mejorar la entrega de oxígeno a los tejidos.
Las realizaciones de ventilaciones apropiadas se vuelven más importantes a medida que la ausencia de pulso persiste. Esto se deba a que a medida que pasa el tiempo se alcanza la fase metabólica del PCR y se necesitan de las ventilaciones para lograr una oxigenación adecuada.
Las características de las ventilaciones apropiadas son las siguientes:
- Realizar dos ventilaciones después de cada 30 compresiones en paciente sin vía aérea avanzada
- La duración de cada ventilación debe ser menor a 1 segundo
- Proporcionar solo el volumen corriente suficiente para que se expanda el tórax(aproximadamente 500-600 mL, o 6-7 mL/kg
- Evitar la ventilación excesiva
- Realizar ventilaciones independientes de las compresiones, cada 8-10 seg(6-8 por minuto) en pacientes con vía aérea avanzada(mascara laríngea, tubo endotraqueal)
Se debe evitar la ventilación excesiva. Esto, debido a que la ventilación a presión positiva aumenta la presión intratoracica, lo que causa una disminución del retorno venoso, de la perfusión pulmonar, del gasto cardiaco y de la presión de perfusión coronaria. Además, estudios han demostrado que la sobre ventilación reduce el éxito de la desfibrilación y disminuye la sobrevida. (3)
Tomando todo lo anteriormente mencionado, las guías ACLS del 2010 recomiendan el uso de una bolsa auto inflable o la instalación de un dispositivo supraglotico para manejo inicial de la ventilación en el PCR. Se difiere la instalación del tubo endotraqueal, a menos que la intubación pueda ser realizada sin interrumpir las compresiones o no se pueda ventilar al paciente mediante otra vía menos invasiva. (2)
Equipo de reanimación
La reanimación usualmente involucra a varios profesionales de la salud de distintas disciplinas, que puede que nunca hayan trabajado juntos antes. Bajo estas circunstancias, establecer roles puede ser difícil. Es por ello, que es imperativo que una persona asuma el rol de líder del equipo. Esta persona será responsable del manejo global de la reanimación que incluye: asegurar que todas las tareas necesarias se estén llevando a cabo de forma competente, incorporar información nueva y útil, coordinar la comunicación entre los miembros del equipo y desarrollar e implementar estrategias de manejo que maximicen los resultados del paciente.
El líder del equipo debe evitar realizar procedimientos, ya que el cambio de tarea altera inevitablemente la atención que se le brinda a las responsabilidades de liderazgo. En el caso de que el personal sea limitado, el líder puede realizar ciertos procedimientos críticos y transferir el liderazgo temporalmente a otro profesional.
Una comunicación organizada es fundamental para proporcionar los cuidados apropiados. Por tanto, toda comunicación debe ser a través del líder y éste es el que comparte la información importante con el equipo. Cuando el líder determine que se debe llevar a cabo determinada tarea, la petición debe ir dirigida a un miembro especifico del equipo. Esto es particularmente importante en el caso de la persona asignada a administrar medicamentos y las desfibrilaciones. (2)
Tratamiento farmacológico
1. Actividad eléctrica sin pulso
A diferencia de la fibrilación ventricular o la taquicardia ventricular no se realiza desfibrilación en la AESP ni en la asistolia. Las principales medidas son la realización de compresiones de calidad, tratamiento vasopresor y el tratamiento rápido de las causas reversibles, sobretodo en casos como el neumotórax a tensión y el taponamiento cardiaco, donde la reanimación cardiopulmonar se vuelve inefectiva.
Mientras un profesional realizar la RCP, el otro reanimador no debe temer realizar los procedimientos apropiados para manejar posibles causas de AESP, incluso si no se cuenta con confirmación definitiva.
La RCP debe ser continuo y solo se debe interrumpir brevemente en los intervalos de 2 min que se usan para evaluar ritmo cardiaco y retornos a la circulación espontanea.
En cuanto al rol de los vasopresores en la AESP, la eficacia de la epinefrina (1 mg IV cada 3-5 min) sigue siendo dudosa, pero persiste como parte del manejo. Las guías de la AHA 2010 permiten sustituir la primera o segunda dosis de epinefrina por vasopresina, ya que en varios estudios no se encontró ninguna fuera superior sobre la otra.
En cuanto a la atropina, la guía de la AHA 2010 la elimino como parte del manejo de la AESP, debido a la ausencia de beneficio terapéutico. La administración de atropina (1 mg cada 3-5 min) puede ser considerada en AESP cuando la FC es lenta (ej.: bradicardia absoluta con una FC menor a 50 lpm o bradicardia relativa que consiste en una frecuencia cardiaca menor a la esperada dada la condición subyacente)
2. Asistolia
los PCR donde la asistolia es el ritmo inicial, tiene un pronóstico muy pobre (0-2% de sobrevida al alta hospitalaria). La asistolia es habitualmente un evento secundario, resultado de una fibrilación ventricular prolongada o AESP, con la consiguiente pérdida de toda actividad eléctrica. También puede ocurrir como resultado de una hipoxia prolongada, acidosis y muerte del tejido miocárdico.
La verdadera asistolia debe ser confirmada revisando que los cables del desfibrilador estén adecuadamente conectados, mejorando la ganancia y confirmando la asistolia en otra derivación. La guía 2010 de la AHA, recomienda que la asistolia sea tratada al igual que la AESP con compresiones torácicas de calidad, vasopresores y evaluando la posibilidad de causas reversibles.
La atropina no se recomienda. Tampoco existe beneficio de la desfibrilación.
El uso rutinario de marcapaso temporal en la asistolia no está recomendado, dado que no se ha demostrado su beneficio en cuanto a sobrevida.
En cuanto a los vasopresores se recomienda la epinefrina (1 mg IV cada 3-5 min), aunque no existe beneficio claramente demostrado. Dosis altas de epinefrina no son recomendadas de forma rutinaria, ya que pese a que se ha observado un aumento de las tasas de reanimación exitosa, no existe mejoría de la sobrevida al alta hospitalaria.
En cuanto a la vasopresina, se ha estudiado como alternativa a la Epinefrina. Sin embargo, no se ha encontrado diferencias significativas entre ambas. En base a esto, las guías permiten reemplazar la primera o segunda dosis de epinefrina por vasopresina.
En cuanto a la atropina, no está recomendada dado a la escasez de datos que apoyen su uso.
Tratamientos inefectivos: varios tratamientos han demostrado ser inefectivos y por tanto no son de uso rutinario:
- Bicarbonato de sodio, excepto en pacientes con hiperkalemia o en sobredosis con AD tricíclicos
- Tratamiento fibrinolitico
- Marcapaso para asistolia y AESP
- Sulfato de magnesio, excepto en pacientes con QT largo inducido por drogas y que desarrollan una torsión de las puntas(11)
Tratamiento de causas reversibles
Dentro de las medidas utilizadas para tratar causas reversibles de PCR se encuentran
- Colocación de dispositivo de vía aérea avanzada en caso de hipoxemia
- Reposición de fluidos en caso de hipovolemia o sepsis
- Transfusión sanguínea en caso de hemorragia intensa
- Fibrinólisis empírica en caso de TEP
- Descompresión torácica en caso de neumotórax a tensión
- Administración de bicarbonato de sodio 1 M en caso de arritmia ventricular grave por cocaína, hiperkalemia o por AD tricíclicos
- Administración de altas dosis de adrenalina en intoxicación por beta bloqueadores o calcioantagonistas.(9)
| Causa | Diagnostico | Tratamiento paliativo | Tratamiento Definitivo |
| Hipovolemia | Respuesta a infusión de volumen | Infusión de volumen, considerar masaje cardiaco con tórax abierto | Hemostasia si hemorragia |
| Hipoxia | Respuesta a oxigeno | Oxigenoterapia, ventilación asistida | Tratamiento de las causas subyacentes |
| Taponamiento cardíaco | Ecocardiografía, pericardiocentesis | Pericardiocentesis | Toracotomía o pericardiotomia |
| Neumotórax a tensión | Ruidos respiratorios asimétricos, desviación de la tráquea | Toracotomía con aguja | Tubo de toracostomia |
| Hipotermia | Temperatura rectal | – | Lavado peritoneal o torácico tibio, compresiones cardiacas con tórax abierto, bypass cardiopulmonar |
| Embolismo pulmonar | Factores de riesgo o evidencia de trombosis venosa profunda | Bypass cardiopulmonar o masaje cardiaco con tórax abierto | Embolectomía pulmonar, terapia lítica |
| Sobredosis de drogas | Historia de ingestión de drogas | Específico para la droga | Específico para la droga |
| Hiperkalemia | Historia de falla renal o de potasio elevado | Insulina, glucosa, bicarbonato de sodio | Hemodiálisis |
| Acidosis | Gases en sangre arterial | Hiperventilación, bicarbonato de sodio, cloruro de calcio | Tratar la causa subyacente |
Fig. 5. Diagnóstico y tratamiento de causas frecuentes de Actividad eléctrica sin pulso (10)
Monitorización
Tradicionalmente la monitorización durante la reanimación se ha basado en la evaluación del electrocardiograma en una o más derivadas y en la palpación del pulso femoral o carotídeo. El en este tipo de monitorización, consiste en que por un lado el ECG sólo entrega información acerca de actividad eléctrica, sin permitir evaluar actividad mecánica, mientras que el pulso no permite estimar con exactitud el grado de flujo que realmente existe. Una forma de monitorización más completa, incluye la evaluación de la presión de perfusión coronaria, volumen espirado de CO2 y saturación venosa central de oxígeno.
1. Presión de perfusión coronaria (PPC):
Consiste en el flujo sanguíneo que llega al miocardio y depende de la diferencia de presión entre la aorta y la aurícula derecha durante la diástole.
Su medición permite evaluar si la reanimación se está llevando a cabo de forma apropiada, requiriéndose una PPC mínima de 15 mmHg para alcanzar ROSC. Además, indica si se produce o no contracción mecánica en la AESP, permite evalúa ROSC y obtener monitoreo de gases seriados.
Para poder medirla se requiere de la lectura simultanea de los datos arrojados por una línea arterial permanente y un CVC, de modo que su uso en el departamento de urgencia es bastante impracticable.
2. Volumen de CO2 al final de la espiración:
La presión parcial de CO2 medida al final de la espiración es un indicador confiable del gasto cardiaco durante la reanimación. Se mide mediante capnografía, luego de la intubación endotraqueal. Su valor depende de la producción de CO2, ventilación alveolar y flujo sanguíneo pulmonar y se correlaciones muy bien con la presión de perfusión coronaria y cerebral. De este modo, cuando la ventilación se mantiene constante y no existe administración exógena de CO2 (administración de bicarbonato), solo el aumento del gasto cardiaco durante la reanimación y ROSC aumenta su valor. Además, permite identificar la existencia de flujo en los pacientes con AESP, ya que en pacientes con actividad mecánica cardiaca puede existir flujo pulsátil que no puede ser detectado mediante palpación del pulso, pero sí mediante la elevación del volumen de CO2 espirado cuando no se están realizando compresiones.
3. Saturación venosa central de oxigeno (SvcO2):
Cuando está disponible, constituye un método adicional para evaluar la calidad de la reanimación. La saturación venosa mixta en la arteria pulmonar, representa el oxígeno que permanece en la sangre posterior a su extracción. Los cambios en la SvcO2 reflejan cambios en la entrega de oxígeno y por tanto cambios en el gasto cardiaco. Permite detectar rápidamente ROSC, sin tener que interrumpir las compresiones, ya que en estos casos se produce un aumento de SvcO2, debido al aumento de entrega de oxígeno a los tejidos. (10)
Conclusión
El PCR es una de las causas más frecuentes de muerte en el mundo y en nuestro país, por lo tanto es importante saber reconocerlo y manejarlo.
La principal etiología del PCR es de origen cardiaco, sin embargo no se debe olvidar que existen diversas causas, para lo cual es útil recordar las 5H(hipovolemia, hipoxia, hidrogeniones(acidosis), hipo/hiperkalemia, hipotermia) y las 5T(taponamiento cardíaco, tóxicos, trombosis pulmonar, trombosis coronaria, neumotórax a tensión).
Se reconoce a una persona en PCR, porque no responde, no respira/ respira débilmente o no se logra palpar el pulso. Ante una situación como esta, se debe activar el protocolo de emergencia, instalar un monitor cardiaco y evaluar el ritmo. En el caso de los ritmos no desfibrilables la clave es el masaje cardiaco de calidad, para lo cual es fundamental que cumpla con las siguientes características: mantener una frecuencia de 100-120 compresiones por minutos, hundir 5 cm el tórax y permitir que su expansión posterior y mantener una proporción 30 compresiones/2 ventilaciones o en caso de contar con vía aérea avanzada realizar compresiones de forma continua. Paralelamente, las ventilaciones deben cumplir con los siguientes criterios: duración máxima de 1 s por ventilación y en el caso de contar con vía aérea avanzada, mantener una frecuencia de 6-8 por minuto. Adicionalmente, se deben administrar vasopresores como la Adrenalina en dosis de 1 mg IV o IO y repetir las dosis cada 3-5 min y realizar el manejo de causas reversibles.
El proceso de reanimación cardiopulmonar debe contar con mínimo de interrupciones, reduciéndolas a comprobar pulso, evaluar ritmo y realizar el cambio de reanimador cada 2 min. Es esencial que el equipo este organizado por un líder que velara por la correcta realización de la reanimación y la necesidad de procedimientos adicionales.
Por último, se debe mantener al paciente monitorizado mediante caponografia dentro de lo posible, para poder evaluar la calidad de la reanimación y el ROSC.
Bibliografía
- Podrir, P. (2016). Overview of sudden cardiac arrest and sudden cardiac death. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/overview-of-sudden-cardiac-arrest-and-sudden-cardiac-death?topicKey=CARD%2F963&elapsedTimeMs=0&source=search_result&searchTerm=cardiac+arrest&selectedTitle=1~150&view=print&displayedView=full
- Poner, Ch. (2016). Avance cardiac life support (ACLS) in adults. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/advanced-cardiac-life-support-acls-in-adults?source=search_result&search=ACLS&selectedTitle=1~150
- Pozner, Ch. (2016). Basic life support (BLS) in adults. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/basic-life-support-bls-in-adults?source=search_result&search=bls&selectedTitle=1~39
- Dirección nacional de salud programa nacional de primeros auxilios. (2010). Capítulo III del manual de primeros auxilios de la cruz roja chilena. 2016, de Cruz Roja de Chile Sitio web: http://www.cruzroja.cl/files/Capitulo_iii_rcp_2010_manual_ppaa_CRCh1.pdf
- Flisfisch, H.,Aguiló, J.,& Leal, F. (2014). Actualización en paro cardiorrespiratorio y resucitación cardiopulmonar. Rev. Medicina y Humanidades., VI, 29-36
- Mayanza, S., Barretoa, J., Grovea, X., Iglesias, V.,& Breinbauerd, H.(2009). Paro cardiorrespiratorio extra-hospitalario de causa cardiaca en Santiago de Chile: Experiencia del equipo medicalizado del SAMU Metropolitano. Revista chilena de medicina intensiva, 24, 9-16.
- Aguirre, M.,& Mayanz, S.(2009). Registro de paro cardiorrespiratorio perianestésico en el hospital clínico de la Universidad de Chile: primeros tres años de experiencia. Rev Chil Anest , 38, 214-223.
- Podrid, P.& Cheng, J. (2016). Pathophysiology and etiology of sudden cardiac arrest. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/pathophysiology-and-etiology-of-sudden-cardiac-arrest?source=search_result&search=pahtophysiology+cardiac+arrest&selectedTitle=5~150
- Calderon de la Barca, J.,Montero, F., Jimenez, L.& Torres, J.B. (2015). Soporte vital avanzado en adultos. En Medicina de urgencias y emergencias(7-11). España: Elsevier.
- Ward, K., Kurz, M.& Neumar, R.(2014). Adult Resuscitation. En Rosen’s Emergency Medicine concepts and clinical practice (88-97). Philadephia: Elsevier.
- Pozner, Ch.& Link, M.(2016). Supportive data for advanced cardiac life support in adults with sudden cardiac arrest. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/supportive-data-for-advanced-cardiac-life-support-in-adults-with-sudden-cardiac-arrest?source=search_result&search=supportive+advanced+cardiac+live+support&selectedTitle=1~150
- Rittenberger, J.& Callaway, C. (2016). Post-cardiac arrest management in adults. 2016, de Uptodate Sitio web: http://www.uptodate.com/contents/post-cardiac-arrest-management-in-adults?source=search_result&search=post+cardiac+arrest&selectedTitle=1~29

