TEC
06/12/2016
- Introducción
Definición
El traumatismo encéfalo-craneano (TEC) es el resultado de una lesión cerebral no degenerativa, no congénita, producida por una fuerza mecánica externa, que puede dar lugar a un deterioro permanente o temporal de las funciones cognitivas, físicas y psicosociales, asociado a un estado de conciencia disminuido o alterado. El daño puede ser focal, limitado a una sola área del cerebro, o involucrar a más de un área del cerebro. A su vez, el traumatismo cerebral puede ser cerrado o abierto. Una lesión cerrada ocurre cuando la cabeza se golpea fuerte y repentinamente contra un objeto pero el objeto no penetra en el cráneo. El TEC abierto es aquel en que la duramadre se rompe y en ocasiones puede resultar de una lesión penetrante, que ocurre cuando un objeto perfora el cráneo y penetra en el tejido cerebral. EL TEC se distingue de la contusión de cráneo, que corresponde a un impacto mecánico sobre la bóveda craneana que no produce alteración del contenido craneano, y que puede asociarse a dolor local. El TEC es una patología heterogénea. Existen muchas maneras de clasificar a los pacientes de acuerdo a la gravedad clínica, mecanismos de lesión, y fisiopatología, cada uno de los cuales puede afectar el pronóstico y tratamiento. Epidemiología
El traumatismo encéfalo-craneano (TEC) representa uno de los mayores problemas de salud pública, ya que es considerada la primera causa de muerte y discapacidad en la población menor de 45 años.
La incidencia en EE.UU. fue estimada en 583.2 casos por 100.000 habitantes en 2003, mientras que tasas más bajas son reportadas en Europa (235 por 100.000) y en Australia (322 por 100.000).
La incidencia es más alta en los niños de 0 a 4 años, en adolescentes y adultos jóvenes, y en los adultos mayores (>65 años).
Al igual que en la mayoría de las lesiones traumáticas, la incidencia de TEC es significativamente mayor en hombres en comparación con las mujeres, en proporciones que varían entre 2:1 y 2,8:1. Para TEC severo, la proporción es más acentuada, 3,5:1. Otros factores de riesgo de TEC son nivel socioeconómico bajo y alteraciones psiquiátricas y cognitivas subyacentes.
En Chile, la causa de muerte por accidentes y traumatismos, corresponde a la tercera causa de muerte, después de las enfermedades cardiovasculares y el cáncer, y corresponde a la primera causa en menores de 45 años, con predominio del sexo masculino.
Datos estimativos en nuestro país indican que la tasa de hospitalización por TEC es de 200 por 100.000 habitantes por año. Alrededor del 50% de ellas corresponden a TEC leves, los casos moderados representan aproximadamente el 25%, y tienen mortalidad del 2% a 3%. El resto están dados por formas graves y en ellos la mortalidad es mayor al 36%. Sobre el 97% de los pacientes con Glasgow de 3, mueren o quedan en estado vegetativo persistente.
Por otra parte, se estima que en aquellas personas que fallecen como consecuencia de un accidente o politraumatismo, en el 40% a 50%, está comprometido el Sistema Nervioso Central. En Chile, el TEC es la causa de mortalidad en aproximadamente un 40% de los accidentes de tránsito fatales, y a su vez, la principal causa de muerte por TEC son los accidentes automovilísticos (sobre el 50% de los casos).Etiologías
La principal causa de TEC son las caídas, sobre todo en las edades extremas de la vida, y la mayor causa de muerte por TEC son los accidentes de tránsito, relacionados con automóviles, motocicletas, bicicletas y peatones. Otras causas de traumatismos cerebrales están relacionadas con la violencia, como asaltos con armas de fuego y maltrato infantil, y lesiones deportivas. En la mitad de los casos está involucrado el uso de alcohol.
La causa del traumatismo cerebral juega un papel muy importante en el pronóstico del paciente. Por ejemplo, aproximadamente el 91 por ciento de los traumatismos cerebrales relacionados con el uso de armas, terminan siendo fatales, mientras que sólo un 11 por ciento de los traumatismos cerebrales causados por caídas terminan en la muerte.
- Fisiopatología
La fisiopatología del TEC se divide en dos categorías diferentes pero que están relacionadas: lesiones cerebrales primarias y lesiones cerebrales secundarias.
Lesiones cerebrales primarias: ocurren en el momento del trauma. Los mecanismos más frecuentes son por impacto directo, rápida aceleración/desaceleración, lesión penetrante y ondas de choque. Aunque estos mecanismos son heterogéneos, todos son el resultado de fuerzas mecánicas externas transferidas al contenido intracraneal. El daño que resulta incluye una combinación de contusiones y hematomas focales, así como de cizallamiento de tractos de sustancia blanca (daño axonal difuso) con edema cerebral e inflamación.
– Los mecanismos de cizallamiento conducen a daño axonal difuso, que se observa anatomopatológicamente y en las neuroimágenes como múltiples lesiones pequeñas dentro de tractos de sustancia blanca. Los pacientes con daño axonal difuso severo típicamente se presentan con coma profundo sin aumento de la presión intracraneal y con frecuencia tienen un peor pronóstico.
– Las contusiones cerebrales focales son las lesiones más frecuentemente encontradas. Las contusiones se ven comúnmente en la base de las áreas frontales y temporales. En la coalescencia de contusiones cerebrales se pueden producir hematomas intraparenquimatosos.
– Los hematomas extra-axiales se encuentran por lo general cuando las fuerzas están distribuidas a la bóveda craneal y a las capas cerebrales más superficiales. Estos incluyen hematomas epidural, subdural, y hemorragia subaracnoidea.
o En los adultos, los hematomas epidurales se asocian típicamente a los vasos durales como la arteria meníngea media, y casi siempre se asocian a una fractura de cráneo. Tienen una forma lenticular y tienden a no asociarse con daño cerebral subyacente. Por esta razón, los pacientes que sólo tienen hematomas epidurales en la TC puede tener un mejor pronóstico que los individuos con otros tipos de hemorragias traumáticas.
o Los hematomas subdurales resultan del daño a las venas puente, que drenan las superficies corticales cerebrales a senos venosos durales, o desde la eclosión de contusiones corticales superficiales. Tienden a tener forma de medialuna y con frecuencia están asociados a lesión cerebral subyacente.
Aproximadamente una tercera parte de los pacientes con TEC grave desarrollan coagulopatía, que se asocia con un mayor riesgo de hemorragia, pobres resultados neurológicos y muerte.
Mientras que la coagulopatía puede resultar de medicamentos del paciente, el TEC también produce coagulopatía a través de la liberación sistémica del factor tisular y fosfolípidos cerebrales en la circulación que conducen a coagulación intravascular inadecuada y coagulopatía de consumo.
Lesiones cerebrales secundarias: Corresponden a los mecanismos de cascada de daño molecular que se inician en el momento del trauma inicial, y continúan durante horas o días. Estos mecanismos incluyen: excitotoxicidad mediada por neurotransmisores, desbalances electrolíticos, disfunción mitocondrial, respuestas inflamatorias, apoptosis, isquemia secundaria por vasoespasmo, daño vascular.
Estos llevan a su vez a la muerte celular neuronal, así como a edema cerebral y aumento de la presión intracraneal que puede además agravar el daño cerebral. Estas diversas vías de lesión celular han sido objeto de un extenso estudio preclínico en el desarrollo de tratamientos neuroprotectores para prevenir la lesión cerebral secundaria en el TEC. No existen estudios clínicos que hayan demostrado que estas estrategias tengan un claro beneficio en pacientes.
Sin embargo, un aspecto crítico para mejorar el daño cerebral secundario después del TEC es la evitación de daños cerebrales secundarios que pueden agravar la lesión neuronal en las células vulnerables a causa de la lesión cerebral traumática inicial. Algunos ejemplos son la hipotensión y la hipoxia (que disminuyen la entrega de oxígeno y glucosa al cerebro), fiebre y convulsiones (que pueden aumentar aún más la demanda metabólica), y la hiperglicemia (que puede exacerbar los mecanismos de lesión).
- Diagnóstico y diagnósticos diferenciales
Los efectos del TEC pueden variar desde discapacidad grave y permanente a déficits funcionales y cognitivos más sutiles que a menudo no son detectadas durante la evaluación inicial. Estos problemas pueden surgir días más tarde. Algunos síntomas como cefalea, mareos, confusión y fatiga tienden a comenzar inmediatamente después de la lesión, pero desaparecen con el tiempo.
Con respecto al diagnóstico diferencial, las manifestaciones neurológicas pueden imitar diferentes patologías del sistema nervioso central, como intoxicaciones, accidente cerebro vascular, encefalopatía hipóxico-isquémica, causas metabólicas, infecciones, etc., por lo tanto, el antecedente de traumatismo o la presencia de lesiones del cuero cabelludo generalmente aclaran el diagnóstico.
Se debe realizar una anamnesis completa. Se debe preguntar por el mecanismo de lesión, energía involucrada, pérdida de conciencia y su duración, presencia de convulsiones, signos de focalización, vómitos, amnesia del evento, entre otras manifestaciones neurológicas. También se debe recopilar información sobre la presencia de síntomas físicos, cognitivos, emocionales y relacionados con el sueño.
Si cualquiera de los siguientes síntomas aparece de forma repentina o empeoran con el tiempo después de una lesión cerebral traumática, especialmente dentro de las primeras 24 horas, las personas deben consultar a un servicio de urgencia.
Las personas deben buscar atención médica inmediata si experimentan cualquiera de los siguientes síntomas:
– Pérdida o cambio en la conciencia desde unos pocos segundos a unos pocos horas
– Disminución del nivel de conciencia, por ejemplo, dificultad para despertar
– Convulsiones
– Dilatación pupilar asimétrica o visión doble
– Rinorraquia u otorraquia
– Náuseas y vómitos
– Déficit neurológico, por ejemplo, disartria, paresia de extremidades o cara, pérdida del equilibrio
Otros síntomas comunes que deben ser monitoreados incluyen:
– Leve a profunda confusión o desorientación
– Problemas para recordar, concentrarse o tomar decisiones
– Cefalea
– Mareos, vértigo o pérdida del equilibrio o de la coordinación
– Problemas sensoriales, tales como visión borrosa, zumbido en los oídos, mal sabor en la boca
– Sensibilidad a la luz o el sonido
– Cambios de humor, agitación u otro comportamiento inusual
– Sentimientos de depresión o ansiedad
– Fatiga o somnolencia; falta de energía o motivación
– Cambios en los patrones del sueño
El diagnóstico de TEC en niños puede ser un desafío, ya que pueden ser incapaces de informar a otros que se sienten diferentes. Un niño con TEC puede mostrar los siguientes signos o síntomas:
– Cambios en la alimentación o en lactancia
– Llanto persistente, irritabilidad o inquietud
– Cambios en la capacidad de poner atención; falta de interés en un juguete o actividad favorita
– Cambios en la forma en que el niño juega
– Cambios en los patrones de sueño
– Tristeza o depresión
– Pérdida de una habilidad, como el control de esfínteres
– Pérdida del equilibrio o inestabilidad al caminar
– Vómitos
- “Valoración rápida” inicial del paciente.
Debido a que las lesiones traumáticas cerebrales son generalmente emergencias, los médicos necesitan evaluar la situación rápidamente. Todos los pacientes deben ser evaluados mediante la Escala de Coma de Glasgow (Tabla 1), con énfasis en la respuesta motora. Esta evaluación debe ser realizada una vez que el paciente ha sido reanimado y su aplicación e interpretación es evolutiva, dado que el deterioro es común en las primeras horas después del trauma. Una puntuación GCS de 13 a 15 se considera TEC leve, de 9 a 12 se considera TEC moderado, y 8 o menos es un TEC grave.
La GCS es universalmente aceptada como una herramienta para la clasificación del TEC debido a su simplicidad, reproducibilidad, y valor predictivo para el pronóstico global. Sin embargo, está limitada por factores de confusión tales como la sedación, parálisis, intubación endotraqueal e intoxicaciones, por tanto se deben consignar. Estos problemas suelen ser especialmente importantes en los pacientes con una baja puntuación.
También se debe realizar una evaluación del tamaño y reactividad pupilar, ya que la presencia de una anisocoria mayor a 2 mm asociada a una midriasis unilateral o es indicativa de compromiso del III par craneal y debe asumirse como secundaria a una herniación uncal, lo que representa una urgencia neurológica. A su vez, cualquier anomalía en los reflejos pupilares directo y consensual también es sinónimo de complicación grave, de compromiso del mesencéfalo, habitualmente por una herniación cerebral.
Un examen neurológico completo se debe realizar lo más precozmente posible para determinar la severidad clínica del TEC. Se evaluaran las habilidades motoras y sensoriales y el funcionamiento de uno o más nervios craneales. También se pueden realizar pruebas de audición y habla, coordinación y equilibrio, estado mental y observar cambios de humor o comportamiento, entre otras.
- “Pruebas Diagnósticas”
Se debe solicitar hemograma, electrolitos, glicemia, pruebas de coagulación, alcoholemia y toxicología urinaria.
- “Exámenes complementarios”
La imagenología ayuda a determinar el diagnóstico y el pronóstico de un paciente con traumatismo cerebral. A los pacientes con TEC leve se les puede realizar una radiografía de cráneo AP, lateral y proyección de Towne para ver si existe una fractura de hueso o una radiografía cervical para descartar inestabilidad de la espina cervical. El paciente debe permanecer inmovilizado en la camilla y con cuello inmovilizador hasta que el personal médico tenga la seguridad de que no existe ningún riesgo de lesión en la espina cervical. Para casos moderados a graves, la tomografía computarizada (TC) es la modalidad de imagen preferida en la fase aguda del trauma craneal y debe realizarse lo más rápidamente posible. La TC detectará fracturas de cráneo, hemorragias, hematomas, contusiones, patrones focales o difusos de daño axonal y edema cerebral. Las guías actuales recomiendan TC cerebral en todos los pacientes con TEC con una escala de coma de Glasgow de 14 o inferior.
El seguimiento con TC debe realizarse si hay algún deterioro clínico. Aunque no existe una clara indicación para el seguimiento de rutina con TC en ausencia de cambios clínicos o cambios en los parámetros fisiológicos tales como la PIC, la práctica varía considerablemente en este sentido.
Existen dos escalas de clasificación basadas en TC que se utilizan actualmente:
– La escala Marshall utiliza hallazgos de la TC para clasificar las lesiones en seis categorías diferentes. Ha demostrado predecir con precisión el riesgo de aumento de la presión intracraneal y los resultados en adultos, pero carece de reproducibilidad en pacientes con múltiples tipos de lesión cerebral.
– La escala de Rotterdam es una clasificación más reciente desarrollada para superar las limitaciones de la escala Marshall. Ha mostrado resultados prometedores, pero requiere una mayor validación.
La resonancia magnética (RM) puede usarse luego de la evaluación y tratamiento inicial del paciente con traumatismo cerebral. La RM puede mostrar más detalle que los rayos X o los TC. Desafortunadamente, la RM no es ideal como imagen de rutina en pacientes con TEC cuando llegan a una sala de emergencia debido a que es un procedimiento lento y no está disponible en todos los hospitales.
- “Criterios de Ingreso”, que permiten conocer cuál será el destino del paciente.
Existen diferentes escenarios clínicos:
– Escenario 1: Pacientes con GCS=15
Pacientes sin factores de riesgo (Tabla 2) de lesión intracraneana, deben ser observados por 2 a 4 horas desde ocurrido el trauma. Además se debe solicitar radiografía de cráneo y si evolucionan favorablemente en ese período, pueden ser dados de alta a domicilio con indicación de reposo y observación. Si presentan factores de riesgo o si presentan signos de alarmas (Tabla 3) durante la observación inicial se debe realizar un TC y deben ser evaluados por el especialista. Si tienen TC normal y evolucionan favorablemente, poder ser dados de alta después de un periodo de 4 a 6 horas, con las mismas indicaciones.
– Escenario 2: Pacientes con GCS 13-14
Todos deben ser evaluados mediante TC y se debe realizar observación estricta por al menos 4 a 6 horas. Hospitalizar dependiendo de los resultados del TC.
– Escenario 3: Pacientes con GCS 9-12
Todos deben ser evaluados mediante TC y ser hospitalizados en Unidad de Pacientes Críticos, mantenerse en observación y ser re-evaluados mediante TC si se presenta algún deterioro.
– Escenario 4: Pacientes con GCS ≤ 8
Todos deben ser evaluados mediante TC y además se debe realizar una evaluación neuroquirúrgica de forma urgente.
“Algoritmo diagnóstico”
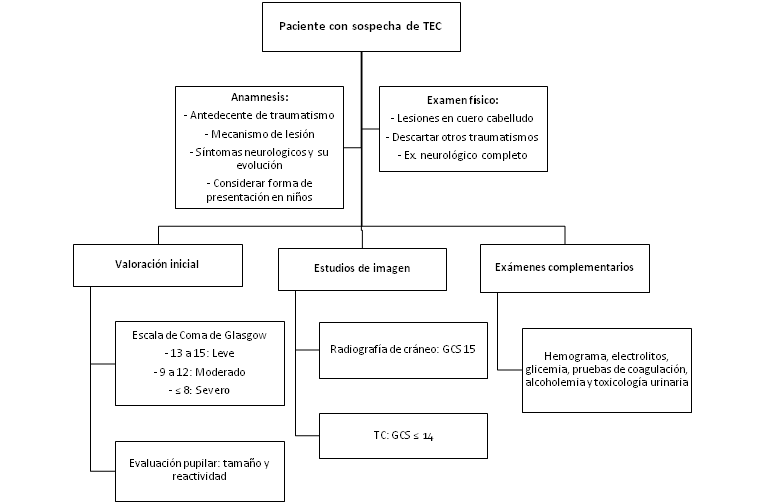
- Manejo
Manejo inicial (Atención pre-hospitalaria y reanimación inicial)
Se debe que considerar que con frecuencia estos pacientes se encuentran politraumatizados, por lo que el manejo inicial de todo paciente con TEC moderado o severo se basa en el ABCDE de la reanimación.
La principal meta del manejo prehospitalario del TEC es prevenir la hipotensión y la hipoxia.
- Manejo de la vía aérea
Mantener vía aérea permeable.
La intubación endotraqueal precoz generalmente está recomendada para pacientes con GCS menor o igual a 8 por personal bien entrenado.
- Ventilación
Administración de oxígeno para saturación de oxígeno del 95%. Mantener normoventilación (PaCO2 entre 35 y 40 mmHg), evitando tanto la hipo como la hiperventilación.
Se deben descartar lesiones con riesgo vital inmediato como neumotórax a tensión, hemotórax masivo y tórax inestable.
- Circulación y control de la hemorragia
Se debe realizar una adecuada reposición de fluidos mediante el uso de cristaloides isotónicos. No se recomienda el uso de ringer lactato, por su baja osmolaridad, y tampoco las soluciones glucosadas, salvo en hipoglicemia. La reanimación debe mantenerse hasta recuperar PA sistólica > 90 mmHg.
Se debe realizar un adecuado control de la hemorragia. Las heridas de cuero cabelludo son una fuente importante de hemorragias.
Manejo médico-quirúrgico del TEC moderado-grave
Medidas generales
- – Posición de la cabeza en 30 grados de inclinación en pacientes hemodinámicamente estables, en línea media.
- – Garantizar euvolemia y evitar hipotensión mediante el aporte de soluciones isotónicas y/o derivados sanguíneos según necesidad. En caso de requerirse se pueden utilizar drogas vasoactivas, siendo el fármaco de primera elección la noradrenalina.
- – Optimizar el aporte de oxígeno cerebral, manteniendo Sa02 > 94% y PaO2 > 60 mmHg, normocapnia y niveles de hemoglobina ≥ 10 gr/dL.
- – Analgesia mediante el uso de AINEs y/u opiáceos en pacientes hemodinámicamente estables.
- – Sedación en caso de agitación psicomotora o GCS ≤ 8.
- – Control de la glicemia, evitando tanto la hipoglicemia como la hiperglicemia. Se recomienda mantener la glicemia menor de 180 mg/dL. No se recomienda el control estricto de la glicemia mediante el uso insulina de forma agresiva, dado que incrementa el riesgo de hipoglicemia y se asocia a una mayor mortalidad.
- – Control de la natremia, manteniendo una natremia entre 140 y 155 mEq/L, dado que niveles menores aumentan la PIC.
- – Control de la temperatura. Mantener la normotermia mediante el uso de antipiréticos, dispositivos superficiales de enfriamiento o incluso catéteres endovasculares para control de la temperatura.
- – Anticonvulsivantes de manera profiláctica durante 7 días (fenitoína, ácido valproico, levetiracetam). El uso de fármacos antiepilépticos en el tratamiento agudo del TEC ha demostrado que reduce la incidencia de convulsiones precoces, pero no impide el desarrollo posterior de epilepsia. Las razones para prevenirlas incluyen el riesgo de status epiléptico, que tiene una alta tasa de mortalidad en este contexto, y el potencial de las convulsiones de agravar una injuria sistémica. Además, convulsiones recurrentes pueden aumentar el flujo sanguíneo cerebral y por lo tanto podrían aumentar la PIC.
- – Nutrición, se recomienda nutrición enteral precoz y considerar vía parenteral cuando no es posible vía enteral. Evaluación para gastrostomía.
- – Kinesioterapia motora y respiratoria en todos los pacientes.
- – Prevención de trombosis venosa profunda (TVP). El riesgo aumentado de TVP en pacientes con TEC puede ser reducido mediante el uso de tromboprofilaxis mecánica usando compresiones neumáticas intermitentes. El uso de agentes antitrombóticos debe ser individualizado de acuerdo al grado de sangrado intracraneal y el riesgo de TVP.
Tratamiento quirúrgico
Las indicaciones de cirugía de urgencia luego de un TEC severo están basadas en el estado neurológico, usualmente definido por el GCS, y en los hallazgos en el TC.
- – Hematoma extradural ― si es mayor a 30 cm2 o sintomático. La cirugía de evacuación de forma urgente está recomendada en pacientes con hematoma extradural agudo y en coma (GCS≤8) que tiene anormalidades pupilares (anisocoria).
- – Hematoma subdural agudo ― si el espesor mayor a 10 mm o existe desviación de la línea media >5 mm. Considerar en deterioro clínico (disminución de 2 o más puntos en la GCS), progresión de la lesión, aumento de la PIC.
- – Lesiones focales supratentoriales ― En lesiones hemisféricas las indicaciones quirúrgicas no están bien definidas. Las guías recomiendan craneotomía con evacuación si la hemorragia excede los 50 cm3 en volumen, o si el GCS es 6 a 8 en una paciente con una hemorragia frontal o temporal mayor a 20 cm3 con desviación de la línea media de al menos 5 mm y/o compresión cisternal en el TC.
- – Lesiones de fosa posterior ― la cirugía está recomendada cuando hay evidencia de efecto de masa significativo.
- – Hundimiento de cráneo ― si es expuesto o mayor a 10 mm.
- – Heridas penetrantes ― Generalmente está recomendado el debridamiento superficial y cierre de la duramadre para evitar fuga de LCR. Se deben retirar cuerpos extraños y restos óseos.
En la craniectomía descompresiva una porción substancial del cráneo es removida para reducir el aumento de la PIC. Puede ser realizada en combinación con el procedimiento de evacuación o como tratamiento primario del aumento de la PIC. El uso de esta técnica es controversial y su eficacia en TEC es desconocida.
Monitorización
- – Monitoreo básico: oximetría de pulso, capnografía, electrocardiográfico continuo, frecuencia cardiaca y respiratoria, temperatura, monitoreo continuo de PA, diuresis horaria.
- – Laboratorio básico: ELP, glicemia, hematocrito/hemoglobina, plaquetas, pruebas de coagulación, gasometría arterial y venosa.
- – Neuromonitoreo multimodal:
- – Presión intracraneana (PIC): en todos los pacientes con TEC grave o TC anormal con evidencia de efecto de masa por lesiones como hematomas o contusiones. Un catéter ventricular conectado a un transductor medidor de presión es el método de monitorización de la PIC más preciso y costo-efectivo y tiene una ventaja terapéutica permitiendo el drenaje de LCR para tratar aumentos en la PIC. Todo paciente con una PIC mayor a 20 mmHg requiere de una evaluación diagnóstica o una intervención terapéutica.
- – Presión de perfusión cerebral (PPC): el umbral sugerido es alrededor de 60 mmHg, se debe evitar una PPC menor de 50 mmHg y mayor de 70 mmHg.
- – Saturación venosa yugular de oxígeno (SjVO2): evitar caída bajo 55%.
- – Considerar la monitorización electroencefalográfica.
Manejo de la hipertensión intracraneana (HIC)
La mayoría de las guías y protocolos clínicos recomiendan iniciar el tratamiento de la hipertensión intracraneana cuando la PIC aumenta alrededor de 20 mmHg. Generalmente la primera medida es el drenaje ventricular. El LCR debe ser removido a un velocidad de aproximadamente 1 a 2 mL/minuto, por dos a tres minutos a la vez, con intervalos de dos a tres minutos, hasta que se haya logrado una PIC satisfactoria (PIC <20 mmHg) o hasta que ya no se obtenga fácilmente LCR. La eliminación lenta también puede ser lograda por drenaje gravitacional pasivo a través de la ventriculostomía.Si la PIC se mantiene elevada, otras intervenciones incluyen terapia osmótica, hiperventilación y sedación. En casos refractarios, coma barbitúrico, hipotermia inducida y craniectomía descompresiva pueden ser consideradas. Terapia osmótica ― La inyección intravascular de agentes hiperosmolares (manitol, solución salina hipertónica) crea un gradiente osmolar, con traspaso de agua a través de la barrera hematoencefálica. Esto conduce a una disminución en el volumen intersticial y disminución de la PIC.- El manitol es el agente más utilizado para el de control de la PIC y también se ha demostrado que mejora el flujo sanguíneo cerebral. Se administra en bolos de 0,25 a 1 g/kg cada cuatro a seis horas según sea necesario. Se requiere seguimiento de la osmolaridad sérica (<320 mmol/L), balance hídrico, función renal y electrolitos. – La solución salina hipertónica se está utilizando cada vez más en este contexto, pero con diferentes volúmenes y tonicidad (3 a 23,4%), y como bolo o en infusión continua. Se requiere más estudio para clarificar el rol de la solución salina hipertónica en el manejo de la hipertensión intracraneana. Hiperventilación ― La hiperventilación puede ser usada para reducir la PIC. Con esta medida la PaCo2 disminuye lo que conduce a vasoconstricción cerebral, que a su vez se traduce en una disminución del volumen sanguíneo cerebral y de la PIC. Sin embargo, la vasoconstricción inducida también puede causar isquemia secundaria y, por lo tanto, puede empeorar los resultados. Se recomienda evitar la hiperventilación, especialmente en la fase aguda (las primeras 24 a 48 horas) después del TEC. La hiperventilación leve a moderada puede ser considerada en etapas posteriores, pero una PaCO2 menor a 30 mmHg debe evitarse. Sedación ― Los medicamentos sedantes y la parálisis farmacológica se utilizan a menudo en los pacientes con TEC grave y PIC elevada. La razón es que una sedación adecuada puede disminuir la PIC mediante la reducción de la demanda metabólica. La sedación puede también mejorar la asincronía ventilatoria y mitigar las respuestas simpáticas de hipertensión y taquicardia. Estos posibles efectos beneficiosos son contrarrestados por el potencial de estos fármacos para provocar hipotensión y vasodilatación cerebral que, a su vez, pueden agravar la hipoperfusión cerebral y elevar la PIC.- El propofol tiene una corta duración de acción que permite una evaluación neurológica clínica de forma intermitente y también tiene efectos neuroprotectores. Se ha visto que parece estar asociado con un mejor control de la PIC en comparación a la sedación con morfina. Sin embargo, los pacientes con TEC están en particular riesgo de desarrollar el raro pero potencialmente fatal síndrome de infusión de propofol (acidosis metabólica grave, rabdomiolisis, hiperpotasemia, insuficiencia renal y colapso cardiovascular). Como resultado de ello, se sugiere que cuando se utiliza en TEC, la velocidad de infusión de propofol no exceda de 4 mg/kg por hora y que los pacientes sean monitorizados para detectar cambios en el ECG, acidosis láctica y elevaciones de la CK.- El coma barbitúrico se ha usado tradicionalmente en este contexto y sigue siendo una opción de tratamiento para la elevación de la PIC resistente a otras terapias. Sin embargo, hay pocos datos clínicos para apoyar su uso. Se ha visto que tanto el pentobarbital como el tiopental se asocian a un mejor control de la PIC. El pentobarbital se administra en una dosis de carga de 5 a 20 mg/kg en bolo, seguido de 1-4 mg/kg por hora. – Otros agentes sedantes también se pueden usar, aunque ninguno de ellos ha sido bien estudiado en pacientes con TEC grave. Estos incluyen las benzodiacepinas o los opiáceos (por ejemplo, midazolam, morfina, fentanilo) usados individualmente o en combinación con barbitúricos y/o bloqueo neuromuscular.En ausencia de ensayos clínicos para apoyar el uso de cualquier protocolo específico, se sugiere que el uso de la sedación sea individualizada de acuerdo a las circunstancias clínicas específicas y que la elección del agente sea individualizada de manera similar, teniendo en cuenta también la experiencia local. Hipotermia terapéutica ― La hipotermia inducida ha sido propuesta como tratamiento para el TEC en base a su potencial para reducir la PIC, así como para proporcionar neuroprotección y prevenir las lesiones cerebrales secundarias. Los resultados obtenidos en los estudios no son concluyentes y existe variabilidad con respecto a la profundidad y duración de la hipotermia que no permite sacar conclusiones. Por lo tanto, la hipotermia terapéutica debe limitarse a pacientes con niveles elevados de la PIC resistente a otras terapias. A continuación se presenta un flujograma que integra las recomendaciones generales sobre el manejo del paciente con TEC grave e HIC.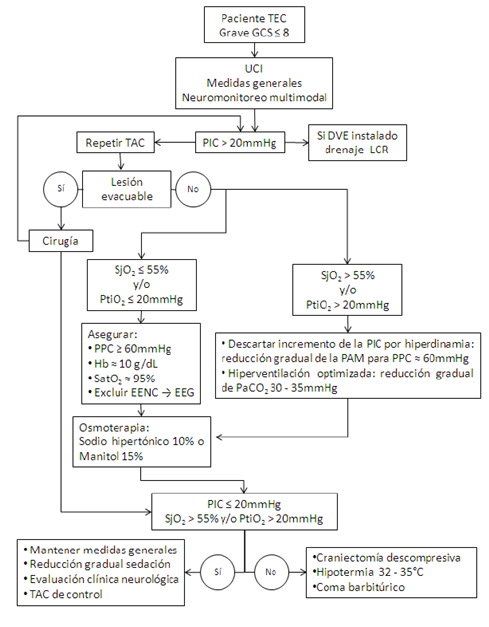
Guía Clínica AUGE: Traumatismo Cráneo Encefálico moderado o grave. Ministerio de Salud. 2013
Tratamiento neuroprotectorHasta la fecha, no existen agentes neuroprotectores o estrategias (incluyendo la hipotermia inducida) que hayan demostrado que produzcan un mejor resultado. Algunos agentes que están siendo investigados incluyen la progesterona intravenosa, el magnesio, el oxígeno hiperbárico, la ciclosporina y la eritropoyetina.
Conclusión
El TEC es una patología con una elevada morbimortalidad, correspondiendo a la primera causa de muerte y discapacidad en la población menor de 45 años de edad. Las principales etiologías son las caídas, principalmente en edades extremas, y los accidentes de tránsito, que se asocian a una mayor severidad y mortalidad. Con respecto a la fisiopatología, sabemos que existen las lesiones cerebrales primarias que ocurren al momento del trauma y que no se pueden evitar, y las lesiones cerebrales secundarias que se van desarrollando con el tiempo y pueden ser evitables mediante un manejo adecuado. El diagnóstico del TEC a menudo no representa un gran desafío, debido a que frecuentemente existe el antecedente del trauma. Sin embargo, en ciertos casos, es importante realizar un diagnóstico diferencial con otras patologías que afectan el SNC como los accidentes cerebro-vasculares, infecciones, entre otras. La valoración inicial del paciente debe ser rápida y se realiza mediante la Escala de Coma de Glasgow que clasifica el TEC en leve, moderado y severo. También es importante la evaluación pupilar, ya que su alteración puede significar una herniación cerebral. El examen complementario más importante corresponde a la tomografía computarizada que debe realizarse en todos los pacientes con GCS ≤ 14 o con GCS=15 asociado a factores de riesgo. El manejo inicial del TEC se basa en el ABCDE de la reanimación ya que con frecuencia los pacientes se encuentran politraumatizados. Dentro del manejo del TEC moderado-grave es importante la hospitalización en UCI, adoptando múltiples medidas generales, la evaluación neuroquirúrgica, la monitorización continua, incluyendo el neuromonitoreo, y el manejo de la hipertensión intracraneana.
Referencias bibliográficas
- – Apunte “Evaluación y manejo del paciente con TEC”. Sociedad de Neurocirugía de Chile. Servicio de Neurocirugía, Hospital de Puerto Montt.
- – Carney N, Totten A, O’Reilly C, et al. Guidelines for the Management of Severe Traumatic Brain Injury 4th Edition. Brain Trauma Foundation. September 2016.
- – Evans, RW. Concussion and mild traumatic brain injury. UpToDate. 2015.
- – Guía Clínica AUGE: Traumatismo Cráneo Encefálico moderado o grave. Ministerio de Salud. 2013.
- – Hemphill JC, Phan N. Management of acute severe traumatic brain injury. UpToDate. 2015.
- – Hemphill JC, Phan N. Traumatic brain injury: Epidemiology, classification, and pathophysiology. UpToDate. 2013.
- – Ortiz, Armando. Traumatismo Encefalocraneano (TEC) Una puesta al día. Rev. Med. Clin. Condes. 2006: 17(3): 98-105.
- – Traumatic Brain Injury: Hope Through Research. National Institute of Neurological Disorders and Stroke (NINDS). 2010.
Anexos
Tabla 1: Escala de Coma de Glasgow
|
Parámetro |
Respuesta |
Puntaje |
|
Apertura ocular |
Espontánea |
4 |
|
Respuesta a la orden verbal |
3 |
|
|
Respuesta al dolor |
2 |
|
|
Sin apertura ocular |
1 |
|
|
Respuesta verbal |
Orientada |
5 |
|
Confusa |
4 |
|
|
Palabras inapropiadas |
3 |
|
|
Sonidos incomprensibles |
2 |
|
|
Sin respuesta verbal |
1 |
|
|
Respuesta motora |
Obedece órdenes |
6 |
|
Localiza al dolor |
5 |
|
|
Retirada al dolor |
4 |
|
|
Flexión al dolor |
3 |
|
|
Extensión al dolor |
2 |
|
|
Sin respuesta motora |
1 |
Tabla 2: Factores de riesgo
|
Antecedentes del accidente |
Mecanismos de alta energía Muerte de uno de los accidentados Sospecha de lesión penetrante de cráneo |
|
Antecedentes del paciente |
Edad > 65 años Epilepsia Tratamiento anticoagulante oral o coagulopatía previa Antecedente de enfermedad neuroquirúrgica previa Alcoholismo crónico Abuso de drogas Paciente sin apoyo social |
|
Elementos de la anamnesis |
Segunda consulta Pérdida de conciencia mayor a 5 minutos Cefalea intensiva y progresiva Vómitos explosivos Presencia de convulsiones Amnesia pre o post traumática |
|
Hallazgos del examen físico y neurológico |
Presencia de déficit neurológico Presencia de otorragia Presencia de otorraquia o rinorraquia Signos de fractura de base de cráneo (ojos de mapache, signo de Battle) Agitación psicomotora |
|
Estudio radiológico |
Presencia de fractura de cráneo |
Guía Clínica AUGE: Traumatismo Cráneo Encefálico moderado o grave. Ministerio de Salud. 2013
Tabla 3: Signos de alarma
|
– Deterioro progresivo de conciencia y/o disminución de GCS ≥ 2 puntos – Signos de focalidad neurológica – Cefalea progresiva – Vómitos explosivos recurrentes – Agitación psicomotora – Convulsiones |
Guía Clínica AUGE: Traumatismo Cráneo Encefálico moderado o grave. Ministerio de Salud. 2013
