Definiciones
Podemos definir accidente cerebrovascular (ACV) como un síndrome clínico caracterizado por síntomas y/o signos neurológicos focales causados por una interrupción abrupta del flujo sanguíneo a un área específica del cerebro. Estos síntomas se caracterizan por desarrollarse en un periodo breve de tiempo y permanecer por más de 24 hr.
El ACV puede ser origen isquémico, si la interrupción del flujo sanguíneo es causada por una obstrucción del vaso correspondiente, o de origen hemorrágico, si es por una rotura de éste.
El Accidente Isquémico Transitorio (AIT) es una entidad de similares características clínicas y etiologías al ACV de origen isquémico, salvo en que la duración de los síntomas es menor a 24 hr, y será tratado en un apartado al final del capítulo.
Epidemiología
Según las últimas estadísticas del Departamento de estadísticas e información de salud (DEIS), dependiente del ministerio de salud (MINSAL), en el año 2011 los ACV fueron la primera causa aislada de mortalidad tanto en hombres como mujeres; lo que evidencia el impacto de esta patología y propone un desafío tanto en su prevención como su manejo, siendo en este último de suma importancia los cuidados otorgados durante una atención de urgencia.
Dentro de los factores de riesgos se evidencia que se trata de los mismos factores asociados a enfermedades cardiovasculares, considerando tanto factores no modificables (edad y sexo masculino) como modificables (tabaquismo, alcohol, obesidad, sedentarismo, dislipidemia y diabetes mellitus). En este grupo de pacientes destaca con particularidad, la alta asociación con hipertensión arterial y la fibrilación auricular.
Anatomía
La sangre llega al cerebro a través de dos sistemas arteriales: (1) El sistema anterior que proviene de la arteria carótida interna y sus 2 ramas principales son la a. cerebral anterior y media, a través de las cuales se irriga el 80% del territorio encefálico que incluye: retina, nervio óptico y los lóbulos frontal, parietal (2/3 anteriores), temporal (región anterior) y los núcleos de la base (putamen, brazo anterior de la cápsula interna, lenticular y cápsula externa).
(2) el sistema posterior, proveniente de las arterias vertebrales, que dan origen a las arterias cerebrales posteriores. La circulación posterior irriga el 20% del parénquima, dentro de lo cual se incluye el tronco encefálico (muy importante por su función critica para lograr la vigilia y otras funciones vitales como el centro respiratorio y la regulación del ritmo cardiaco), cerebelo, tálamo, núcleos auditivos y vestibulares, lóbulo temporal (por media y posterior) y occipital.
Cada arteria cerebral presenta un territorio específico de irrigación, de manera que el déficit de flujo sanguíneo a través de alguna, generará un cuadro clínico específico y concordante con el territorio de la arteria (o rama) que irriga. Para ver la asociación entre arteria y clínica ver el cuadro 61.1 Clínica del infarto cerebral establecido según su localización (Molina et cols 2015).
La magnitud del daño causado por el ACV depende no solo de la arteria afectada, sino también de la presencia de colaterales. Se debe recordar existen conexiones entre la circulación anterior y posterior y entre la circulación del hemisferio derecho e izquierdo a través del polígono de Wills, lo que permite muchas veces mantener un flujo sanguíneo mínimo a través de la red de colaterales pese a tener una obstrucción de una arteria de mayor calibre.
Fisiopatología
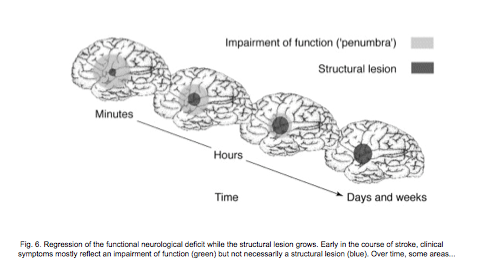
El ACV resulta de la interrupción del flujo sanguíneo al parénquima cerebral, en virtud del cual se interrumpen los suministros de oxígeno y glucosa hacia las células cerebrales, si el aporte de flujo diminuye la célula entra en un estado de hibernación, donde detiene su metabolismo y su actividad eléctrica, pero sin daño en sus estructuras celulares, por lo que célula con potencial de recuperar su función si se restablece el flujo sanguíneo. Sin embargo, si la interrupción del flujo sanguíneo es sostenida o sobrepasa un umbral crítico, se echan a andar mecanismos de exitotoxicidad, con daño en las membranas celulares, que finalizan con la muerte celular y la pérdida definitiva de su función.
En el siguiente diagrama se muestra como en un tiempo precoz, el territorio afectado por la isquemia se divide en zonas: la zona central que presenta desde el inicio una lesión estructural, con muerte neuronal por un flujo sanguíneo muy disminuido (bajo el umbral crítico). La segunda zona es la zona de “penumbra” donde las células se encuentran en hibernación y tienen potencial de recuperar su función. Sin embargo, con el paso de las horas, si la isquemia es persistente la zona de “penumbra” evoluciona hacia el daño celular, con la muerte neuronal definitiva.
Etiología
Dentro los ACV de origen isquémico, las principales etiologías son aterotrombótico, lacunar, cardioembólico, y otros.
Un tercio de los ACV isquémicos corresponde a etiología aterotrombótica, en donde el vaso sanguíneo se obstruye por una trombosis local generada por un accidente de placa aterosclerótica. Por la presencia de flujo turbulento, las áreas más propensas a sufrir accidentes de placa son las bifurcaciones de las ramas principales de la a. cerebral media y el polígono de willis. Como los vasos sanguíneos comprometidos son de mayor calibre, en general los ACV de etiología aterotrombótica presentan una clínica florida, con deficit focales tanto motores como sensitivos y en algunos casos incluso puede presentar compromiso de conciencia o síntomas mas difusos.
Los ACV de etiología lacunar corresponde a la obstrucción de arterias perforantes de pequeño calibre, y se presentan principalmente en las regiones subcorticales (ganglios de la base, tálamo y cápsula interna) y de tronco encefálico. La obstrucción de éstos vasos se debe principalmente a émbolos pequeños o a la lipohialinosis, que corresponde al daño vascular generada por la hipertensión crónica que genera un aumento en el grosor de la pared del vaso y así la obstrucción de su lumen. Por su origen en vasos de menor calibre, el tamaño de los ACV lacunares comprometen desde pocos milímetros hasta 2 cm, y por lo mismo presentan clínica mas focal. Existen múltiples sd clínicos descritos por ACV lacunares, siendo los principales el deficit motor puro, el déficit sensitivo puro y el sd ataxia hemiparesia.
Los ACV de origen cardioembólico corresponden a un cuarto de los ACV isquémico. Éstos se generan por el desprendimiento de un trombo originado en un territorio distal que va a obstruir un vaso sanguíneo encefálico. Las principales fuentes de éstos émbolos son los trombos intrauriculares generador por episodios de fibrilación auricular y trombos intramurales de arterias extracranenas, principalmente la a. carótida común, que generan una embolia arterio-arterial.
Dentro de las otras etiologías de ACV se encuentran: disección de arteria carótida o vertebral, vasconstricción intensa causada por drogas (cocaína, anfetaminas), vasculitis de SNC, estados pro trombóticos (uso de ACO, deficit de proteína C, S, policitemia, sd anti fosfolipido)
DIAGNÓSTICO Y DIAGNÓSTICOS DIFERENCIALES
El diagnóstico del ACV es principalmente clínico a travez de 3 ejes principales (1) la presencia de focalidad neurológica, (2) que pueda ser explicada por la afectación de un territorio arterial, y (3) ausencia de otra causa que explique el cuadro.
Los síntomas de focalidad neurógica son un amplio conjunto de síntomas que dependen del territorio vascular afectado (ver cuadro 1 en anexos). En general corresponden a síntomas negativos, siendo los principales: deficit motor (paresias o plejía), deficit sensitivo (hipoestesia o anestesia), deficit visuales (hemianopsias o cuadrantopsias) y trastornos del lenguaje (afasia, disartria) sin embargo no hay que olvidar otros síntomas mas vagos que también pueden corresponder a déficit focales como lo son el vértigo, mareos, temblor, alteraciones de la marcha y del equilibro, alteraciones de la conducta (desfrontalización), del reconocimiento de objetos (agnosias), entre otros.
Los síntomas se inician de forma súbita o con una progresión rápida, en el curso de minutos a horas y son permanentes en el tiempo, sin fluctuaciones.
Entre los síntomas acompañantes del ACV puede presentarse (pero no es requisito para hacer el diagnóstico): compromiso de conciencia, nauseas, vómitos, cefalea y convulsiones.
Los principales diagnósticos diferenciales son:
-ACV hemorrágiaco
-Sd confusional agudo (por hipoglicemia, infecciones, alteraciones metabolicas, etc) que ocasionalmente puede presentar síntomas focales, pero además siempre presenta compromiso de conciencia fluctuante lo que lo diferencia del ACV
-Migraña con aura, que aunque típicamente el aura corresponde a un síntoma positivo, puede presentar síntomas focales acompañando la cefalea clásica de la migraña,
-Colecciones extradurales (hematoma subdural o epidural), que pueden presentar compromiso de conciencia y síntomas focales según su localización
-Parálisis de Todd (síntomas focales que aparecen tras una convulsión)
Evaluación inicial
La evaluación del paciente se inicia con el ABCDE que siempre debe ser evaluado.
Posteriormente se debe hacer una anamnesis acotada para definir la presencia de síntomas neurológicos y la presencia o no de otros síntomas acompañantes que nos guíen con el diagnóstico diferencial. Se debe hacer especial énfasis en la hora de aparición de los síntomas ya que será determinante en el manejo. Si el paciente no puede dar una anamnesis precisa o se encontraba durmiendo, se debe considerar el tiempo de inicio de los síntomas como el último momento en que fue visto asintomático.
La anamnesis remota se debe enfocar a la presencia de factores de riesgo cardiovasculares, uso de fármacos (especialmente hipoglicemiantes orales), antecedentes de patología en los días previos (infecciones, arritmias, IAM reciente, etc), abuso de sustancias, convulsiones y trauma.
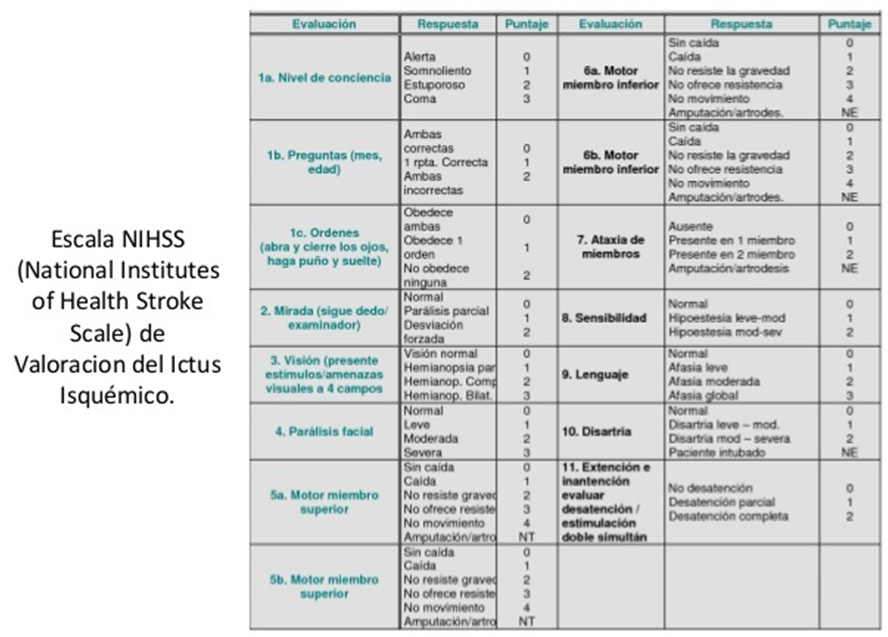
En el examen físico se debe constatar los signos vitales, el nivel de conciencia (con la escala de glasgow o GCS) y hacer énfasis en el examen neurológico. Éste último se puede sistematizar a través del NIHSS (National Institutes of Health Stroke Scale, ver anexo) que permite objetivar la presencia de síntomas focales y al repetirse permite evaluar su evolutibidad en el tiempo. Además se debe realizar un examen físico cardiovascular siendo los principales ítems: soplos carotídeos, ritmo y soplos cardiacos, pulsos distales, lo que nos pudiera orientar en la etiología del ACV.
Dentro de la evaluación inicial se agrega también el ECG y el HGT, que deben realizarse a todo paciente con sospecha de ACV.
Pruebas diagnósticas
A todo paciente con sospecha de ACV se debe realizar un TAC de cerebro sin contraste lo más rápidamente posible. Éste examen permite descartar con una alta sensibilidad y especificidad la presencia de un ACV de origen hemorrágico, que se observa como una imagen hiperdensa (blanca) en el parénquima cerebral. Además se deben buscar imágenes sugerentes de un ACV isquémico precoz como el signo de la cuerda (contraste espontáneo de la ACM), borramiento de los pliegues insulares y la pérdida de diferenciación entre la sustancia gris y la sustancia blanca, sin embargo estos signos no siempre están presentes.
En el caso de tener disponibilidad y que no retrase el manejo, se puede realizar una RNM cerebro protocolo stroke, que permite observar de forma precoz signos específicos de isquemia (zona hiperintensa en difusión). Sin embargo no es un examen ampliamente disponible y su realización demora entre 20 a 30 minutos, (vs 20 segundos que demora realizar un TAC cerebro), y requiere que el paciente se encuentre estable y tranquilo, por lo que no es un examen que deba realizarse de forma obligatoria.
Exámenes complementarios
De forma paralela al estudio y las imágenes iniciales se debe realizar un estudio de laboratorio básico, que incluye hemograma, pruebas de coagulación, glicemia, función renal y electrolitos plasmáticos. Se puede ampliar este estudio según los diagnósticos diferenciales planteados.
De forma posterior, tras la estabilización y manejo inicial del paciente debe realizarse el estudio etiológico del ACV que considera:
A. Estudio de cavidades cardiacas: Ecocardiograma (transtorácico y/o transesofágico) y electrocardiograma.
B. Estudio de vasos sanguíneos (extra e intracraneanos): Ecografía doppler carotidea, angio-TAC o angio-RNM.
Manejo específico
El manejo especifico del ACV isquémico considera todas las terapias dirigidas a desobstruir el vaso sanguíneo comprometido y así restablecer el flujo sanguíneo, para recuperar la función de la zona de penumbra. Por esto es un manejo tiempo dependiente, ya que mientras más precoz sea el tratamiento, mayor será el territorio recuperado.
El único trombolítico autorizado por la FDA para el manejo agudo del ACV es el alterase (tPA), en dosis de 0,9 mg/kg, máximo 90 mg. Se administra el 10% de la dosis como bolo inicial en 1 minuto, y el resto en una infusión continua durante 60 minutos.
El “periodo de ventana terapéutica” es el tiempo en el cual el paciente es candidato a recibir trombolisis ya que la zona de penumbra es aún recuperable. Posterior a este periodo, aunque se administren trombolíticos, la función neurológica ya no es recuperable y además conlleva un mayor riesgo de sangrado, por lo que esta contraindicada la trombolisis. La ventana terapéutica se considera hasta 4.5 hr desde el inicio de los síntomas o la última vez que el paciente fue visto asintomático.
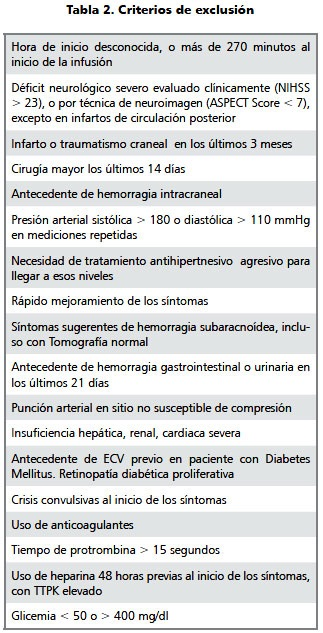
Hay que recordar que la trombolisis no esta exenta de complicaciones, siendo la principal la hemorragia intracraneana. Por ello es contraindicación de recibir trombolíticos todas las condiciones que signifiquen un mayor riesgo de sangrado (revisar anexo).
La trombolisis intraarterial es una alternativa a la trombolisis sistémica que consiste en avanzar una guía hasta la arteria culpable y de forma mecánica o mediante fármacos, destruir el trombo que causa la obstrucción.
Éste método permite ampliar la ventana terapéutica hasta las 6 hr y tiene una menor tasa de complicaciones asociadas, sin embargo requiere de un centro especializado con radiología intervencional, lo cual no es ampliamente disponible en nuestro medio.
Ademas los pacientes deben recibir antiagregación plaquetaria con aspirina (150 – 300 mg/d VO), que debe iniciarse en las primeras 24 hr de iniciado el ACV en los pacientes que no recibirán trombolisis. En los pacientes sometidos a trombolisis la aspirina se debe suspender en las primeras 24 hr y esta contraindicada en caso de hemorragia intracerebral.
Manejo general
Todo paciente en sospecha de ACV isquémico agudo debe ser hospitalizado de manera inmediata. En el caso que el servicio donde consultó no cuente con la posibilidad de acceder a un neurólogo, imágenes (TAC de cerebro sin contraste) o unidad monitorizada, deberá ser trasladado al centro más cercano que cumpla con dichos requerimientos. La hospitalización debe ser en una unidad especializada (UTAC, unidad de tratamiento del ataque cerebrovascular) o en una unidad de intermedio, si ésta no se encuentra disponible. En caso de presentar inestabilidad hemodinámica el paciente debe acceder a una unidad de cuidados intensivos.
En las primeras horas el paciente debe permanecer en reposo absoluto, en régimen cero (para prevenir la aspiración), se debe administrar oxígeno solo en caso de saturación bajo 94% y mantener con monitorización continúa.
El manejo de la hipertensión arterial en el ACV debe realizarse con precaución ya que PA muy elevadas pueden aumentar el riesgo de sangrado y PA bajas o que disminuyen abruptamente pueden empeorar la isquemia, especialmente en la zona de penumbra. Las metas de PA dependerán de si el paciente es candidato para trombolisis o no. En caso de que el paciente sea candidato a trombolisis las metas de PA son PAS <180 y PAD < 110. Si el paciente no recibirá trombolisis se reserva el manejo agudo de la presión arterial solo si la PAS < 220, PAD < 120 o la PAM < 130 mmHg. Para el manejo de la PA se recomiendan fármacos endovenosos, idealmente labetalol que permite una titulación paulatina. Se debe evitar los fármacos VO y las caídas bruscas de la PA.
Otras medidas generales de neuroprotección incluyen: cabecera en 30º, evitar la hipo e hiperoxia, evitar la hipo e hipertensión (metas antes descritas), evitar la hipo e hiperglicemia (meta glicemia 140 -180), evitar la fiebre y manejo activo con antipiréticos en caso de aparición, analgesia adecuada en en caso de dolor, prevenir y tratar las crisis convulsivas.
Se debe evitar la sobrehidratacion de los pacientes para evitar el edema cerebral. Por ello se debe hidratar EV a los pacientes solo en caso de deshidratación y se debe evitar infusiones de mantención en las primeras horas.
Además se debe tener precaución en caso de que el paciente presente agitación psicomotora. Se prefiere evitar la sedación profunda y mantenida. De ser absolutamente necesario se deben utilizar benzodiacepinas de vida media corta para poder hacer seguimiento clínico de los síntomas del paciente.
CONCLUSIONES
El ACV isquémico es una urgencia médica de gran importancia a nivel nacional, que implica no solo una alta mortalidad, sino también una alta tasa de discapacidad asociada, lo que repercute directamente en la calidad de vida de las personas.
Es por esto que paciente que todo paciente que se presente con síntomas focales de inicio precoz y subito se debe sospecha de forma inmediata un ACV y realizar el estudio indicado. Solo así se podrá brindar un tratamiento específico para mejorar el pronostico y funcionalidad de los pacientes.
Finalmente, se debe considerar que en esta patología los detalles marcan la diferencia, de modo que se debe tener una visión integral del paciente, con enfoque es su manejo precoz y posterior hospitalización en centros especializados.
Accidente Isquémico Transitorio (TIA)
Se define TIA como un episodio de síntomas neurológicos focales sin lesión isquemica aguda en la neuroimagen. Antiguamente se planteaba el dignostico de TIA cuando los síntomas focales eran de corta duracion, con resolución espontánea en menos de 24 hr, sin embargo esta definición esta actualmente en desuso, debido a que en todo paciente con síntomas focales se debe sospechar un ACV isquemico y no un TIA, ya que tiene un alto riesgo de presentar isquemia definitiva de no mediar tratamiento médico.
Pese a que los síntomas pueden haber desaparecido al momento de la consulta, los pacientes con un TIA tienen un alto riesgo de recurrencia, por ello se han desarrollado diversas escalas para poder estratificar el riesgo y así definir el estudio y manejo. Una de estas escalas es el ABCD2 (ver anexo) donde puntajes mayores o iguales a 4 tienen un riesgo de 5% de infarto a los 2 días y deben ser estudiados y manejados de forma similar al ACV isquémico.
Además, los pacientes con FA o estenosis carotídea presentan un alto riesgo, independiente de su puntaje ABCD2, por lo que siempre deben ser estudiados.
El manejo de estos pacientes debe ser idéntico al de un ACV isquémico lo que incluye: diagnóstico por imágenes, inicio precoz de tratamiento antitrombótico, mendidas generales de neuroprotección, manejo antihipertensivo agudo en caso necesario, estudio cardiaco y vascular para definir etiología.
ANEXOS
NIHSS (National Institutes of Health Stroke Scale)
Criterios de inclusión y exclusión de trombolisis

Escala ABCD2

Bibliografía
Rosen’s emergency medicine : concepts and clinical practice / editor-in-chief, John A. Marx; senior editors, Robert S. Hockberger, Ron M. Walls ; editors, Michelle H. Biros … [et al.].—8th ed
Ministerio de Salud. (2013). Guía Clínica AUGE, Accidente Cerebro Vascular Isquémico en personas de 15 años y màs. Recuperado el 15 de Septiembre de 2016, de MINSAL: http://web.minsal.cl/portal/url/item/7222754637e58646e04001011f014e64.pdf
Soto, F. (s.f.). Avances en accidente vascular encefálico isquémico. Rev. Med. Clin. CONDES, 19(5), 498 – 503.
Illanes D., S., & Diaz T., V. (2008). Manejo inicial del accidente cerebrovascular (ACV) isquémico agudo. Los detalles hacen la diferencia. Rev Hosp Clin Univ Chile, 19, 119-126.
Molina, T., Calvo, R., Ochoa, J., Jiménez, L., Castilla, S., Montero, F., & Cañadillas, F. (2015). Accidente Cerebrovascular. En F. Montero Pérez, & J. M. L, Medicina de Urgencias y Emergencias (5ta edición ed., págs. 387 – 396). Barcela, España: Elsevier España.
Oliveira Filho, J., & T, M. (20 de Julio de 2016). Antithrombotic treatment of acute ischemic stroke and transient ischemic attack. (S. Kasner, Ed.) Recuperado el 20 de Septiembre de 2016, de UpToDate: www.uptodate.com
J, O. (09 de Diciembre de 2015). Initial assessment and management of acute stroke. (K. Scott, Ed.) Recuperado el 20 de Septiembre de 2016, de UpToDate: www.uptodate.com
Lavados P, S. C. (2007). Incidence, case- fatality rate, and prognosis of ischaemic stroke subtypes in a predominantly Hispanic-Mestizo population in Iquique, Chile (PISCIS project): a community-basaed incidencia study. Lancet Neurology, 6, 140-148.
The National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group. (1995). Tissue Plasminogen Activator for Acute Ischemic Stroke. N Engl J Med, 333, 1581-1588.
Berkhemer, O., Fransen, P., & cols, D. B. (1 de January de 2015). A Randomized Trial of Intraarterial Treatment for Acute Ischemic Stroke. N Engl J Med, 372, 11-20.

