1. Introducción
El shock es una condición de riesgo vital caracterizado por una falla circulatoria aguda. Sus efectos iniciales son reversibles, sin embargo, rápidamente los cambios se tornan irreversibles y evoluciona a falla orgánica múltiple (FOM) y muerte en el 20-50% de los casos según la etiología. (1) Es por ello que cuando un médico sospecha un shock, debe rápidamente evaluar, estabilizar e identificar la etiología para administrar la terapia adecuada y así evitar la FOM y muerte. (2)
Definición
Se define como un estado de desbalance entre un consumo insuficiente de oxígeno para las necesidades celulares y un déficit de aporte, aumento del consumo periférico y/o utilización inadecuada del oxígeno. Sus características más relevantes son: 1) presentar una enorme constelación de posibles etiologías, 2) ser de rápida instalación y de evolución aguda (patología tiempo dependiente) y 3) necesidad de instaurar una terapia precoz. El shock indiferenciado se refiere a la situación donde el shock es reconocido, pero su causa aún no es clara.
Epidemiología
Es un motivo de consulta muy frecuente. Se estima que en Estados Unidos hay 1.200.000 consultas por shock al año en el Servicio de urgencias (SU). Hay muy pocos estudios que evalúen la incidencia de shock indiferenciado en el SU. En un estudio se estimó que el tipo de shock más frecuente era el séptico con un 62%, cardiogénico o hipovolémico en el 16% cada uno y finalmente el shock obstructivo sólo en el 2% de los casos. (2)
Fisiopatología
Existe un desbalance entre el aporte y transporte (DO2) y los requerimientos de oxígeno (VO2) a nivel celular. El transporte de oxígeno se define como el gasto cardiaco (GC) x la concentración de oxígeno en la sangre (CaO2) x 10. La CaO2 depende de la hemoglobina, saturación arterial de oxígeno (SaO2) y una constante que es 1.39. Por su parte el GC se define como volumen sanguíneo (VS) x frecuencia cardiaca (FC). El VS depende de la precarga, postcarga y la contractibilidad cardiaca. De lo anterior, podemos deducir que las variables que juegan un rol protagonista en el shock son la Hb, SaO2, la precarga, postcarga y la contractibilidad cardiaca. La terapia, entonces, debe estar orientada a mejorar estos parámetros.
Tipos de shock
Se expondrán dos formas de clasificar este síndrome. La primera es la clasificación fisiopatológica, donde se enumeran 4 tipos de shock los que están descritos en más detalle en la tabla N°1. Es importante recalcar que en la mayoría de los casos se presentan con más de una forma de shock a la vez. (3) En la tabla N°1 se describe con más detalle el diagnóstico diferencial de los 4 tipos de shock.
- Hipovolémico: Disminución del contenido vascular, ya sea por pérdidas o por acumulación de líquido en un tercer espacio. Clínicamente se caracteriza por presentar una precarga muy disminuida (mucosas secas, vena cava inferior colapsable) y la presencia de una causa que explique la disminución de volumen intravascular.
- Distributivo: Alteración entre el continente y el contenido vascular por vasodilatación. Se puede sub dividir en causas sépticas y no sépticas. Clínicamente presentan hipotensión sin signos de precarga disminuida o postcarga aumentada (edema, yugulares ingurgitadas) con un ventrículo izquierdo (VI) usualmente hiperdinámico.
- Cardiogénico: Secundario a una falla miocárdica intrínseca. Lo más frecuente es cuando se necrosa > 40% del tejido miocárdico, pero no es la única etiología. Clínicamente se puede reconocer en que la hipotensión se acompaña de signos de congestión pulmonar como disnea, crepitaciones y radiografía compatible y de VI hipodinámico.
- Obstructivo: Consecuencia de un fallo miocárdico extrínseco. Clínicamente se presentan con yugulares ingurgitadas pero sin signos de alteración en la pre o postcarga
Otra clasificación se puede realizar según el manejo primario etiológico. Esta clasificación tiene 5 categorías y está resumida en la tabla N°2. A grandes rasgos se separan en causas que requieren infusión de volumen, causas que requieren mejoría de bomba cardiaca ya sea por soporte inotrópico o reversión de la descompensante cardiaca, causas que requieren soporte de volumen y vasopresores, causas que requieren intervención urgente de la obstrucción al gasto cardiaco y, por último, intoxicaciones que requieren un antídoto específico. (4)
2. Diagnóstico
Los hallazgos clínicos asociados al shock indiferenciado en el SU dependen de la etiología de base y de la etapa de presentación en que se encuentre el paciente. Se describen 3 fases clínicas del shock (3):
- Estadio I o shock compensado: Se echan a andar los mecanismos de compensación propios del organismo, los que hacen que los síntomas sean escasos. La taquicardia (frecuencia cardiaca (FC) > 100 lpm) es el signo clínico más precoz seguido de la vasoconstricción periférica.
- Estadio II o shock descompensado: Desarrollo de manifestaciones neurológicas (ansiedad y agitación) y cardiovasculares (taquicardia e hipotensión), oliguria y acidosis metabólica por fallo de los mecanismos de compensación. El cuadro aún puede ser reversible con una terapia precoz enérgica.
- Estadio II o shock irreversible: Disfunción de los órganos diana, que termina produciendo FOM y muerte.
Criterios diagnósticos de shock indiferenciado (3,4):
- Apariencia de enfermedad o estado mental alterado.
- FC > 100 lpm.
- Frecuencia respiratoria (FR) > 22 rmp o PaCO2 < 32 mm Hg.
- Déficit de base arterial < 4 mEq/L o incremento de lactato > 4 mmol/L o > 36 mg/dL.
- Débito urinario < 0.5 mL/kg/hora.
- Duración de hipotensión arterial > 20 minutos.
Valoración inicial
La evaluación inicial como en todo paciente en el SU, es indiferenciada y debe incluir la observación del estado general del paciente, edad, signos vitales y el ABCDEU:
- Permeabilidad de vía aérea: evaluar si puede hablar, manejo de secreciones, presencia de estridor y pronóstico de permeabilidad al futuro.
- Ventilación: Evaluar FR, oximetría de pulso, uso de musculatura accesoria, auscultación pulmonar. Hay que recordar que la oximetría de pulso no es confiable en pacientes con pulsos poco perceptibles o con extremidades muy frías, situaciones frecuentes en los pacientes en shock.
- Circulación: Evaluar FC, llene capilar, presión arterial, palidez, diferencia de temperatura central y periférica, mottling score y presencia de sangrados evidentes.
- Déficit neurológico: Descripción detallada de nivel de lenguaje y conexión con el medio, movilidad de 4 extremidades, pupilas y Glasgow.
- Exponer: Se deben buscar lesiones en áreas menos expuestas como ingle y periné. Además se debe solicitar rápidamente un electrocardiograma (EKG) y hemoglucotest.
- Ultrasonido: Herramienta de suma utilidad. Se describirá posteriormente.
₋ Acciones primarias: Se refieren al primer paso del manejo del shock indiferenciado. Según los hallazgos encontrados en los puntos anteriores, se debe indicar: box monitorizado, posición de Trendelenburg en caso de shock hipovolémico, oxígeno por naricera, por de Venturi al 50% o mascarilla de recirculación, dos accesos venosos permeables, volumen, manejo de vía aérea, control de fiebre y dolor si es necesario y suspensión de fármacos antihipertensivos y diuréticos si corresponde.
Valoración secundaria
Una vez evaluado al paciente e indicado las medidas iniciales, se procede a la evaluación secundaria donde se debe tener como objetivo la identificación etiológica del shock, evaluación de sus manifestaciones clínicas específicas y pronóstico:
- Anamnesis: Cuando sea posible según el contexto del paciente y sus acompañantes, se debe recabar información sobre los siguientes aspectos:
- Antecedentes mórbidos: enfermedades diagnosticadas, cirugías recientes, alergias, fármacos nuevos y de uso habitual, uso de alcohol y drogas y antecedentes familiares o personales de patología cardiaca.
- Historia reciente de trauma, quemaduras, vómitos, diarrea, poliuria, fiebre, disnea, tos con expectoración hemoptoica, puntada de costado, angina, palpitaciones, síncope, focalidad y neurológica.
- Temporalidad: Forma de instauración, duración de los síntomas, si es primera vez que le sucede, presencia de algún desencadentante claro.
- Evolución: Evolutividad sintomática, maniobras terapéuticas utilizadas.
- Examen físico: Los signos clínicos sugerentes de shock carecen de una adecuada sensibilidad y especificidad para esta patología, sin embargo, debido a la gravedad del cuadro, ante la presencia de cualquiera de los siguientes signos, se debe pensar y descartar un shock indiferenciado. (3)
- Examen general: El paciente puede verse pálido, frío, sudoroso y con un pulso débil y rápido. Todos estos hallazgos demuestran mecanismos de compensación adrenérgicos frecuentes en un paciente en shock. Sin embargo, hay que recordar que son hallazgos inespecíficos.
- Taquicardia: Es el signo clínico más precoz que debe hacer sospechar al médico de la presencia de un shock y se define como FC > 100 lpm. Puede incluso ser aislada. Se debe considerar, en primer lugar, que hay cientos de etiologías que pueden explicar la taquicardia, algunas tan frecuentes como la fiebre, el esfuerzo físico o el dolor, por lo que este signo debe ser interpretado en el contexto del paciente. En segundo lugar, actualmente dada la alta frecuencia de uso de betabloqueadores y otras drogas inótropas negativas, la cifra de > 100 lpm se considera un punto de corte relativo, el que necesariamente debe interpretarse en el contexto del paciente.
- Hipotensión: Ocurre en la mayoría de los pacientes con shock indiferenciado. Puede ser definida como presión arterial sistólica (PAS) < 90 mm Hg, presión arterial media (PAM) < 65 mm Hg o caída de la PAS en > 40 mm Hg. Es importante considerar que en el shock en estadio I, la hipotensión no está presente, por lo que la ausencia de hipotensión no es sinónimo de ausencia de shock. Pero si la hipotensión está presente, es un signo ominoso. Estudios sugieren que en pacientes con shock médico y traumático, la presencia de hipotensión al ingreso al SU tienen 3 a 4 veces más riesgo de mortalidad intrahospitalaria que aquellos sin hipotensión. (5,6)
- Taquipnea: Se define como FR > 20 rpm. Es un mecanismo compensatorio temprano en pacientes con shock y acidosis metabólica inicial. Si bien tiene el mismo problema que la taquicardia, ya que la taquipnea puede ser explicada por múltiples causas, debe hacer sospechar al médico de un posible shock indiferenciado o al menos de un paciente descompensado.
- Oliguria: Se define como una cantidad de eliminación de orina < 500 mL/hr o < 0.5 mL/kg/hr. En el shock se debe a la redistribución de flujo vascular hacia órganos nobles (corazón, cerebro, glándulas adrenales) con consecuente disminución de débito cardiaco hacia los riñones.
- Alteración del estado de consciencia: Puede ser cualitativo o cuantitativo. Se explica por una hipoperfusión cerebral.
- Disminución del llene capilar: Un llene capilar > 2 segundos se considera alterado y demuestra hipoperfusión periférica.
- Livideces: Es un signo clínico poco frecuente que ha demostrado ser un buen predictor de mortalidad en shock séptico. (7) Para su interpretación se utiliza el Mottling score como demuestra la figura N°1.
Pruebas diagnósticas:
- Hemoglucotest: Es un examen barato y rápido que puede entregar un diagnóstico preciso. Debe ser uno de los primeros exámenes en evaluar junto con el lactato.
- Lactato: niveles elevados reflejan una pobre perfusión distal debido al shock (acidosis láctica tipo A). Se considera elevado o en riesgo de hipoperfusión > 2 mmol/lt o > 18 mg/dL. Se considera insuficiencia circulatoria valores > 4 mmol/lt o > 36 mg/dL. Es el examen más importante, ya que es un criterio diagnóstico como se verá a continuación. Si está alterado, debe repetirse en 6 horas para evaluar la curva de lactato.
- Electrocardiograma: Es un examen de suma importancia. Junto con las enzimas cardiacas, pueden apoyar el diagnóstico etiológico de isquemia miocárdica, pero además puede evaluar taqui o bradiarritmias, signos de cardiomiopatías y enfermedad del pericardio, entre otras.
- Función renal: niveles de creatininemia y BUN deben solicitarse para evaluar la afectación renal.
- Electrolitos plasmáticos: Pueden estar alterados en el contexto de un paciente en shock hipovolémico.
- Recuento hematológico automatizado: Es un examen útil, ya que puede informar de hipovolemia si se observa un hematocrito alto que indique hemoconcentración y se puede encontrar anemia y trombocitopenia secundaria a hemorragia. La leucocitosis si bien puede indicar sepsis, es un hallazgo poco específico que también puede indicar otras causas de shock como la pancreatitis o el trauma.
- Pruebas de coagulación: Pueden verse afectadas en el contexto de un paciente séptico con una hemorragia importante, realizando el diagnóstico de coagulopatía intravascular diseminada (CID).
- Gases en sangre arterial: Se deben solicitar en todo paciente con shock indiferenciado para objetivar el nivel de oxigenación sanguíneo y para evaluar el equilibrio ácido-base.
- Pruebas hepáticas: Se deben solicitar para evaluar la repercusión orgánica del shock.
Exámenes complementarios
- Grupo sanguíneo y Rh: Se debe solicitar en todo paciente con antecedentes de trauma o sospecha de shock hemorrágico.
- Proteína C reactiva: Examen relevante con valor para el seguimiento del paciente. Si bien tiene alta sensibilidad, tiene baja especificidad, pues se eleva con varias de las etiologías del shock indiferenciado.
- Estudios microbiológicos de primera línea: En pacientes con sospecha de shock séptico, se debe solicitar dos hemocultivos de sangre periférica (al menos 8 mL por muestra), sedimento de orina, urocultivo (foco más frecuente en adultos mayores) y otros según clínica (cultivo de expectoraciones, cultivos de catéter, punción lumbar, etc). Cabe considerar que estos son exámenes que demoran al menos 24 horas en entregar un resultado, pero si se solicitan posterior al inicio de antibioterapia empírica, su rendimiento disminuye considerablemente.
- Enzimas cardiacas: Se deben solicitar en todo paciente, ya que pueden realizar el diagnóstico etiológico y orientar rápidamente la terapia definitiva del shock.
- Dímero D: Se puede solicitar si la sospecha de tromboembolismo pulmonar es baja. En caso de que exista una alta sospecha, se debe solicitar una tomografía computarizada (TAC) de tórax con angio para certificar el diagnóstico e iniciar el tratamiento precoz.
- Imágenes:
- Radiografía de tórax portátil: Se solicita en la mayoría de los pacientes que ingresan por shock. Se deben ir a buscar etiologías específicas como neumonía, neumotórax, hemotórax, congestión pulmonar o perforación de víscera hueca. En algunos casos como en el shock hipovolémico u obstructivo puede estar normal.
- Otras imágenes según la sospecha clínica: Se puede solicitar radiografía de abdomen, TAC de cerebro, médula, tórax, abdomen y/o pelvis.
- Ultrasonografía con protocolo RUSH: La ecografía es un examen rápido, barato, que se puede realizar en la cama del paciente sin la necesidad de movilizarlo y que ha sido cada vez más validado por la literatura en la evaluación inicial del shock indiferenciado y otros motivos de consulta. (8-14) La evaluación consta de la visualización de varios segmentos corporales según distintos protocolos (visualización de corazón, pericardio, vena cava inferior, pulmón y pleura, cavidad peritoneal, aorta y venas profundas de extremidades inferiores), los cuales si bien no son diagnósticos, se ha demostrado que en operadores entrenados en la técnica, disminuyen la incerteza y optimizan significativamente los recursos en el SU. Es relevante mencionar que la mayoría de la información disponible del uso de ultrasonografía en shock indiferenciado se extrapola de su uso en trauma. La información actual proviene de pequeños estudios que observacionales que han demostrado su uso en confirmar la sospecha clínica, favorecer un cambio de terapia y en detectar complicaciones de procedimientos, pero sin cambios en sobrevida y con una baja sensibilidad diagnóstica para algunas etiologías del shock indiferenciado. Por lo anterior, se debe considerar a esta técnica imagenológica sólo como un apoyo para la toma de decisiones.
Criterios de ingreso
El shock indiferenciado es una emergencia con riesgo vital, por lo que cada vez que se sospeche o se confirme este diagnóstico, el paciente debe ser estabilizado dentro de lo posible e ingresado a una unidad de paciente crítico según su estado posterior al manejo inicial, el resultado de los exámenes de laboratorio y los requerimientos específicos del paciente (monitorización central drogas vasoactivas, manejo avanzado de vía aérea, hemodiálisis de urgencia). (3)
3. Manejo
Terapia general
El manejo del shock indiferenciado se inicia en el momento de la instauración de las medidas básicas descritas en la valoración inicial. Posteriormente se procede a realizar un manejo general que incluye una monitorización, manejo ventilatorio, resucitación con volumen adecuada y agentes vasoactivos.
- Monitorización: Se debe indicar:
- Monitorización electrocardiográfica continua
- Oximetría de pulso
- Medición de presión arterial o línea arterial especialmente si se indican vasopresores,
- Medición de diuresis horaria con instalación de sonda Foley
- Medición seriada de lactato: Se debe medir a las 6 horas esperando un clearence de lactato de al menos un 20%. El valor de lactato tiene valor pronóstico (15-18)
En caso de no respuesta a terapia inicial a las 6 horas, se debe indicar (19):
- Medición de presión venosa central (PVC) con un catéter venoso central en casos de shock séptico, insuficiencia cardiaca o renal para guiar la terapia con objetivo de ≥ 8 mm Hg.
- Medición de la saturación venosa central (SvcO2): Objetivo ≥ 70%.
- Manejo ventilatorio: El aporte de oxígeno suplementario es una medida inicial básica en el manejo del shock indiferenciado. Si bien se puede intentar el uso de mascarillas y ventilación mecánica no invasiva (VMNI) como primera línea cuando no hay contraindicación, en general se prefiere la intubación endotraqueal (IT) como terapia inicial en todo paciente en shock que presente disnea severa, hipoxemia o persistencia o empeoramiento de acidemia, debido a que las otras formas de suplementación de oxígeno se asocian a mayor riesgo de falla de tratamiento y rápida progresión a paro cardiorrespiratorio (PR). Además, la IT tiene otros beneficios como proteger la vía aérea de la aspiración, disminuir el trabajo de los músculos respiratorios y disminuir la postcarga del VI por aumento de la presión intratorácica. (2,4)
- Resucitación con volumen: Es un pilar esencial en el manejo del shock indiferenciado, incluso en el shock cardiogénico. Es importante mantener una adecuada monitorización para evitar el riesgo de edema pulmonar agudo. El objetivo fisiopatológico que se busca es aumentar el volumen de fin de diástole del VI, es decir, aumentar la precarga para favorecer el gasto cardiaco siguiendo la ley de Frank Starling. La resucitación involucra 4 elementos que deben ser definidos previamente (2-4):
- Elección del fluido: Se eligen los cristaloides como primera opción, debido a sus escasos efectos adversos y su bajo precio. Los coloides, si bien han demostrado ser igual de efectivos que los cristaloides, se les deja como tratamiento de segunda línea por sus efectos adversos (reacciones anafilácticas, disminución de recuento plaquetario, prolongación de TTPA) y su precio. (20,21)
- Tasa de administración de fluidos: Debe ser una resucitación vigorosa en bolos de 500 mL pasados inicialmente entre 15-20 minutos endovenoso hasta completar 1-2 litros totales (o 30 mL/kg).
- Objetivo de resucitación: En general los objetivos son un aumento de la presión arterial para mantener una PAM 65-70 mm Hg, disminución de frecuencia cardiaca y aumento del débito urinario.
- Efectos adversos: El efecto adverso más importante de la terapia de resucitación es el edema pulmonar agudo. La monitorización con PVC se debe pensar en pacientes que no han respondido a la terapia en 1-2 horas.
- Agentes vasoactivos:
- Vasopresores: Se indican ante una hipotensión severa o refractaria a la terapia con volumen. La primera línea de tratamiento son los agonistas adrenérgicos por su rápido inicio de acción, alta potencia y baja vida media. Se usa la norepinefrina, la que tiene predominantemente efecto alfa adrenérgico pero con un modesto efecto beta agonista que mantiene el GC. La dosis inicial es 0.1-0.2 mcg/kg/min endovenoso. Otros agentes como la dobutamina o la epinefrina deben ser utilizados con cuidado, ya que presentan mayores efectos adversos y no han demostrado ser mejores que la norepinefrina. (22,23)
- Inotrópicos: La terapia de primera línea (que puede acompañar a la norepinefrina) es la dobutamina por su efecto predominantemente beta adrenérgico. La dosis inicial recomendada es 0.5-1 mcg/kg/min.
- Vasodilatadores: Al reducir la postcarga, podrían aumentar el GC sin aumentar la demanda miocárdica de oxígeno. Sin embargo, presentan un alto riesgo de hipotensión, por lo que los nitratos debieran usarse cuidadosamente sólo en algunos casos.
Terapia específica
Al mismo tiempo de realizar el manejo general, se debe iniciar el manejo específico por patología si es posible. Algunos ejemplos más relevantes de intervenciones se describen a continuación:
– Shock séptico: Se deben indicar antibióticos empíricos precozmente una vez obtenidas las muestras microbiológicas. Se puede iniciar cefalosporinas de tercera generación endovenoso si el riesgo de Pseudomonas es bajo. En cambio, si es alto, se recomienda iniciar vancomicina más otro antipseudomónico (quinolona, aminoglicósido, carbapenémico). Se ha demostrado que el uso precoz de los antibióticos se asocia a disminución de mortalidad en pacientes sépticos. (24)
– Infarto agudo miocárdico (IAM): Se debe indicar agentes antiplaquetarios y terapia de revascularización.
– Hemorragia traumática o no traumática: Se debe realizar ultrasonografía con protocolo FAST para evaluar sitio de sangrado y posteriormente ingreso a pabellón quirúrgico. En los casos en donde la etiología es un aneurisma abdominal roto o una hemorragia digestiva, la intervención quirúrgica suele ser también la mejor opción.
– Tromboembolismo pulmonar severo: Se debe indicar trombolisis endovenosa ya sea con estreptoquinasa 250.000 UI los primeros 30 minutos y luego 100.000 UI/hora por 24 horas o con alteplase (tPA) 100 mg en dos horas.
– Arritmias malignas: Puede ser bradi o taquiarritmias. Se deben solicitar exámenes generales para descartar la causa metabólica y administrar atropina o intentar cardiovertir eléctricamente según si es bradi o taquiarritmia respectivamente. En caso de presentar una causa metabólica como acidosis o hiperkalemia, debe manejarse precozmente.
– Shock anafiláctico: 0.3-0.5 mg intramuscular. En Chile la ampolla viene 1:1000, no es necesario diluirla. Se deben tomar un tercio o la mitad de la ampolla.
– Disección aórtica ascendente: Hipotensión y shock pueden presentarse en los casos de disección retrógrada que generen insuficiencia aórtica aguda, tamponamiento pericárdico o IAM. El paciente debe trasladarse rápidamente al pabellón quirúrgico.
– Neumotórax a tensión: Toracostomía de urgencia en el segundo espacio intercostal del hemitórax comprometido sobre la tercera costilla con aguja de descompresión (se puede utilizar una vía venosa gruesa), seguido posteriormente de instalación de pleurostomía en el quinto espacio intercostal.
– Tamponamiento pericárdico: Se debe realizar una pericardiocentesis guiada por ultrasonografía.
– Crisis adrenal: Se debe administrar volumen y dexametasona 4 mg endovenoso en 1-5 minutos y luego cada 12 horas.
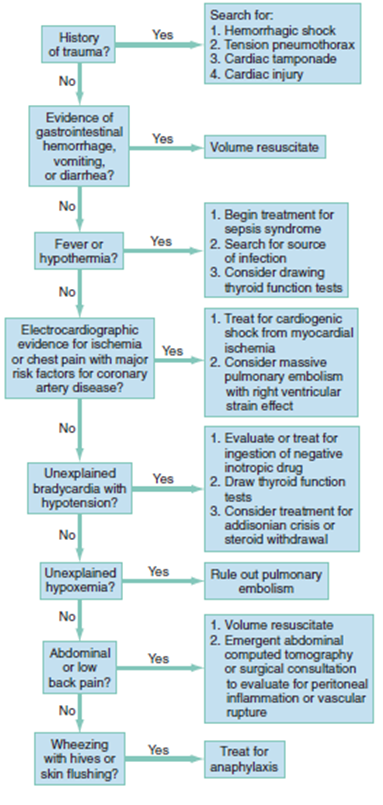
En la figura N°2 se adjunta un algoritmo de enfrentamiento etiológico-terapéutico. (4)
4. Conclusiones
El shock indiferenciado es un motivo de consulta importante en el SU debido a su alta mortalidad y la necesidad de instaurar medidas terapéuticas precoces. Su enfrentamiento inicial es estructurado y con alto nivel de sospecha. Se debe realizar el ABCDEU, buscando principalmente aquellos signos precoces que de shock tales como apariencia general, FC, FR, vasoconstricción periférica y otros signos de adrenergia. Por lo mismo, no se debe esperar la aparición de la hipotensión para la sospecha y las medidas terapéuticas. Además, dentro del mismo enfrentamiento, se deben incluir la medidas iniciales básicas (monitor, posición de Trendelenburg, oxígeno, dos vías venosas permeables, entre otras) y la solicitud de exámenes de laboratorio iniciales y complementarios según sospecha. Dentro de los exámenes generales, el más importante es el lactato y su recontrol (ya sea arterial o venoso), ya que tiene valor pronóstico.
Posteriormente y una vez completada la primera parte, se debe iniciar un manejo agresivo que contemple monitorización, manejo ventilatorio avanzado, resucitación con fluidos y agentes vasoactivos, teniendo metas claras de reanimación y un control clínico horario. Paralelamente, se debe clasificar el tipo del shock (hipovolémico, distributivo, cardiogénico, obstructivo o combinado) para orientar la etiología y el manejo específico.
Referencias
(1) Angus D, et al: Epidemiology of severe sepsis in the United States: Analysis of incidence, outcome, and associated costs of care. Crit Care Med 2001; 29:1303-1310.
(2) Vincent JL, De Backer D. Circulatory shock. N Engl J Med. 2013 Oct;369(18):1726-34.
(3) F.J. Montero Perez, J.M. Torres Murillo, J.A. vega Reyes, J.M. Dueñas Jurado, V. Torres Degayón, R. Lucchini Leiva y L. Jiménez Murillo. Capítulo 16: Shock. Sección 3 Urgencias cardiovasculares, pág 130-136.
(4) John A. Marx, Robert S. Hockberger, and Ron M. Walls. Rosen’s Emergency Medicine: Concepts and Clinical Practice8th edition, chapter 6: Shock, pag 34-41.
(5) Jones AE, Puskarich MA: Sepsis-induced tissue hypoperfusion. Crit Care Nurs Clin North Am 2011; 23:115-125. 23.
(6) Benington S, Ferris P, Nirmalan M: Emerging trends in minimally invasive haemodynamic monitoring and optimization of fluid therapy. Eur J Anaesthesiol 2009; 26:893-905.
(7) E Bastos de Moura, F Ferreira Amorim, C Darwin Silveira and M Oliveira Maia. Assessment of the mottling score as a mortality predictor in critically ill patients. Critical Care201317(Suppl 2):P217.
(8) Perera P, Mailhot T, Riley D, Mandavia D. The RUSH exam: Rapid Ultrasound in Shock in the evaluation of the critically lll. Emerg Med Clin North Am. 2010 Feb;28(1):29-56, vii.
(9) Bagheri-Hariri S, Yekesadat M, Farahmand S, Arbab M, Sedaghat M, Shahlafar N, Takzare A, Seyedhossieni-Davarani S, Nejati A. The impact of using RUSH protocol for diagnosing the type of unknown shock in the emergency department. Emerg Radiol. 2015 Oct;22(5):517-20.
(10) Atkinson PR, McAuley DJ, Kendall RJ, Abeyakoon O, Reid CG, Connolly J, Lewis D. Abdominal and Cardiac Evaluation with Sonography in Shock (ACES): an approach by emergency physicians for the use of ultrasound in patients with undifferentiated hypotension. Emerg Med J. 2009 Feb;26(2):87-91.
(11) Shokoohi H, Boniface KS, Pourmand A, Liu YT, Davison DL, Hawkins KD, Buhumaid RE, Salimian M, Yadav K. Bedside Ultrasound Reduces Diagnostic Uncertainty and Guides Resuscitation in Patients With Undifferentiated Hypotension. Crit Care Med. 2015 Dec;43(12):2562-2569.
(12) Mesterházi A, Barta M, Zubek L. Evaluation of the diagnostic value of bedside ultrasonography in the emergency care. Orv Hetil. 2016 Apr 10;157(15):569-74.
(13) Haydar SA, Moore ET, Higgins GL 3rd, Irish CB, Owens WB, Strout TD. Effect of bedside ultrasonography on the certainty of physician clinical decisionmaking for septic patients in the emergency department. Ann Emerg Med. 2012 Sep;60(3):346-58.e4.
(14) Jones AE, Tayal VS, Sullivan DM, Kline JA Randomized, controlled trial of immediate versus delayed goal-directed ultrasound to identify the cause of nontraumatic hypotension in emergency department patients. Crit Care Med. 2004 Aug;32(8):1703-8.
(15) Arnold, Ryan C.; Shapiro, Nathan I; Jones, Alan E.; Schorr, Christa; Pope, Jennifer; Casner, Elisabeth; Parrillo, Joseph E.; Dellinger, R. Phillip; Trzeciak, Stephen. MULTICENTER STUDY OF EARLY LACTATE CLEARANCE AS A DETERMINANT OF SURVIVAL IN PATIENTS WITH PRESUMED SEPSIS. Shock, 2009, (32), 1, pp 35-39
(16) Nathan I. Shapiro, MD, MPH, Michael D. Howell, MD, Daniel Talmor, MD, MPH, Larry A. Nathanson, MD, Alan Lisbon, MD, Richard E. Wolfe, MD, J. Woodrow Weiss, MD. Serum Lactate as a Predictor of Mortality in Emergency Department Patients with Infection. Annals of Emergency Medicine, 2005, 45 (5) , pp. 524-528.
(17) Vincent JL, Dufaye P, Berré J, Leeman M, Degaute JP, Kahn RJ. Serial lactate determinations during circulatory shock. Crit Care Med 1983;11:449-51.
(18) Jansen TC, van Bommel J, Schoonderbeek FJ, et al. Early lactate-guided therapy in intensive care unit patients: a multicenter, open-label, randomized controlled trial. Am J Respir Crit Care Med 2010;182:752-61.
(19) R. Phillip Dellinger, MD et al. Surviving Sepsis Campaign, International Guidelines for Management of Severe Sepsis and Septic Shock: 2012. Critical Care Medicine, 2013, 41, Number 2
(20) Finfer S, Bellomo R, Boyce N, French J, Myburgh J, Norton R, SAFE Study Investigators. A comparison of albumin and saline for fluid resuscitation in the intensive care unit. N Engl J Med. 2004;350(22):2247.
(21) Virgilio RW, Rice CL, Smith DE, James DR, Zarins CK, Hobelmann CF, Peters RM. Crystalloid vs. colloid resuscitation: is one better? A randomized clinical study. Surgery. 1979;85(2):129.
(22) De Backer D, Aldecoa C, Njimi H, Vincent JL. Dopamine versus norepinephrine in the treatment of septic shock: a metaanalysis. Crit Care Med 2012;40:725-30.
(23) Myburgh JA, Higgins A, Jovanovska A, Lipman J, Ramakrishnan N, Santamaria J. A comparison of epinephrine and norepinephrine in critically ill patients. Intensive Care Med 2008;34:2226-34.
(24) Gaieski, David F. MD; Mikkelsen, Mark E. MD, MSCE; Band, Roger A. MD; Pines, Jesse M. MD, MBA, MSCE; Massone, Richard MD; Furia, Frances F. MD; Shofer, Frances S. PhD; Goyal, Munish MD. Impact of time to antibiotics on survival in patients with severe sepsis or septic shock in whom early goal-directed therapy was initiated in the emergency department. Critical Care Medicine:2010 (38)4, pp 1045-1053
Anexos
Tabla 1: Subdivisiones y etiologías más frecuentes de los 4 diferentes tipos de shock
| Tipo de shock | Subdivisión | Causas |
| Hipovolémico | Hemorrágico | Trauma, hemorragia digestiva, sangrado intra y post operatorio, pancreatitis hemorrágica, disección aórtica, hemorragia postparto, hemorragia traumática |
| No hemorrágico | Pérdidas gastrointestinales (diarrea, vómito), pérdidas cutáneas (ataques de calor, gran quemado, enfermedades dermatológicas extensas, pérdidas renales (diuresis osmótica, nefropatía perdedora de sal, hipoaldosteronismo), pérdidas por tercer espacio (trauma, obstrucción intestinal, peritonitis, cirrosis, síndrome nefrótico, insuficiencia cardiaca descompensada) | |
| Distributivo | Séptico | Gram (+), Gram (-), fúngico, viral, parasitario |
| No séptico | Shock inflamatorio con síndrome de respuesta inflamatoria sistémica (SIRS) (secundario a trauma, pancreatitis, post infarto, embolia aérea o grasa, síndrome de leak capilar idiopático), shock neurogénico (lesión cerebral traumática, lesión medular, disfunción mitocondrial), shock anafiláctico (picadura de abeja, alimentos, fármacos), drogas y toxinas (sobredosis de narcóticos, mordidas de insecto, reacciones transfusionales, intoxicación por metales pesados o monóxido de carbono), shock endocrino (crisis adrenal, coma mixedematoso) | |
| Cardiogénico | Cardiopático | Infarto anterior o derecho extenso, insuficiencia cardiaca descompensada severa, shock séptico avanzado, miocarditis |
| Arritmogénico |
Taquiarritmias (fibrilación auricular, flutter auricular, taquicardia de reentrada, taquicardia, ventricular y fibrilación ventricular) Bradiarritmias (Bloqueo del nodo AV completo o Mobitz II) |
|
| Mecánico | Insuficiencia mitral o aórtica severa, rotura valvular aguda, estenosis aórtica crítica, rotura de aneurisma de pared ventricular, mixoma atrial | |
| Obstructivo | Pulmonar | Tromboembolismo pulmonar severo, hipertensión pulmonar severa, obstrucción aguda de la válvula tricúspide o pulmonar |
| Mecánico | Neumotórax a tensión (trauma, iatrogénico), tamponamiento pericárdico, pericarditis constrictiva, cardiomiopatía restrictiva | |
| Combinado | Muchas formas de shock pueden coexistir. Por ejemplo, hipovolemia puede inducir o coexistir con un shock cardiogénico, presentado una clínica incompatible como fracción de eyección disminuida y mucosas deshidratadas, vena cava inferior colapsable. La clave en estos casos es la respuesta a terapias empíricas. |
Tabla N°2: Clasificación de shock según terapia inicial
| Causas que requieren infusión de volumen | Shock hemorrágico (traumático, hemorragia digestiva, sangrado a cavidad interna) |
| Hipovolemia (pérdidas gastrointestinales, deshidratación severa, secuestro por tercer espacio) | |
|
Causas que requieren mejoría de bomba cardiaca ya sea por soporte inotrópico o reversión de la descompensante cardiaca
|
Isquemia miocárdica (trombosis de arteria coronaria, hipotensión e hipoxemia) |
| Cardiomiopatía (miocarditis aguda, cardiopatía isquémica, diabética, infiltrativa, endocrinológica o congénita) | |
| Arritmias (Fibrilación auricular con respuesta ventricular rápida, taquicardia supraventricular, taquicardia ventricular) | |
| Shock séptico hipodinámico | |
| Sobredosis de drogas inótropas negativas (betabloqueadores, antagonistas del calcio no dihidropiridínicos) | |
| Daño cardiaco estructural (traumático, rotura ventriculoseptal o de músculo papilar) | |
| Causas que requieren soporte de volumen y vasopresores | Shock séptico hiperdinámico |
| Shock anafiláctico | |
| Shock neurogénico central | |
| Sobredosis de drogas | |
| Causas que requieren intervención urgente de la obstrucción al gasto cardiaco | Tromboembolismo pulmonar |
| Tamponamiento cardiaco | |
| Neumotórax | |
| Disfunción valvular (trombosis aguda de válvula protésica, estenosis aórtica crítica) | |
| Intoxicaciones que requieren un antídoto específico | Monóxido de carbono |
| Metahemoglobinemia | |
| Sulfuro de hidrógeno | |
| Cianuro |